Витамин D - Кальциферол, эргостерол, виостерол
Мы приобретаем его посредством солнечного света или с пищей. Ультрафиолетовые лучи действуют на масла кожи, способствуя образованию этого витамина, который затем всасывается в тело. Витамин D образуется в коже под действием солнечных лучей из провитаминов. Провитамины, в свою очередь, частично поступают в организме в готовом виде из растений (эргостерин, стигмастерин и ситостерин), а частично образуются в тканях их холестерина (7-дегидрохолестерин (провитамин витамина D 3).
Кроме того, половые гормоны, пролактин, гормон роста и инсулиноподобный фактор роста 1 увеличивают почечную продукцию активного метаболита. Напротив, гиперкальциемия уменьшает синтез витамина. Кроме того, снижение фосфатемии увеличивается, и ее увеличение снижает производство активного витамина. Полученная величина указывает, достаточны ли достаточные количества или недостаточность ингаляции. По этой причине в настоящее время считается, что отложения этого витамина достаточны, если их концентрация в плазме выше этого значения4.
Потребности в питании определяются как количество каждого из питательных веществ, которое физическое лицо нуждается в оптимальном состоянии здоровья. Они варьируются в зависимости от возраста, пола и физиологических характеристик, таких как беременность и лактация.
При приеме внутрь, витамин D всасывается с жирами через стенки желудка.
Измеряется в Международных Единицах (МЕ). Дневная доза для взрослых составляет 400 МЕ или 5-10 мкг. После получения загара, выработка витамина D через кожу прекращается.
Польза: Должным образом утилизирует кальций и фосфор, необходимые для укрепления костей и зубов. При совместном приеме с витаминами А и С помогает в профилактике простудных заболеваний. Помогает в лечении конъюнктивитов.
Хотя рекомендуемое потребление относится к среднесуточному потреблению, которое должен достичь человек, количество принимаемого внутрь может меняться со дня на день. Как правило, потребление оценивается в течение 7-15 дней, таким образом, что с течением времени количество потребляемого вещества совпадает с рекомендациями.
Когда возрастает потребность в витамине D?
Кроме того, для некоторых питательных веществ было установлено максимальное безопасное потребление или максимально допустимое потребление. Это относится к уровню потребления, выше которого может быть риск для здоровья. Длительное или обширное воздействие на организм не показало избыточного производства холекальциферола на уровнях, способных вызвать интоксикацию.
Заболевания, вызываемые дефицитом витамина D: рахит, сильное разрушение зубов, остеомаляция*, старческий остеопороз.
Витамин D относится к группе жирорастворимых витаминов, обладающих антирахитическим действием (D 1 , D 2 , D 3 , D 4 , D 5)
К витаминам группы D относятся:
витамин D 2 - эргокальциферол; выделен из дрожжей, его провитамином является эргостерин; витамин D 3 - холекальциферол; выделен из тканей животных, его провитамин - 7-дегидрохолестерин; витамин D 4 - 22, 23-дигидро-эргокальциферол; витамин D 5 - 24-этилхолекальциферол (ситокальциферол); выделен из масел пшеницы; итамин D 6 - 22-дигидроэтилкальциферол (стигма-кальциферол).
Во-первых, это зависит от количества 7-дегидрохолестерина в эпидермисе. У пожилых людей более низкое количество 7-дегидрохолестерина в коже. Во-вторых, это зависит от количества меланина. Люди с более высоким содержанием меланина требуют более длительного воздействия солнца на синтез того же количества холекальциферола. Это связано с тем, что меланин поглощает солнечные фотоны. Аналогично, кремы с солнечной защитой поглощают излучение, прежде чем проникать в кожу. Кремы с коэффициентом защиты 15 уменьшают их емкость более чем на 98%.
Зимой солнечные лучи проникают в землю под углом более наклонный. В этой ситуации больше фотонов поглощается озоновым слоем. Точно так же, в первые часы утра и последний день, угол, с которым солнечные лучи проникают в землю, более наклонный. В широтах более 37 ° севернее и южнее экватора, особенно в зимние месяцы, число фотонов, достигающих земной поверхности, ниже. Однако известно, что если воздействие солнца вызывает небольшую эритему, и сразу после применения солнцезащитного крема, риск для кожи минимален.
Сегодня витамином D называют два витамина - D 2 и D 3 - эргокальциферол и холекальциферол - это кристаллы без цвета и запаха, устойчивые в воздействию высоких температур. Эти витамины являются жирорастворимыми, т.е. растворяются в жирах и органических соединениях и нерастворимы в воде.
Регулируют обмен кальция и фосфора: участвуют в процессе всасывания кальция в кишечнике, взаимодействуют с паратиреоидным гормоном, отвечают за кальцификацию костей.В детском возрасте при авитаминозе D вследствие уменьшения содержания в костях солей кальция и фосфора нарушается процесс костеобразования (рост и окостенение), развивается рахит. У взрослых происходит декальцификация костей (остеомаляция).
Жирные кислоты морских рыб представляют собой богатейший источник колекальциферола, причем основным источником является лосось, поскольку он наиболее часто потребляется. Яйца, масло, печень и другие внутренние органы также являются продуктами, которые содержат витамин, но его потребление низкое из-за его высокого содержания холестерина. В таблице 3 показано содержание холекальциферола в пищевых группах.
Соки, молоко и другие молочные продукты обогащены кальцием. Пищевая промышленность использует как эргокальциферол, так и колекальциферол для обогащения пищевых продуктов, хотя использование последних чаще. Содержание витамина не выражается в микрограммах или международных единицах, а в процентах от адекватного потребления для взрослых людей 11.
Немецкий химик А. Виндаус, более 30 лет изучавший стерины, в 1928 году обнаружил эргостерол - провитамин D, превращавшийся под действием ультрафиолетовых лучей в эргокальциферол Было выяснено, что под влиянием ультрафиолетовых лучей некоторое количество витамина D может образовываться в коже, причем облучение может быть как солнечным, так и с помощью кварцевой лампы. . Подсчитано, что 10-минутное облучение животных оказывает на организм такое же действие, как введение в рацион 21 % рыбьего жира. В облученных продуктах витамин D образуется из особых жироподобных веществ (стеринов). В последнее время в животноводстве широко используют ультрафиолетовое облучение животных, особенно молодняка, а также кормов.
Некоторые молочные продукты, особенно обезжиренное и полумешенное молоко, некоторые соки и злаки обогащены разным количеством витамина. Хотя обогащение пищи показало свою полезность в увеличении потребления этого витамина в популяции, как это делается в настоящее время, оно имеет некоторые недостатки. С одной стороны, молоко обогащается главным образом. Тем не менее, молоко не является пищей, равномерно потребляемой всем населением, особенно потребление людей с высоким уровнем риска, таких как афроамериканская раса и вегетарианцы.
Кроме того, в последние годы наблюдается тенденция к снижению потребления молока у населения. Этот недостаток можно преодолеть за счет укрепления всех молочных продуктов, включая йогурты, сыры и другие молочные продукты. Остальные презентации, содержащие витамин, связанный с другими витаминами и минералами, не указаны, поскольку существует много препаратов. Следует помнить, что у лиц с хроническим заболеванием печени происходит значительное изменение активности 25-гидроксилазы печени, поэтому лучше вводить кальцифедиол вместо холекальциферола.
Основные источники: рыбий жир, икра, печень и мясо, яичный желток, животные жиры и масла, сардины, сельдь, лосось, тунец, молоко. сенной муке, Витамин D содержится в большом количестве и в яичном желтке, дрожжах, хорошем сене, растительном масле, травяной муке и других продуктах. В растениях витамина, как правило, нет, но в них содержится его провитамин эргостерол, который в организме животных превращается в витамин D.
Неблагоприятные последствия этих препаратов недостаточны. При длительном лечении и при высоких дозах возможно появление гиперкальциемии, чего избегают путем корректировки дозы в соответствии с рекомендациями приема внутрь для населения и корректируется путем приостановки введения препарата. Потребление зависит не только от возраста, но и от пола, расы и факта специальных диет.
По возрасту население с наибольшим риском дефицита - это пожилые люди. С возрастом уровни 7-дегидрохолестерина в коже снижаются, воздействие на солнце ниже, а способность кожного синтеза колекальциферола на 25% ниже. Однако в этом возрасте потребление витаминных и минеральных добавок выше, по крайней мере, у американского населения14. Однако женщины старше 50 лет чаще потребляют питательные вещества, обогащенные витамином15. Причина двоякая: с одной стороны, большее количество меланина в коже частично поглощает ультрафиолетовые лучи, уменьшая кожный синтез витамина, а с другой стороны, непереносимость лактозы чаще встречается у этой группы индивидуумов, поэтому что потребление молока ниже.
Суточная потребность 2,5 мкг, для детей и беременных - 10 мкг. Отрицательно влияют на усвоение витамина D расстройства кишечника и печени, дисфункция желчного пузыря.
У беременных и кормящих животных потребность в витамине D повышается, т.к. необходимо дополнительное количество его для предупреждения рахита у детей.
Действие
Витамин D содержится в продуктах
Наконец, строгие вегетарианские индивидуумы, как правило, имеют низкие гормональные отложения. Эти проценты ниже, чем другие национальности17. Это значение обнаружено у примерно 50% пациентов, которые госпитализированы с острым переломом шейки бедра. Однако его присутствие было обнаружено почти во всех клетках организма, включая мозг, сердце, кожу, бета-клетки поджелудочной железы, гонады, предстательную железу, молочную железу, ободочную кишку и клетки иммунной системы. В результате увеличивается производство и созревание остеокластов и высвобождение соляной кислоты и коллагеназ.
Основная функция витамина D - обеспечение нормального роста и развития костей, предупреждение рахита и остеопороза. Он регулирует минеральный обмен и способствует отложению кальция в костной ткани и дентине, таким образом, препятствуя остеомаляции (размягчению) костей.
Поступая в организм, витамин D всасывается в проксимальном отделе тонкого кишечника, причем обязательно в присутствии желчи. Часть его абсорбируется в средних отделах тонкой кишки, незначительная часть - в подвздошной. После всасывания кальциферол обнаруживается в составе хиломикронов в свободном виде и лишь частично в форме эфира. Биодоступность составляет 60-90%.
Все это приводит к мобилизации кальция из костных отложений, поэтому концентрация кальция в плазме в норме. Кроме того, вторичный гиперпаратиреоз индуцирует потерю фосфора в моче, уменьшая уровни электролита в плазме. Результатом является неадекватный продукт кальция-фосфор, который способствует дефекту минерализации костной матрицы. Появляется замедление роста, деформация кости, особенно длинных костей, и повышенный риск перелома23. У взрослого человека с наибольшим присутствием минерализованной кости деформации кости не происходят.
Витамин D влияет на общий обмен веществ при метаболизме Ca2+ и фосфата (НРО2-4). Прежде всего, он стимулирует всасывание из кишечника кальция, фосфатов и магния. Важным эффектом витамина при этом процессе является повышение проницаемости эпителия кишечника для Ca2+ и Р.
Витамин D является уникальным - это единственный витамин, действующий и как витамин, и как гормон. Как витамин он поддерживает уровень неорганического Р и Са в плазме крови выше порогового значения и повышает всасывание Са в тонкой кишке.
Однако остеоид не минерализуется должным образом, что приводит к остеомаляции. Как и при остеопорозе, у пациентов с остеомалязией низкая минеральная плотность костной ткани, измеренная рентгеновской денситометрией с двойной энергией, и повышенный риск перелома. В отличие от остеопороза, остеомаляция вызывает генерализованную боль в костях и проксимальную мышечную слабость. Иногда из-за присутствия боли болезнь путается с миозитом, фибромиалгией или синдромом хронической усталости24.
Кроме того, существует исследование, в котором показано снижение риска падения у пожилых людей35. Сегодня мы знаем, что витамин оказывает множество функций не только на уровне костей, но и во многих местах организма. Однако обогащения молока, как это делается сегодня, недостаточно. Он образуется на коже с воздействием ультрафиолетовых лучей в достаточном количестве, чтобы покрыть повседневные потребности.
В качестве гормона действует активный метаболит витамина D - 1,25-диоксихолекациферол, образующийся в почках. Он оказывает влияние на клетки кишечника, почек и мышц: в кишечнике стимулирует выработку белка-носителя, необходимого для транспорта кальция, а в почках и мышцах усиливает реабсорбцию Ca++.
Витамин D 3 влияет на ядра клеток-мишеней и стимулирует транскрипцию ДНК и РНК, что сопровождается усилением синтеза специфических протеидов.
Если мы берем солнце время от времени, нам не нужно искать его в рационе. Он действует вместе с гормональным параторидом и кальцитонином при абсорбции кальция и фосфора. Фармакологические основы терапии. Некоторые исследователи полагали, что болезнь вызвана нехваткой свежего воздуха и солнечного света; другие утверждали, что болезнь зависит от фактора в рационе.
Мелланби и Хулдщинский показали, что обе идеи были правильными; добавление масла трески в рацион или воздействие солнечного света предотвращало болезнь или вылечивало ее. Эти наблюдения привели к выяснению структур коллекальциферола и эргокальциферола и, в конечном счете, к открытию того, что эти соединения требуют дополнительной обработки в организме, чтобы стать активными. Основным провитамином, обнаруженным в тканях животных, является 7-дегидрохолестерин, который синтезируется в коже. Воздействие кожи на солнечный свет превращает 7-дегидрохолестерин в холекальциферол.
Однако роль витамина D не ограничивается защитой костей, от него зависит восприимчивость организма к кожным заболеваниям, болезням сердца и раку. В географических областях, где пища бедна витамином D, повышена заболеваемость атеросклерозом, артритами, диабетом, особенно юношеским.
Он предупреждает слабость мускулов, повышает иммунитет (уровень витамина D в крови служит одним из критериев оценки ожидаемой продолжительной жизни больных СПИДом), необходим для функционирования щитовидной железы и нормальной свертываемости крови.
Конечная активация кальцитриола происходит главным образом в почках, но также имеет место в плаценте и почках. децидуас, а также в макрофагах. Почвы являются преобладающим источником кальцитриола в кровообращении. Ферментная система, ответственная за 1-гидроксилирование 25-гидроксихолекальциферола, связана с митохондриями в проксимальных канальцах. Регулирование является как хроническим, так и острым. Имеются данные о том, что гипокальцемия может непосредственно активировать гидроксилазу, а также косвенно влиять на нее, вызывая секрецию паратиреоидного гормона.
Так, при наружном применении витамина D 3 уменьшается характерная для псориаза чешуйчатость кожи.
Есть данные, что, улучшая усвоение кальция и магния, витамин D помогает организму восстанавливать защитные оболочки, окружающие нервы, поэтому он включается в комплексную терапию рассеянного склероза.
Витамин D 3 участвует в регуляции артериального давления (в частности, при гипертонии у беременных) и сердцебиения.
Гипофосфатемия значительно увеличивает активность гидроксилазы. Кальцитриол оказывает контроль отрицательной обратной связью фермента, что отражает прямое действие на почки, а также ингибирование производства паратиреоидного гормона. Характер регуляторных механизмов эстрогена и пролактина на 1а-гидроксилазе неизвестен. Витамин влияет на метаболизм фосфата параллельно методу Са 2. Механизм действия кальцитриола похож на механизм действия стероидных и тиреоидных гормонов. Структурный анализ рецептора кальцитриола указывает на то, что он относится к тому же семейству супергенов, что и рецепторы стероидов и тиреоидных гормонов.
Витамин D препятствует росту раковых и клеток, что делает его эффективным в профилактике и лечении рака груди, яичников, предстательной железы, головного мозга, а также лейкимии.
Гиповитаминоз. Недостаток витамина Д у детей приводит к заболеванию рахитам. Основные проявления этого заболевания сводятся к симптоматике недостаточности кальция. Прежде всего страдает остеогенез: отмечается деформация скелета конечностей (искривление их в результате размягчения - остеомаляции), черепа (позднее заращение родничков), грудной клетки (появление своеобразных «четок» на костно-хрящевой границе ребер), задерживается прорезывание зубов. Развивается гипотония мышц (увеличенный живот), возрастает нервно-мышечная возбудимость (у младенца выявляется симптом облысения затылочка из-за частого вращения головкой), возможно появление судорог, У взрослого недостаточность кальция в организме приводит к кариесу и остеомаляции; у пожилых - к развитию остеопороза (снижение плотности костной ткани вследствие нарушения остеосинтеза), Разрушение неорганического матрикса объясняется усиленным «вымыванием» кальция из костной ткани и нарушением реабсорбции кальция в почечных канальцах при дефиците витамина Д.
Кальцитриол также, по-видимому, оказывает влияние, которое происходит настолько быстро, что их интерпретируют как слишком быстрые явления, что объясняется геномными действиями. Рисунок 17: Структуры 7-дегидрохолестерина, эргостерина, холекальциферола и эргокальциферола.
Его дефицит вызывает рахит, остеопороз и остеомаляцию, с декальцификацией кости, которая деформируется даже при сохранении той же массы. Отсутствие роста у детей и деформации скелета у взрослых может возникать во время беременности и лактации, с симптомами боли в пояснице, спазма и мышечной слабости, деформации позвоночника и таза.
На схеме ниже показано угнетение (пунктирная стрелка) всасывания, снижение поступления кальция в кость и уменьшение экскреции кальция при недостатке витамина Д. Одновременно в ответ на гипокальциемию секретируется паратирин и увеличивается (сплошная стрелка) поступление кальция из кости в кровяное русло (вторичный гиперпаратиреоидизм).
Симптомы гиповитаминоза
Основным признаком недостаточности витамина D является рахит и размягчение костей (остеомаляция).
Более легкие формы дефицита витамина D проявляются такими симптомами как:
потеря аппетита, снижение веса,
ощущение жжения во рту и в горле,
бессонница,
ухудшение зрения.
Рахит - одна из самых распространенных детских болезней - известен с незапамятных времен. Картины фламандских художников с изображением детей с искривленными позвоночниками, руками и ногами ясно указывают на распространение рахита в 15 веке. Широкое распространение рахит получил в Великобритании - его еще стали называть «английская болезнь». Как стало известно позднее, для активации антирахитического витамина необходим ультрафиолет, поэтому очагами рахита стали крупные города с тесной застройкой и задымлением. При рахите наиболее резко выражены нарушения в костях ног, грудной клетке, позвоночнике и черепе. Хрящевая и костная ткани становятся ненормально мягкими, что приводит к их деформации и искривлению. Заболевание рахитом возможно и при достаточном содержании витамина в пище, но при нарушении его всасывания в пищеварительном тракте (расстройства пищеварения в раннем возрасте).
При недостатке витамина D у животных снижается содержание кальция и фосфора в крови, пропадает аппетит, нарушается работа органов дыхания, задерживается рост, появляется размягчение конечностей, ломкость костей. Иногда возникают судороги мышц головы, шеи и конечностей. Наиболее выраженным рахит бывает у молодых животных. Давно известно, что рахит хорошо лечить рыбьим жиром.
Гипервитаминоз Д. Достаточно опасен гипервитаминоз D (возникает при дозах, превышающих лечебные во много раз), т. к. при этом возникает гиперкальцемия организма и обызвествление внутренних органов: почек, желудка, легких, крупных кровеносных сосудов. Избыток витамина D откладывается в печени и может вызвать отравление.
Избыточный прием витамина Д приводит к интоксикации и сопровождается выраженной деминерализацией костей - вплоть до их переломов. Содержание кальция в крови повышается. Это приводит к кальцификации мягких тканей, особенно склонны к этому процессу почки (образуются камни и развивается почечная недостаточность), Повышение уровня кальция (и фосфора) в крови объясняется следующим: 1) резорбцией костной ткани (сплошная стрелка); 2) увеличением интенсивности всасывания кальция и фосфора в кишечнике 3) увеличением их рсабсорбции в почках (т. е. угнетением экскреции с мочой - пунктир).

В нормальных условиях повышение содержания кальция в крови будет приводить к образованию неактивного 24,25(0 Н)2-Д3, который не выбывает резорбцию («рассасывание») кости, однако при гипервитаминозе Д этот механизм становится неэффективным/ Интересно, что пигментация кожи (загар) является защитным фактором, предохраняющим от избыточного образования витамина Д при УФ-облучении кожи. Однако у светлокожих жителей северных стран, испытывающих недостаток солнечной инсоляции, витамин-Д-дефицитные состояния, как правило, не развиваются, так как их диета включает рыбий жир.
Метаболизм. Витамины группы Д всасываются подобно витамину А. В печени витамины подвергаются гидроксилированию микросомной системой оксигеназ по С-25 (из витамина Д. образуется 25(ОН)-Д3, т. е. 25-гидроксихолекальциферол), и затем переносятся током крови с помощью специфического транспортного белка в почки. В почках осуществляется вторая реакция гидроксилирования по С-1 с помощью митохондриальных оксигеназ (образуется 1,25(ОН)2-Д3, т. е. 1,25-дигидроксихолекальциферол, или кальцитриол). Эта реакция активируется паратиреоидным гормоном, секретируемым паращитовидной железой, когда уровень кальция в крови снижается. Если уровень кальция адекватен физиологической потребности организма, вторичное гидроксилирование происходит по С-24 (вместо С-1), при этом образуется неактивный метаболит 1,24(ОН)2-Д3 В реакциях гидроксилирования принимает участие витамин С.

Витамин Д3, накапливается в жировой ткани. Выводится главным образом с калом в неизмененном или окисленном виде, а также в виде конъюгатов.
Витамин Н - Биотин, коэнзим R
Витамин Н водорастворим, сравнительно новый член семействавитаминов группы В .
Биотин нужен для синтеза аскорбиновой кислоты. Необходим для нормального метаболизма жиров и белка.
РНП для взрослых 150 – 300 мкг. Может синтезироваться кишечными бактериями. Сырые яйца препятствуют его усвоению организмом. Синергичен с витаминами В2, В6, ниацином, А и сохраняет кожу здоровой.
Польза: Помогает предохранить волосы от седины. Облегчает боли в мышцах. Уменьшает проявления экземы и дерматита.
Заболевания, вызываемые дефицитом биотина: нарушение метаболизма жиров.
Лучшие натуральные источники: орехи, фрукты, пивные дрожжи, говяжья печень, молоко, почки и нешлифованный рис, желток яйца.
В 1935-1936 гг. Kogi и Tonnies впервые выделили кристаллический биотин из желтка яиц. Для этой цели они использовали 250 кг желтков яиц и получили 100 мг биотина с температурой плавления 148°.
Известны аминокислотные производные биотина, среди которых наиболее
изучен биоцитин, обладающий высокой активностью для многих микроорганизмов.
Он представляет собой пептид биотина и лизина. В настоящее время выяснена причина патологических изменений, возникающих при кормлении животных сырым яичным белком. В нем содержится авидин-белок, который специфически соединяется с биотином (введенным внутрь с пищевыми продуктами или синтезированным кишечными микроорганизмами) в неактивный комплекс и тем самым препятствует его всасыванию.
Рекордное количество (6,81 мкг/г) найдено в печени акулы.
Наиболее богаты витамином печень, почки, надпочечники; сердце и желудок содержат среднее, а мозговая ткань, легкие и скелетные мышцы-минимальное количество биотина.
Наиболее богаты витаминами свиная и говяжья печень, почки, сердце быка, яичный желток, а из продуктов растительного происхождения-бобы, рисовые отруби, пшеничная мука и цветная капуста. В животных тканях и дрожжах биотин находится преимущественно в связанном с белками виде, в овощах и фруктах-в свободном состоянии.
Биосинтез биотина .
Биосинтез биотина осуществляют все зеленые растения, некоторые бактерии
и грибы. Изучение путей биосинтеза биотина началось после выяснения строения его молекулы. Химическое расщепление биотина проходит через образование дестиобиотина, диаминопеларгоновой кислоты и, наконец, пимелиновой кислоты.
Взаимодействие с другими витаминами.
Установлена связь биотина с другими витаминами, в частности с фолиевой кислотой, витамином B12 - аскорбиновой кислотой, тиамином и пантотеновой кислотой. 0собенно тесные взаимоотношения существуют между биотином и фолиевой кислотой. Биотин благоприятно влияет на общее состояние организма и сохранение аскорбиновой кислоты в тканях цинготных морских свинок. В свою очередь аскорбиновая кислота замедляет, хотя и не предотвращает развитие авитаминоза биотина у крыс.
При недостаточности биотина снижается содержание тиамина в печени, селезенке,. почках и мозге животных. У крыс, содержавшихся на рационе, лишенном биотина, содержание витамина B12 было выше, чем у контрольных животных, получавших биотин. Эти два витамина тесно связаны между собой в обмене пропионовой кислоты у микроорганизмов и животных. Существует тесная связь между биосинтезом биотина и пантотеновой кислоты у микроорганизмов и зеленых растений (В. В. Филиппов, 1962). Биотин облегчает симптомы пантотеновой недостаточности и, наоборот, пантотеновая кислота смягчает проявление авитаминоза биотина.
Биотиновый авитаминоз у животных характеризуется прекращением роста и падением веса тела (до 40%), покраснением и шелушением кожи, выпадением шерсти или перьев, образованием красного отечного ободка вокруг глаз в виде «очков», атактической походкой, отеком лапок и типичной позой животного с согбенной (кенгу-руподобной) спиной. Дерматит, который развивается у животных при недостаточности биотина, может быть охарактеризован как себорея десквамационного типа, сходная с той, которая наблюдается у детей.
У крыс авитаминоз биотина развивается через 4-5 недель скармливания опытного рациона, а у цыплят первые признаки авитаминоза появляются через 3 недели.
Помимо внешних признаков, биотиновый авитаминоз вызывает глубокие морфологические изменения в тканях и органах, а также нарушения в обмене веществ. Известны изменения в зобной железе, коже и мышцах крыс. Характерны обильный гиперкератоз, акантез и отеки. Разрушенные волосяные стволы перемешаны с гиперкератозными пластинками. Установлено расширение волосяных сумок, отверстия которых закупорены гиперкератозным материалом. В последней фазе развития авитаминоза наблюдается атрофия жира в гиперкератозных пластинках. Недостаток биотина в рационе крыс приводит к уменьшению его содержания в тканях. В печени и мышцах количество витамина снижается в 5 раз, а в мозговой ткани-на 15%. В крови авитаминозных крыс накапливается пировиноградная кислота, развивается ацидоз и снижается концентрация сахара. При этом глюкозурия не наблюдается, но уменьшается содержание редуцирующих Сахаров в печени при нормальном содержании их в мышцах; у животных развивается креа-тинурия.
Человек полностью удовлетворяет свою потребность в биотине за счет синтеза его микрофлорой кишечника, поэтому гиповитаминоз можно получить только в эксперименте.
Гиповитаминоз может развиться в основном при дисбактериозе кишечника, возникающего, например, в результате приема антибиотиков.
Симптомы гиповитаминоза
Возможные последствия дефицита биотина: себорейный дерматит, анемия, депрессия, потеря волос, высокий уровень сахара в крови, воспаление или бледность кожи и слизистых оболочек, бессонница, потеря аппетита, мышечные боли, тошнота, воспаление языка, сухая кожа, высокий уровень холестерина в крови.
Взаимодействие
* Сырой яичный белок содержит вещество, которое называется авидин - антивитамин биотина. Это вещество связывает биотин и препятствует его всасыванию в кровь. При нагревании происходит денатурация (необратимое нарушение структуры) авидина в яичном белке, и поэтому приготовленные яйца не мешают усваивать биотин.
* Алкоголь ослабляет способность к усвоению биотина, и поэтому хроническое злоупотребление алкоголем может привести к дефициту биотина.
* Жиры масла, подвергшиеся тепловой обработке или воздействию воздуха в течение длительного времени, замедляют усвоение биотина.
* Антибиотики, лекарства с содержанием серы и сахарин также влияют на усвоение биотина.
Если вам нужно длительное лечение антибиотиками - это относится и к детям, и к взрослым, - синтез биотина может резко сократиться из-за гибели полезных кишечных бактерий, что делает дополнительный прием необходимым.
Витамин Н показан при выпадении волос и псориазе, в косметике его применяют в составе средств для ухода за волосами и в масках.
Метаболизм Биотин, связанный с белками, поступает с пищей, при помощи протеиназ переходит в свободное состояние и всасывается в тонком кишечнике. При поступлении в кровь он вновь соединяется с белками (альбуминами) и поступает в ткани. Задерживается биотин главным образом в печени и почках. Выводится в неизменённом виде с мочой и калом. Коферментной формой витамина Н является N5-карбоксибиотин.
Структура и свойства.
В основе строения биотина лежит тиофеновое кольцо, к которому присоединена мочевина, а боковая цепь пердставлена валериановой кислотой:
Биотин представляет собой кристаллическое вещество, хорошо растворимое в воде и спирте. Это устойчивое соединение, биологическая активность которого не меняется после кипячения растворов и при доступе кислорода.
Эмпирическая формула : С 10 Н 16 О 3 N 2 S.
проф. Круглов Сергей Владимирович (слева), Кутенко Владимир Сергеевич (справа)
Редактор страницы: Кутенко Владимир Сергеевич

Кудинов Владимир Иванович
Кудинов Владимир Иванович , Кандидат медицинских наук, Доцент Ростовского Государственного медицинского университета, Председатель ассоциации эндокринологов Ростовской области, Врач – эндокринолог высшей категории

Джериева Ирина Саркисовна
Джериева Ирина Саркисовна Доктор медицинских наук, доцент, врач-эндокринолог
ГЛАВА 4 МЕТАБОЛИЗМ ВИТАМИНА D И ПОЧКИ
ДЖ. ЛЕМАН, Р. У. ГРЕИ
(J. LEMMANN, R. W. GRAY)
Давно известно, что тяжелые почечные заболевания часто сопровождаются поражениями костной ткани, включая рахит или остеомаляцию, а также замедлением всасывания кальция в кишечнике. Рахит или остеомаляция в Сочетании с замедлением всасывания кальция в кишечнике являются и признаками недостаточности витамина D. За последние 15 лет в результате появления множества новых сведений об эндокринной природе витамина D выяснилась роль почек в его метаболизме. Кроме того, необходимость лечения все большего числа больных с хронической почечной недостаточностью до и в процессе поддерживающего их жизнь диализа заставила клинически оценить эти новые сведения и широко использовать их в практической медицине. Ниже обобщены современные представления о метаболизме и действии витамина D, причем специальное внимание уделяется роли почек в этих процессах и анализу нарушений метаболизма витамина D в условиях патологии.
ИСТОРИЧЕСКИЙ ОЧЕРК
История витамина D началась с выяснения возможных популяционных особенностей в строении скелета и изучения патогенеза рахита как костного заболевания. Согласно описанию Геродота (484-425 гг. до н. э.), у убитых египетских солдат, которые по обычаю с детства не закрывали голов от солнца, черепа были твердыми, тогда как у персидских солдат, всегда носивших тюрбаны, черепа оказывались мягкими. Такие наблюдения расценивались как указания на то, что солнечное освещение может обеспечивать толщину и твердость костей. Медицинской проблемой рахит становится только в XVII в., когда в Англии и Северной Европе образуются города. Вскоре появились и случайные наблюдения об излечивающем рахит действии рыбьего жира. К сожалению, широкое применение этого народного лечебного средства задержалось более чем на столетие, пока не сформировалось представление о важности веществ, присутствующих в пище в следовых количествах (в частности, витаминов).
К концу XIX в. географические исследования вновь указали на распространенность рахита в городах, население которых испытывало недостаток солнечного света. Изучение скелета умерших больных рахитом позволило установить сниженную минерализацию костей и меньшее содержание кальция и фосфора в них, тогда как исследования обмена веществ обнаружили низкую скорость всасывания кальция и фосфора в кишечнике таких больных.
К концу I мировой войны на пути к пониманию природы рахита было сделано два главных шага. Mellanby разработал метод воспроизведения рахита у щенков, показав, что это заболевание в эксперименте излечивается жиром печени трески. Такие наблюдения отчетливо указывали на присутствие в диете антирахитного фактора. Примерно в то же время Huldchinsky, удалось вылечить детей с помощью облучения их под ртутной лампой. Более того, у 1 ребенка облучение только одной руки обусловило появление рентгенографических признаков улучшения состояния костей всего скелета. Это наблюдение явилось первым четким доказательством возможности образования в организме циркулирующего и имеющего, по-видимому, гормональную природу антирахитного фактора. Впоследствии опыты на крысах с экспериментальным рахитом показали, что к излечению приводит облучение не только самих крыс, но и их пищи. Присутствующий в диете антирахитный фактор оказался жирорастворимым веществом, отличающимся от витамина А. В 1932 г. было установлено строение витамина D-секостерина, образующегося при облучении пищевых продуктов, а в 1936 г. была определена и структура природного витамина D. Взятые вместе, эти наблюдения сформировали основу современного представления, согласно которому витамин D одновременно является гормоном и (в условиях ограниченного солнечного освещения) витамином.

Структура витамина D
ХИМИЧЕСКОЕ СТРОЕНИЕ ВИТАМИНА D
На рис. 39 представлена структура витамина D 3 - холекальциферола, а также система нумерации положений углеродных атомов в его молекуле. Витамин D 2 - эргокальдиферол - отличается лишь присутствием двойной связи между 22-м и 23-м углеродным атомом и дополнительной метильной группы в положении 24. Молекулярная масса витамина D 3 равна 384. Он нерастворим в воде, но легко растворяется в органических растворителях и жирах. Витамин весьма чувствителен к окислению на воздухе или перекисями в растворе и разрушается в кислой среде. Недавно был опубликован обзор, посвященный строению и конфигурации молекул витамина D и аналогичных секостероидов.
МЕТАБОЛИЗМ ВИТАМИНА D
Подробное выяснение путей метаболизма витамина D 3 стало возможным лишь после его химического синтеза с изотопной меткой, разработки хроматографических методов разделения его метаболитов и создания способов биологической оценки эффектов как самого витамина D 3 , так и его метаболитов. 7-Дегидрохолестерин образуется в коже под действием фермента и в условиях ультрафиолетового облучения (в основном при длине волн 300-310 нм) превращается в превитамин D 3 . Последний спонтанно подвергается температурной изомеризации в витамин D 3 , который затем соединяется с сывороточным витамин D-связывающим глобулином (ДСГ). Комплекс витамина D 3 с белком переносится кровью в печень, где витамин D 3 гидроксилируется по 25-му углеродному атому, образуя основную форму витамина в плазме - 25-OH-D 3 . Это вещество в свою очередь транспортируется ДСГ в почки, где оно может подвергаться дальнейшему гидроксилированию в гормональную форму витамина D 3 -l,25-(OH) 2 -D 3 .
Синтез витамина D 3 в коже
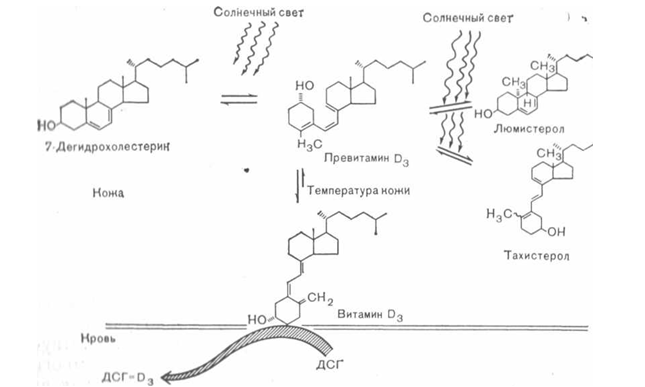
Синтез витамина D
Современные представления о синтезе витамина D 3 в коже схематизированы на рис. 41. Как уже отмечалось, превитамин D 3 образуется в коже из 7-дегидрохолестерина. Кожа содержит большие количества этого предшественника, благодаря чему не лимитируется скорость образования превитамина. Holick и соавт. облучали кожу человека in vitro и нашли, что воздействие света, имитирующее солнечное облучение близ экватора, уже за несколько часов может обеспечить максимальное образование превитамйна D 3 в базально-клеточных слоях кожи. Некоторое время назад уже было высказано предположение, что темная пигментация кожи может полностью исключать синтез в ней витамина D. Более поздние исследования Holick и соавт. показали, что с увеличением пигментации кожи удлиняется срок воздействия света, необходимый для максимального образования превитамина D 3 . Такое замедление образования превитамина D 3 могло бы, следовательно, снижать синтез витамина D 3 в сильно пигментированной коже в условиях ограниченности солнечного освещения. Превитамин D 3 затем подвергается в коже температурно-зависимому неферментативному превращению и витамин D 3 . Для превращения 50% имеющегося в коже провитамина Da в витамин D 3 требуется примерно 1 сут. После этого витамин D 3 связывается с ДСГ и попадает в кровь. Подробности механизма образования комплекса ДСГ - D 3 и его проникновения в кровь остаются неизвестными.
Транспорт витамина D и eго метаболитов: витамин D-связывающий глобулин
Витамин D-связывающий глобулин синтезируется в печени и идентичен групповому специфическому белку человека (Gc), давно известному генетикам. Генетические варианты этого белка, по-видимому, не различаются по способности связывать стерины группы витамина D. Поскольку суммарная концентрация всех метаболитов витамина D в сыворотке в норме не достигает 10 -7 М (см. ниже), а молярная концентрация ДСГ примерно на два порядка выше, то очевидно, что такой избыток связывающего белка способствует сохранению витамина D и его метаболитов в условиях ограниченного их поступления в организм предотвращает токсичность витамина D при увеличении его потребления или синтеза в коже. ДСГ не только участвует в транспорте метаболитов витамина D в крови, но и присутствует в форме комплекса с цитозольным белком в клетках многих тканей. Недавно этот белок был индентифицирован как актин. Предполагается, таким образом, что ДСГ может участвовать в переносе секостероидов из внеклеточной жидкости внутрь клеток. С другой стороны, основной детерминантой транспорта стероидов в клетки может быть концентрация свободных (не связанных с ДСГ) метаболитов витамина D.
Синтез 25-OH-D 3 в печени
Циркулирующий в крови витамин D быстро захватывается печенью, где он подвергается гидроксилированию по 25-му углеродному атому с образованием 25-OH-D 3 . Гидроксилирование осуществляется в основном микросомной монооксигеназой со смешанной функцией и требует присутствия молекулярного кислорода, флавопротеина и цитохрома Р-450. Км этого фермента составляет примерно 10 -8 М. Активность микросомной гидроксилазы при введении витамина D 3 снижается. Кроме того, печень содержит и митохондриальную 25-гидроксилазу, требующую в качестве кофакторов железосеросодержащий белок и цитохром Р-450, но обладающую гораздо большей Км (примерно 10 -6 М). Это свидетельствует о значении данного фермента в продукции 25-OH-D 3 только при наличии необычно высоких концентраций витамина D 3 . 25-Гидроксилирование обнаружено также в кишечнцке и почках птиц, но с точки зрения количества эти органы играют, вероятно, лишь незначительную роль в общей продукции 25-OH-D 3 .
В печени может происходить и дальнейший метаболизм 25-OH-D 3 с образованием более полярных и биологически неактивных продуктов, что наблюдается в основном в условиях ускоренного микросомного гидроксилирования, вызванного различными фармакологическими средствами.
Синтез 1,25-(OH ) 2 — D 3 и 24,25-(ОН) 2 — D 3 в почках
Дальнейший метаболизм 25-OH-D 3 происходит в основном в почках. Главными метаболитами являются l,25-(OH) 2 -D 3 и 24,25-(ОН) 2 -D 3 . l,25-(OH) 2 -D 3 синтезируется 25-OН-D 3 -1 α -гидроксилазой - митохондриальной монооксигеназой со смешанной функцией, которая у млекопитающих присутствует, по-видимому, лишь в проксимальных канальцах, но у птиц она содержится не только в проксимальных канальцах, но и в клубочках. Этот фермент состбит из нескольких компонентов, включая железосеросодержащий белок, связанный с НАД, флавопротеин и цитохром Р-450, специфичный для 25-OH-D 3 . Специфичный компонент системы (цитохром Р-450) вводит один атом кислорода в положение 1 α . Вся эта ферментная система изучена почти исключительно в почках цыпленка или в первичной культуре клеток его почек. Ее К м колеблется от 1,2 до 3,6х10 -7 М, а V макс составляет примерно 5,5 моль/мг митохондриального белка в 1 мин. В почках млекопитающих этот фермент труднее поддается исследованию, вероятно, из-за присутствия больших количеств 25-ОН-D 3 -связывающих белков, что ограничивает доступность субстрата. Недавние исследования обнаружили, однако, 1 α -гидрокси,лазную активность в митохондриях, выделенных из коркового вещества почек крыс с D-авитаминозом. К м фермента (8,9х10 -7 М) несколько выше, чем для митохондриального фермента у цыплят, хотя последние данные нуждаются в подтверждении. Фермент найден также в почечных срезах крыс, в изолированных клетках крысиной почки и в культуре клеток почки мыши. В большинстве этих исследований ферментативную активность определяли по превращению меченого 25-OH-D 3 в радиоактивные продукты, мигрирующие при высокоэффективной жидкостной хроматографии вместе с аутентичным l,25-(OH) 2 -D 3 . Химически этот продукт был идентифицирован как 1,25-(ОН) 2 -D 3 только в гомогенах почки крысы.
В почке из 25-OH-D 3 образуется и 24,25-(ОН) 2 -D 3 . Это происходит под действием фермента, который также является митохондриальной оксидазой со смешанной функцией и локализуется у крыс, по-видимому, в проксимальных извитых и прямых почечных канальцах. Км 24-гидроксилазы митохондриальных препаратов почки цыпленка составляет примерно 1х10 -6 М, а почки крысы - около 3,8х10 -7 М.
Внепочечный синтез l ,25-(OH ) 2 — D 3 и 24,25-(OH ) 2 — D 3
После того как было показано, что в организме беременных и нефрэктомированных крыс с авитаминозом D меченый 25-OH-D 3 может превращаться в более полярный метаболит, мигрирующий вместе с l,25-(OH) 2 -D 3 , удалось выяснить роль плаценты в метаболизме 25-OH-D 3 с образованием продукта, химически идентифицированного как l,25-(OH)2-D 3 . Недавно были также опубликованы данные, показывающие, что клетки крыши черепа плода крысы в культуре способны синтезировать вещество, мигрирующее вместе с l,25-(OH) 2 -D 3 . В противовес всем этим наблюдениям многократно сообщалось об отсутствии определимых количеств l,25-(OH) 2 -D 3 в сыворотке крови лишенных почек людей, жизнь которых поддерживалась диализом, а также у нефрэктомированных небеременных животных. Совсем недавно, однако, удалось определить низкую концентрацию l,25-(OH) 2 -D 3 в сыворотке крови лишенных почек больных. Больше того, введение таким больным витамина D2 приводило к повышению уровня l,25-(OH) 2 -D 3 в сыворотке (но не до нормы). Хотя эти наблюдения свидетельствуют о том, что у человека в условиях доступности большие количеств предшественника (25-OH-D) немного l,25-(OH) 2 -D может образовываться и вне почек, однако в норме уровень l,25-(OH) 2 -D в сыворотке не зависит от концентрации 25-OH-D. Тем не менее современные исследования дают основания считать, что в определенных условиях (у детей и лиц с авитаминозом D, подвергающихся ультрафиолетовому облучению) уровень l,25-(OH) 2 -D все же может зависеть от концентрации предшественника (25-OH-D).
Почки, по-видимому, служат основным органом, где у человека синтезируется 24,25-(ОН) 2 -D, так как его уровень в сыворотке крови снижается по мере прогрессирования почечной недостаточности, становясь очень низким и часто неопределимым у больных, лишенных почек. Однако на животных получены данные, показывающие, что и другие ткани, в том,числе кишечник и хрящ, могут образовывать из 3 H-25-OH-D 3 меченый метаболит, обладающий теми же хроматографическими свойствами и чувствительностью к разрушающему действию перйодата, что и подлинный 24,25-(ОН) 2 -D 3 . Кроме того, 24,25-(ОН) 2 -D 3 химически идентифицирован в плазме нефрэктомированных свиней, получавших большие дозы витамина D. Подобно этому, уровень 24,25-(ОН) 2 -D в сыворотке крови лишенных почек людей возрастает, когда они получают большие дозы витамина D 2 . Таким образом, при чрезмерно высокой концентрации 25-OH-D в сыворотке крови у человека 24,25-(ОН) 2 -D может синтезироваться и вне почек.
Энтеропеченочная циркуляция метаболитов витамина D
Витамин D и его метаболиты экскретируются в основном с калом. Витамин D 3 , 25-OH-D 3 и l,25-(OH) 2 -D 3 в печени подвергаются конъюгированию и секретируются в желчь. Имеются также данные о том, что эти метаболиты могут реабсорбироваться и реутилизироваться, формируя таким образом «запасной» механизм метаболизма витамина D.
Другие метаболиты витамина D
25-OH-D 3 может превращаться не только в l,25-(OH) 2 -D 3 и 24,25-(ОН) 2 -D 3 , но и в другие соединения. К ним относятся 25,26-(ОН) 2 -D 3 и 25-ОН-D 3 -26,23-лактон. Эти метаболиты, как и 24,25-(ОН) 2 -D 3 , могут подвергаться 1-гидроксилированию, образуя 1,24,25-(ОН) 3 -D 3 , 1,25,26-(OH) 3 -D 3 и l,25-(OH) 2 -D 3 -26,23-лактон. Кроме того, может подвергнуться окислению боковая цепь 1,25-(OH)2-D 3 , в результате чего образуется 23-кислота (кальцитроевая кислота); при окислении же боковой цепи 25-OH-D 3 образуется 24-кислота (холакальциевая кислота). Позднее были выделены 23,25-(ОН) 2 -D 3 , 25-OH-24-оксо-D 3 , 25-ОН-транс-D 3 и 19-нор-10-оксо-25-OH-D 3 . Эти метаболиты в свою очередь могут подвергаться дальнейшей трансформации. Современные данные свидетельствует о том, что биологические эффекты этих метаболитов не соответствуют таковым 1,25-(OH) 2 -D 3 , так что их физиологическая роль остается неясной. Отдельные из них (если не все) наверняка представляют собой продукты деградации.
БИОЛОГИЧЕСКИЕ ЭФФЕКТЫ ВИТАМИНА D
Транспортные процессы в кишечнике
Кальций
Всасывание кальция в кишечнике осуществляется за счет активного транспорта против электрохимического градиента, а также (когда содержание кальция в пище и, следовательно, его концентрация в просвете кишки чрезмерно возрастают) за счет пассивного перемещения. У животных и человека с авитаминозом D всасывание кальция в кишечнике в условиях нормального его поступления с пищей снижается. Введение витамина D 3 животным с авитаминозом D восстанавливает нормальную скорость всасывания кальция в кишечнике не ранее чем через 16 ч. Существование этого лаг-периода позволило предположить, а затем и доказать, что витамин D должен подвергнуться каким-то превращениям, а в кишечнике должны произойти некоторые изменения, прежде чем нормализуется транспорт кальция. Уже давно было показано, что 25-OH-D 3 нормализует транспорт кальция быстрее, чем это делает витамин D 3 . Затем был идентифицирован l,25-(OH) 2 -D 3 и установлено, что он является более эффективным и быстродействующим метаболитом витамина D в отношении стимуляции всасывания кальция в кишечнике. В период максимальной стимуляции активного транспорта, вызванной введением меченого витамина D 3 животным с авитаминозом D, в кишечнике удается определить только меченый 1,25-(OH) 2 -D 3 . Данное соединение связывается, по-видимому, со специфическим рецепторным белком цитозоля клеток кишечника, который переносит стероид в ядро, где он комплексируется с хроматином и индуцирует синтез белка, подобно тому, как это происходит в отношении других стероидных гормонов. В ответ на действие 1,25-(ОН) 2 -О 3 образуется специфическая мРНК, кодирующая синтез специфического кальцийсвязывающего белка (СаСБ). Содержание последнего в кишечнике коррелирует с транспортом кальция в этом органе, увеличиваясь, когда животным с авитаминозом D вводят витамин D 3 или по мере возрастания активного транспорта кальция при ограничении кальция в диете, и снижаясь по мере замедления всасывания кальция в кишечнике, происходящего с возрастом. Эти данные позволяют считать, что СаСБ принимает участие в активном транспорте кальция в кишечнике в качестве переносчика. С другой стороны, СаСБ появляется в кишечнике несколько позднее, чем возникает стимуляция транспорта кальция, вызванная введением 1,25-(ОН) 2 -D 3 животным с авитаминозом D. Кроме того, увеличение всасывания кальция в кишечнике в таких условиях протекает, по-видимому, двухфазно: после начальной транзиторной стимуляции процесса регистрируется повторное и длительное его ускорение. Таким образом, СаСБ может не столько «запускать» транспорт кальция, сколько поддерживать его на повышенном уровне. Предварительное введение животным с авитаминозом D ингибиторов синтеза белка предотвращает действие 1,25-(ОН) 2 -О 3 на синтез СаСБ в кишечнике, но не блокирует восстановления всасывания кальция. Позднее было выдвинуто предположение, что l,25-(OH) 2 -D «запускает» транспорт кальция за счет изменения фосфолипидного состава обращенной в просвет кишечника мембраны клеток. Витамин D может ускорять и пассивное перемещение Са в кишечнике, так как поступление Са при введении витамина D животным с D-авитаминозом возрастает и в том случае; когда кишечник исследуется при низкой температуре или в анаэробных условиях.
У человека в условиях насыщения витамином D всасывание кальция в кишечнике, определяемое либо как истинное (с помощью изотопных методик), либо как результирующее (с помощью балансовых экспериментов), прямо коррелирует с концентрациями l,25-(OH) 2 -D в интервале от нуля до верхней границы нормы. Эта зависимость необычайно чувствительна: у лиц, находящихся на нормальной диете, обеспечивающей поступление 10-25 ммоль кальция в день, при повышении концентрации l,25-(OH) 2 -D в сыворотке крови на 1 пМ всасывание кальция в кишечнике увеличивается на 0,23%, или, на 0,06 ммоль. Таким образом, при нормальном содержании кальция в диете всасывание его в кишечнике определяется доступностью l,25-(OH) 2 -D.
Фосфат
При дефиците витамина D снижается и транспорт фосфата в кишечнике. Введение в таких условиях витамина D или 1,25-(OH) 2 -D 3 усиливает кишечное всасывание фосфата. Этот эффект обусловливается, по-видимому, присутствием именно l,25(OH) 2 -D 3 , так как 25-ОН-D 3 не стимулирует транспорта фосфата при введении его нефрэктомированным животным с авитаминозом D. Наибольшая стимуляция всасывания фосфата после введения l,25-(OH) 2 -D наблюдается в тощей кишке; затем - в двенадцатиперстной и подвздошной. Но хотя по этому вопросу еще имеются противоречия, по-видимому, для проявления стимуляции всасывания фосфата витамином D необходим кальций. Введение l,25-(OH) 2 -D 3 может усиливать кишечное всасывание фосфата и у человека. Однако у лишенных почек и находящихся на гемодиализе больных, у которых концентрацию l,25-(OH) 2 -D в сыворотке крови определить невозможно, всасывается значительная доля фосфата, содержащегося в пище. Это указывает на независимость кишечного всасывания фосфата от l,25-(OH) 2 -D 3 . У людей в условиях насыщения витамином D всасывание фосфата в кишечнике, выраженное в процентах от его поступления с пищей (при нормальных колебаниях последнего), на 1 пМ прироста концентрации l,25-(OH) 2 -D увеличивается на 0,05%.
Хотя наиболее эффективным и быстродействующим в отношении кишечного всасывания кальция и фосфата метаболитом витамина D является именно 1,25-(ОН) 2 -D 3 , в фармакологических дозах определенной активностью могут обладать и другие метаболиты этого витамина. В настоящее время, однако, считают, что l,25-(OH) 2 -D - единственная физиологически значимая форма витамина D для процессов кишечного всасывания этих минеральных веществ.
Кость
Поражение костей (рахит в период роста и остеомаляции у взрослых) - патогномоничный признак D-авитаминоза. Костная патология включает нарушение кальцификации и рассасывание эпифизарных хрящей, а также утрату способности эпифизарного новообразования кости наряду с метафизарным разрастанием неминерализованного остеоидного или костного матрикса. При лечении животных и людей с D-авитаминозом соответствующим витамином наблюдается нормализация эпифизирной кальцификации хряща и происходит нормальный рост кости в сочетании с минерализацией остеоида, что приводит к исчезновению костной патологии. Что касается механизмов перечисленных влияний витамина D на кость, то здесь пока сохраняются противоречивые мнения. С одной стороны, предполагается, что нормальная минерализация костей обусловливается повышением концентраций кальция и фосфата в сыворотке и внеклеточной жидкости, которое в свою очередь является следствием стимулирующего влияния витамина D на всасывание кальция и фосфата в кишечнике. С другой стороны, витамин D или один из его метаболитов мог бы непосредственно действовать на хрящевую и костную ткани, нормализуя их минерализацию. Хотя известно, что передозировка витамина D вызывает деминерализацию скелета, a l,25-(OH) 2 -D in vitro усиливает резорбцию кости, имеются данные, свидетельствующие о способности витамина D стимулировать минерализацию кости. Например, у больных с остеомаляцией, обусловленной хронической почечной недостаточностью, искусственное повышение уровней кальция и фосфата в сыворотке крови не нормализует минерализации костей, тогда как при введении витамина D такая нормализация происходит. Механизм прямого влияния витамина D на кость остается неизвестным. Однако в костных клетках присутствуют специфические рецепторы l,25-(OH) 2 -D, которые теоретически могли бы опосредовать такой эффект.
Кроме того, существуют противоречия относительно природы метаболита витамина D, необходимого для нормальной минерализации костей. В некоторых клинических исследованиях было показано, что при введении одного l,25(OH) 2 -D 3 больным с авитаминозом D исчезают только дефекты минерализации, но избыточные количества остеоида сохраняются. Для полной ликвидации костной патологии в этих исследованиях вводили витамин D 3 , или 25-OH-D 3 , или сочетание l,25-(OH) 2 -D 3 с 24,25-(ОН) 2 -D 3 . Отсюда следует, что для нормального образования кости мог бы требоваться 24,25-(ОН) 2 -D. Позднее, однако, появились сообщения о том, что введение одного l,25-(OH) 2 -D 3 может приводить к полному излечению остеомаляции, несмотря на сохранение низких уровней 25-ОH-D и 24,25-(ОН) 2 -D в сыворотке крови. Больше того, недавние исследования по экспериментальному рахиту у животных показали, что ликвидации костной патологии можно добиться введением аналога витамина D-24,24-дифтор-25-ОН-D 3 , который не подвергается гидроксилированию в 24-м положении, но способен гидроксилироваться в 1-м положении. Приведенные данные свидетельствуют против роли недостаточности 24,25-(OH) 2 -D 3 в патогенезе рахита и остеомаляции. Для окончательного решения этого вопроса необходимы, очевидно, дальнейшие исследования.
Почки
В почках идентифицированы специфические цитозольные рецепторы l,25-(OH) 2 -D 3 , обладающие высоким сродством к этому соединению. Однако влияние витамина D и его метаболитов на почки остается областью противоречий. При исследовании почечного клиренса уже давно было показано, что 25-OH-D 3 и 1,25-(OH) 2 -D 3 усиливают канальцевую реабсорбцию кальция и фосфата у собак, что должно было бы способствовать сохранению запасов этих веществ в организме. Однако последующие исследования по клиренсу у тиреопаратйреоидэктомированных крыс, получавших физиологические дозы l,25-(OH) 2 -D (что восстанавливало всасывание кальция в кишечнике до нормы), не выявили изменений экскреции кальция в расчете на единицу скорости клубочковой фильтрации по мере прогрессивного увеличения концентрации кальция в сыворотке до нормы и выше. В отличие от этого паратиреоидный гормон (ПТГ), как и ожидалось, снижал экскрецию кальция с мочой. Такие наблюдения должны были бы указывать на то, что l,25-(OH) 2 -D не оказывает видимого влияния на транспорт кальция в почечных канальцах. Однако дальнейшее изучение данного вопроса отчетливо продемонстрировало значение l,25-(OH) 2 -D для транспорта кальция в других тканях, где присутствуют l,25-(OH) 2 -D и СаСБ, а также наличие рецепторов l,25-(OH) 2 -D и СаСБ в почках. В аналогичных экспериментах с определением динамики фосфата в почках тиреопаратиреоидэктомированных крыс, получавших 1,25-(ОН) 2 -D 3 , было показано торможение канальцевой реабсорбции фосфата. Этот эффект, по-видимому, опосредуется усилением секреции фосфата более проксимальными сегментами канальца и, возможно, сегментом, располагающимся вне дистальной извитой его части. Больше того, введение l,25-(OH) 2 -D больным с гипопаратиреозом сопровождается снижением уровня фосфата в сыворотке крови. Приведенные данные в совокупности указывают, таким образом, на способность витамина D увеличивать экскрецию фосфата с мочой, причем этот эффект не связан с хорошо известным фосфатурическим действием ПТГ.
У человека повышение концентрации l,25-(OH) 2 -D в сыворотке сопровождается возрастанием экскреции кальция с мочой. В условиях нормального потребления кальция этот эффект является, по-видимому, следствием усиления его кишечного всасывания и повышения концентрации в сыворотке крови, что приводит к увеличению клубочковой фильтрации кальция и (в результате снижения уровня иммунореактивного ПТГ в сыворотке) к торможению канальцевой реабсорбции. При низком содержании кальция в диете повышение уровня 1,25-(ОН) 2 -D в сыворотке крови также сопровождается усилением экскреции кальция с мочой вследствие более эффективного его всасывания в кишечнике и резорбции костной ткани, но кальцийурическая реакция выражена все же слабее, чем в условиях нормального потребления кальция.
Прочие ткани
Обладающие высоким сродством к l,25-(OH) 2 -D рецепторы и (или) зависимый от витамина D СаСБ обнаружены не только в кишечнике, костях и почках, но и в молочных железах, коже, околощитовидных железах, гипофизе и поджелудочной железе. Кроме того, рецепторы были найдены в культивируемых фибробластах человека и некоторых линиях злокачественных клеток.
Рецепторы l,25-(OH) 2 -D 3 имеют константу седиментации, равную примерно 3,3S, и обладают высоким сродством к гормону: К д около 10 -10 М. Присутствие рецепторов 1,25-(ОН) 2 -D и СаСБ в молочных железах согласуется, очевидно, с наличием транспорта Са в молоко. Что касается других тканей, то они не являются общепризнанными мишенями витамина D и его метаболитов, так что роль последних в регуляции их функции остается неизвестной. Можно было бы предположить, что в коже 1,25-(OH) 2 -D регулирует продукцию витамина D. 1,25-(ОН) 2 -D мог бы также облегчить поступление кальция в околощитовидные железы, усиливая тем самым его известное ингибиторное действие на секрецию ПТГ. Подобно этому, облегчая проникновение кальция в β-клетки поджелудочной железы, l,25-(OH) 2 -D мог бы повышать секрецию инсулина.
Возможная роль 24,25-(OH ) 2 — D
После открытия химического синтеза 24,25-(ОН) 2 -D 3 возник интерес к его возможной биологической роли, поскольку он является основным метаболитом витамина D не только у животных, но и у человека. Первые опыты на животных с D-авитаминозом показали, что биологическая активность 24,25-(ОН) 2 -D 3 сравнима с таковой его предшественника - 25-OH-D 3 . Однако эта активность, по-видимому, связана в основном с lα-гидроксилированием метаболита и образованием 1,24,25-(ОН) 2 -D 3 . Исследования, проведенные у здоровых лиц и лишенных почек больных, показали, что введение 24,25-(ОН) 2 -D могло бы стимулировать всасывание кальция в кишечнике, но в последующих наблюдениях этого подтвердить не удалось. Позднее было высказано предположение, что 24,25-(ОН) 2 -D 3 необходим для нормального вылупления цыплят из яиц и участвует в процессе формирования костей. Эту гипотезу подтверждают данные о том, что 24,25-(OH) 2 -D увеличивает синтез протеогликанов в культуре хондроцитов из зон роста и что ядра этих клеток содержат специфические связывающие места для 24,25-(ОН) 2 -D. Однако, как отмечалось выше, введение l,25-(OH) 2 -D людям с D-авитаминозом может приводить к полному излечению остеомаляции, как это наблюдается и при костной патологии у крыс с дефицитом витамина D.
Сообщалось также, что 24,25-(OH) 2 -D тормозит секрецию ПТГ у собак, а также снижает массу гипертрофированных околощитовидных желез у цыплят с дефицитом витамина D. Кроме того, имеются сообщения о присутствии специфических рецепторов 24,25-(OH) 2 -D в околощитовидных железах цыплят с рахитом. Однако скетчардовский анализ не проводился, поэтому указанные рецепторы еще не охарактеризованы с достаточной определенностью. Таким образом, хотя важная роль 24,25-(ОН) 2 -D в гомеостазе кальция вполне возможна эта гипотеза остается умозрительной и требует дополнительных подтверждений.
РЕГУЛЯЦИЯ МЕТАБОЛИЗМА ВИТАМИНА D
Концентрации витамина D и его метаболитов в плазме отражают суммарное количество метаболитов витаминов D 3 и D 2 , поскольку в опытах по связыванию, на которых основаны приведенные данные, обычно не делалось различия между этими формами. Основной формой витамина D, присутствующей в плазме, является 25-OH-D; его средняя концентрация составляет около 60 нМ, или 25 нг/мл. Концентрации самого витамина D и 24,25-(ОН) 2 -D примерно в 10 раз ниже. Концентрация l,25-(OH) 2 -D приблизительно в 1000 раз ниже, чем 25-OH-D. Период полужизни витамина D в плазме - около 1 дня, так как он быстро превращается в 25-OH-D (что установлено для витамина D 3). Период полужизни в плазме 25-OH-D, судя по результатам определения скорости исчезновения введенного 3 Н-25-ОН-D 3 и наклону кривой, спада уровня 25-OH-D 3 после введения его фармакологических; доз, составляет приблизительно 3 нед. Поэтому содержание в плазме 25-OH-D позволяет, по-видимому, точнее оценивать запасы витамина D в организме. Период полужизни в плазме 1,25-(ОН) 2 -D 3 очень мал. Введенный в кровь 3 H-l,25-(OH) 2 -D 3 исчезает из плазмы с полупериодом менее 10 мин, хотя полупериод исчезновения из плазмы l,25-(OH) 2 -D после его приема как у здоровых взрослых людей, так и у лишенных почек больных составляет примерно 6 ч (R. W. Gray, J. Lemann, неопубликованные данные). Поэтому уровень l,25-(OH) 2 -D в плазме прежде всего отражает продукцию этого стероидного гормона.
25-OH-D 3
Синтез 25-OH-D 3 в печени, по-видимому, не является объектом жесткого контроля. Концентрация данного вещества в сыворотке, служащая наилучшим показателем запасов витамина D в организме, зависит главным образом от потребления этого витамина и синтеза его в коже под действием солнечного света. В Англии, где в молоко не добавляют витамин D 2 , концентрация в сыворотке 25-OH-D у здоровых лиц колеблется примерно от 30 нМ в конце зимы до 60 нМ в конце лета, что связано с интенсивностью солнечного облучения. Аналогичные, хотя и слабее выраженные сезонные колебания уровня 25-OH-D в сыворотке крови отмечены в США, где его минимальная концентрация зимой выше, вероятно, вследствие повсеместного добавления витамина D 2 в молоко и что важнее, более высокого уровня 25-OH-D 3 в летнее время. Последнее может отчасти объясняться сохранением превитамина D 3 в коже, так как ДСГ обладает гораздо большим сродством к витамину D 3 , чем к превитамину D 3 . Искусственное облучение 600 см 2 кожи в течение примерно 15 мин за 2 нед. увеличивает содержание 25-OH-D в сыворотке на 4-11 нМ. Расчеты показывают, что каждый квадратный сантиметр облученной кожи мог бы продуцировать до 0,024 нмоль 25-OH-D 3 . Отсюда следует, что солнечное облучение даже ограниченных участков кожи могло бы быть наиболее важной детерминантой содержания 25-OH-D в сыворотке и общих запасов витамина D в организме. Последние, таким образом, зависят в основном от географической широты проживания, сезона года и образа жизни.
Метаболизм и экскреция 25-OH-D 3 исследованы у здоровых взрослых людей после инъекций 3 H-25-OH-D 3 . За 1 нед. с мочой выделяется примерно 10% вещества (почти исключительно в виде водорастворимых конъюгатов его метаболитов); еще 15% экскретируется с калом также в основном в виде конъюгатов и метаболитов. Предполагают, что 25-OH-D 3 метаболизируется и путем окисления боковой цепи.
l,25-(OH) 2 -D 3
Поскольку почечный 25-ОН-Бз-1а-гидроксилазный комплекс локализован в митохондриях, регуляция синтеза 1,25-(ОН) 2 -Оз этой ферментной системой предполагает существование последовательности сигналов. Гормональные или нервные регуляторные стимулы должны были бы действовать на клеточную мембрану, генерируя «вторые мессенджеры», такие как циклический АМФ, или изменяя внутриклеточную концентрацию ионов или субстратов и кофакторов, необходимых для продукции энергии в митохондриях.
Дефицит витамина D у человека, естественно, сопровождается резким снижением сывороточных концентраций 25-OH-D, 24,25-(ОН) 2 -D и l,25-(OH) 2 -D. У таких больных отмечаются также гипокальциемия разной степени выраженности, вторичный гиперпаратиреоз и гипофосфатемия. При назначении им физиологических доз витамина D концентрация l,25-(OH) 2 -D в сыворотке быстро возрастает, превышая нормальный уровень, что свидетельствует о стимуляции почечной 25-OH-D 3 -lα-гидроксилазы и субстратной регуляции продукции гормона. По мере того как у больных с исходным дефицитом витамина D его запасы в организме восстанавливаются, уровень l,25-(OH) 2 -D снижается до нормы. Подобно этому, у животных с D-авитаминозом синтез 1,25-(OH) 2 -D 3 оказывается повышенным по сравнению с таковым у животных с достаточными запасами витамина D в организме, что регистрируется по превращению 3 H-25-OH-D 3 в 3 H-l,25-(OH) 2 -D 3 как in vivo, так и на изолированных почечных канальцах. Больше того, введение витамина D или l,25-(OH) 2 -D 3 животным с D-авитаминозом быстро снижает активность 1α-гидроксилазы in vivo и in vitro. В механизме подавления активности 25-ОН-D-1α-гидроксилазы гормоном (l,25-(OH) 2 -D) может играть роль ингибирование транскрипции генов.
Кальций
В ранних исследованиях на крысах было показано, что уменьшение содержания кальция в диете увеличивает превращение 3 H-25-OH-D 3 в 3 H-l,25-(OH) 2 -D 3 . Затем было установлено, что дефицит кальция повышает и концентрацию l,25-(OH) 2 -D в плазме, причем этот эффект практически исчезал у паратиреоидэктомированных животных. Искусственная гипокальциемия или сокращение количества кальция в пище увеличивает содержание в плазме l,25-(OH) 2 -D и у человека, что связано с возрастанием концентрации паратиреоидного гормона в сыворотке. Кроме того, уровень l,25-(OH) 2 -D в плазме часто оказывается повышенным у больных с первичным гипертиреозом; он также возрастает после инфузий ПТГ. Все эти наблюдения свидетельствуют о том, что дефицит кальция либо непосредственно, либо через стимуляцию секреции ПТГ увеличивает синтез l,25-(OH) 2 -D в почках. При ограничении кальция в диете уровень l,25-(OH) 2 -D в сыворотке несколько повышается даже у паратиреоидэктомированных животных, но сниженная концентрация кальция в среде не стимулирует активности фермента, образующего l,25-(OH) 2 -D, в культуре почечных клеток цыпленка. В то же время добавление ПТГ к среде культивируемых почечных клеток усиливает синтез l,25-(OH) 2 -D, что доказывает непосредственность действия паратиреоидного гормона. Повышение или снижение содержания l,25-(OH) 2 -D в сыворотке крови человека в условиях дефицита или избытка кальция тесно коррелирует с небольшими изменениями уровня ПТГ в сыворотке. Эти результаты указывают на важную роль системы Са - ПТГ в регуляции содержания l,25-(OH) 2 -D в плазме человека.
Фосфат
Ограничение фосфатов в диете усиливает у животных превращение 3 Н-25-ОН-D 3 в 3 H-l,25-(OH) 2 -D 3 . Дефицит фосфата повышает и концентрацию l,25-(OH) 2 -D в сыворотке крови животных и человека, причем данный эффект не зависит от функции околощитовидных желез. Механизм такого эффекта неизвестен. Предполагают, что он опосредуется уменьшением содержания неорганического фосфора в почечных клетках P0J но снижение концентрации фосфата в среде не стимулировало синтез l,25-(OH) 2 -D культурой почечных клеток цыпленка. У крыс повышение содержания l,25-(OH) 2 -D в плазме в ответ на ограничение фосфора в диете (что отражает почечный синтез гормона) блокируется гипофизэктомией, несмотря на сохранение гипофосфатемии. Не исключено, таким образом, гормональное опосредование стимуляции почечного синтеза 1,25-(OH) 2 -D при дефиците фосфора.
Другие факторы
Изучался и ряд других возможных факторов регуляции почечного синтеза l,25-(OH) 2 -D. У молодых растущих животных, у детей и подростков уровень l,25-(OH) 2 -D в плазме выше, чем после наступления половой зрелости. Содержание 1,25-(OH) 2 -D в плазме уменьшается и при старении. Предполагалось поэтому, что такие эффекты могут быть связаны с гормоном роста. Гипофизэктомия снижает уровень l,25-(OH) 2 -D в плазме крыс, причем это влияние нивелируется гормоном роста (СТГ). Больше того, введение СТГ инактным крысам увеличивает содержание l,25-(OH) 2 -D в плазме. С другой стороны, введение СТГ детям с недостаточностью гормона роста не повышает сывороточного уровня l,25-(OH) 2 -D, несмотря на стимуляцию роста; содержание l,25-(OH) 2 -D не всегда повышено и при активной акромегалии. Таким образом, роль СТГ в качестве стимул# синтеза l,25-(OH) 2 -D у человека остается невыясненной. С тем же основанием можно предполагать и участие других факторов, приводящих усиление всасывания кальция в кишечнике под действием l,25-(OH) 2 -D в соответствие с потребностями растущего скелета, для чего необходимы дальнейшие исследования.
К другим физиологическим состояниям, при которых возникает потребность организма в ускоренном всасывании кальция, относятся беременность, образование скорлупы яиц у птиц и лактация. У женщин уровень l,25-(OH) 2 -D в плазме по мере развития беременности повышается. Как уже отмечалось, 1,25-(OH) 2 -D может продуцироваться плацентой, что, вероятно, в какой-то степени и определяет такое повышение. Сопровождается ли беременность дополнительной независимой стимуляцией почечного синтеза l,25-(OH) 2 -D - не известно. Следует отметить, однако, что у птиц эстрогены стимулируют почечный синтез l,25-(OH) 2 -D, а, как известно, концентрация эстрогенов в сыворотке крови по мере развития беременности возрастает. Повышение уровня l,25-(OH) 2 -D в плазме при беременности отчасти может быть связано с увеличением концентрации ДСГ в сыворотке, наблюдающимся в этот период. Во время лактации содержание 1,25-(ОH) 2 -D в сыворотке также повышено. В отношении механизма этого явления имеются противоречия. При кормлении грудью возрастает уровень пролактина, а на птицах показано, что пролактин стимулирует синтез l,25-(OH) 2 -D в почках. Однако у женщин с гиперпролактинемическим синдромом галактореи - аменореи уровень l,25-(OH) 2 -D в плазме не повышен.
Хорошо известно, что метаболический ацидоз сопровождается гиперкальциурией, что требует оценки метаболизма витамина D при ацидозе. В условиях метаболического ацидоза синтез 1,25-(OH) 2 -D у животных с D-авитаминозом тормозится, но у человека в отсутствие дефицита витамина D легкий ацидоз, хотя он и сопровождается повышенной экскрецией кальция с мочой, не вызывает изменений уровня l,25-(OH) 2 -D в сыворотке. Кроме того, у человека метаболический ацидоз не вызывает видимых изменений всасывания кальция в кишечнике. Таким образом, в патогенезе характерной для метаболического ацидоза кальциурии у человека в условиях отсутствия дефицита витамина D изменения метаболизма последнего, по-видимому, не играют никакой роли.
У здорЬвого взрослого человека 3 H-l,25-(OH) 2 -D уже в течение 4-6 ч превращается в более полярные соединения. Около 15-20% его выводится за 1 нед с мочой, главным образом в виде конъюгатов этих более полярных метаболитов, тогда как с калом за то же время выводится примерно 50% (также в виде более полярных метаболитов и конъюгатов). Остальная часть распадается, вероятно, при окислении боковой цепи. Можно полагать; что у здорового человека именно синтез 1,25-(OH) 2 -D, а не его быстрый метаболизм, является основной детерминантой концентрации гормона в плазме.
Регуляция уровня 24,25-(OH ) 2 — D
Содержание 24,25-(ОН) 2 -D в плазме при D-авитаминозе у человека, естественно, снижается до трудно определяемых значений; это вещество появляется в сыворотке только после восстановления в организме запасов его предшественников - 25-OH-D. В отсутствие дефицита витамина D сывороточная концентрация 24,25-(OH) 2 -D у человека прямо коррелирует с концентрацией предшественника (25-OH-D). Таким образом, синтез 24,25-(OH) 2 -D зависит, по-видимому, в основном от доступности 25-OH-D. Нет данных, которые указывали бы на регуляцию синтеза 24,25-(OH) 2 -D (при отсутствии дефицита витамина D) кальцием, фосфором или ПТГ. Как отмечалось выше, вопрос о том, является ли 24,25-(ОН) 2 -D просто начальным продуктом распада витамина D или он обладает физиологической гормональной активностью, до сих пор не решен.
ЗАБОЛЕВАНИЯ, СВЯЗАННЫЕ С ВИТАМИНОМ D
Выяснение метаболизма витамина D и процессов его физиологической регуляции позволяет последовательно проанализировать результаты нарушения продукции и действия этого витамина, а также результаты избыточного его потребления или активации отдельных этапов его метаболизма.
Недостаточность витамина D : рахит и остеомаляция
Патогномоничными признаками рахита и остеомаляции являются деформация скелета у детей, боли в костях, переломы, и слабость проксимальных мышц. Рахит характеризуется нарушением созревания и кальцификации хрящей и костей, а остеомаляция, возникающая после завершения роста скелета, - нарушением минерализации костей. В табл. 13 перечислены основные нарушения метаболизма витамина D, приводящие к era недостаточности и, следовательно, к патологии минерального обмена.
Кожа
Так как синтез витамина D в коже осуществляется неферментативным путем, какие-либо внутренние дефекты этого процесса неизвестны. Недостаточный кожный синтез витамина D обусловливается скорее всего недостатком солнечного облучения в силу различных обстоятельств. В соответствии с этим приобретенная недостаточность витамина D наблюдалась при отсутствии солнечного облучения, особенно среди пожилых лиц или хронически больных, не выходящих из дома или больничной палаты. В США дефицит витамина D встречается редко, что связано, вероятно, с достаточным пребыванием на солнце. Не исключено также, что потребность в витамине D частично покрывается поливитаминными добавками, широко распространенными в практике кормления детей, и, кроме того, добавлением витамина D к молоку (обычно около 400 ME, или 10 мкг витамина D 2 на 1 л). В Англии в отличие от США рахит у детей и подростков, принадлежащих к популяции иммигрантов из азиатских стран, остается важной проблемой. Механизмы возникновения D-авитаминоза в этой группе населения (они исследованы недостаточно) могут быть связаны с ограниченностью» солнечного облучения. Предполагается, кроме того, роль потребления с пищей больших количеств зерновых продуктов, содержащих фитат, что могло бы увеличивать потерю витамина D с калом и затруднять всасывание кальция в кишечнике.
Печень
Генетическая недостаточность печеночной 25-гидроксилазьв не описана. Однако в печени синтезируется не только 25-ОН-D 3 , но и ДСГ. Кроме того, для всасывания витамина D в кишечнике и поддержания энтеропеченочной циркуляции может иметь важное значение и нормальное желчеобразование. Поэтому при тяжелых заболеваниях печени и желчных путей иногда возникает остеомаляция. Возможной причиной остеомаляции, нередко встречающейся у больных, длительно получающих противосудорожные средства (фенобарбитал и фенитоин), считают ускорение распада витамина D и его метаболитов в печени за счет активации микросомной оксидазной системы. Не исключено также, что эти лекарственные вещества способны непосредственно снижать всасывание кальция и фосфора в кишечнике. К остеомаляции могут приводить и заболевания кишечника как вследствие разрыва энтеропеченочной циркуляции витамина D, так и в результате прямого нарушения всасывания кальция и фосфата.
Почки
Причиной рахита в некоторых редких случаях является генетическая недостаточность синтеза l,25-(OH) 2 -D в почках. Существование такого нарушения вначале было доказано чисто логическим путем: по отсутствию терапевтического эффекта фармакологических доз витамина D или 25-OH-D 3 у тех детей с заболеванием костей, у которых полное выздоровление наступало при введении физиологических доз l,25-(OH) 2 -D 3 (1,2-- 2,4 нмоль/сут, или 0,5-1,0 мкг/сут). Позднее у таких детей были отмечены нормальные уровни 25-OH-D и очень низкие концентрации l,25-(OH) 2 -D в сыворотке, что указывало на нарушение синтеза последнего. Этот дефект, наследуемый как аутосомно-рецессивный признак, получил название витамин D-зависимого рахита I типа.
Среди больных с нефротическим синдромом и нормальной скоростью клубочковой фильтрации симптомы костного заболевания встречаются редко, но гистологически выявляются признаки остеомаляции. Уровни 25-OH-D, l,25-(OH) 2 -D и 24,25-(OH) 2 -D в этих случаях снижены, что отражает возрастание потерь витамина D и его метаболитов с мочой, вероятно, в связи с аналогичными потерями ДСГ. Молекулярная масса и изоэлектрическая точка ДСГ сходны с таковыми альбумина, и это могло бы способствовать его фильтрации при увеличении проницаемости клубочков. Хотя у больных нефрозом потери 25-OH-D с мочой могут достигать 10 нмоль и более в сутки, они все же меньше, чем расчетная средняя величина нормального суточного кругооборота этого соединения у здоровых людей. Поэтому потеря 25-OH-D с мочой может быть не единственной причиной его низкого уровня в сыворотке крови у таких больных. Больше того, нет каких-либо указаний на возникновение нефротического синдрома в ходе прогрессирующего поражения клубочков, чрезвычайно часто сопровождающегося остеодистрофией при наступлении почечной недостаточности. Можно полагать, таким образом, что потери с мочой метаболитов витамина D и ДСГ слабо влияют на сывороточную концентрацию несвязанного (свободного) 25-OH-D или 1,25-(OH) 2 -D, которая в основном и определяет биологические эффекты витамина D.
У некоторых больных с хронической почечной недостаточностью, особенно у детей, рахит возникает на фоне как будто нормального потребления витамина D с пищей. В костных биоптатах взрослых больных с хроническим заболеванием почек и поражением костей, называемым почечной остеодистрофией, часто обнаруживают не только изменения, обусловленные вторичным гиперпаратиреозом, но и различной степени остеомаляцию. Давно и хорошо известно также, что у больных с хроническим заболеванием почек нарушено всасывание кальция в кишечнике. Почти 40 лет назад показано, что всасывание кальция в кишечнике у больных с почечной остеодистрофией и выраженной почечной недостаточностью составляет в среднем лишь 1,8 ммоль/сут, или всего 7% от количества кальция, содержавшегося в диете, тогда как у здоровых людей, получавших ту же диету, обеспечивающую поступление примерно 27 ммоль кальция в сутки, всасывание достигает 8,1 ммоль/сут, или 28%. Чрезвычайно низкое всасывание кальция в кишечнике у больных с почечной остеодистрофией не поддается терапии физиологическими дозами витамина D, которые у больных с D-авитаминозом излечивают рахит. Как отмечалось выше, всасывание кальция в кишечнике зависит в основном от концентрации l,25-(OH) 2 -D в плазме, которая в свою очередь должна определяться способностью почек синтезировать этот гормон. Недавние наблюдения, проведенные среди взрослых больных с почечными заболеваниями, обнаружили нормальный или даже несколько повышенный уровень 1,25-(ОН) 2 -D в плазме в период умеренного снижения скорости клубочковой фильтрации (примерно до 50 мм/мин); вероятно, это обусловлено развитием вторичного гиперпаратиреоза, характерного для ранних стадий почечной недостаточности. Кроме того, у таких больных всасывание кальция в кишечнике оказывалось обычно в пределах нормы. С прогрессированием почечной недостаточности содержание l,25-(OH) 2 -D в плазме снижается и достигает очень низкого или неопределимого уровня у лишенных почек больных, находящихся на диализе. При падении СКФ ниже 50 мл/мин наблюдалось и прогрессивное уменьшение всасывания кальция в кишечнике. Имеется сообщение о том, что у детей содержание l,25-(OH) 2 -D в плазме может снижаться уже на ранних стадиях почечной недостаточности. Хотя частое поражение канальцево-интерстициальной ткани у детей могло бы за счет избирательного повреждения канальцев ограничивать синтез l,25-(OH) 2 -D оставшейся почечной тканью, все же снижение уровня этого соединения в плазме выявляется в таких случаях не всегда.
Пероральное введение l,25-(OH) 2 -D больным с хроническими заболеваниями почек усиливает всасывание кальция в кишечнике и прямо зависит от дозы. Примерно 1,6 нмоль, или 0,68 мкг 1,25-(ОН) 2 -D 3 в сутки (т. к. количество, близкое к величине расчетной скорости кругооборота в норме, повышает всасывание кальция в кишечнике до уровня, наблюдаемого у здорового человека. Таким образом, почечная недостаточность, по-видимому, не сопровождается значительным нарушением реакции на 1,25-(ОН) 2 -D 3 . Длительное его введение при хронической почечной недостаточности может, следовательно, повышать концентрацию кальция в сыворотке, снижать сывороточный уровень ПТГ и щелочной фосфатазы и способствовать ликвидации почечной остеомаляции. Однако у некоторых больных с почечной недостаточностью и изолированной остеомаляцией (без биохимических или гистологических признаков гиперпаратиреоза) введение 1,25-(OH) 2 -D быстро приводит к гиперкальциемии, но не излечивает заболевания костей. Хотя эти данные позволяют предполагать дефицит не только l,25-(OH) 2 -D, но и какого-то другого метаболита витамина D у соответствующих больных, результаты недавних исследований указывают на то, что остеомаляция в таких случаях могла бы быть связанной с отравлением алюминием. Пока не известно, могут ли введение 1,25-(ОН) 2 -D 3 и, следовательно, поддержание его нормальной концентрации в сыворотке наряду с коррекцией уровня фосфата в ней на ранних стадиях почечной недостаточности предупреждать развитие почечной остеодистрофии» по мере прогрессирования этой недостаточности. Поскольку l,25-(OH) 2 -D усиливает всасывание кальция и фосфора в кишечнике, возникающее в результате этого повышение их содержания в сыворотке могло бы вызвать кальцификацию мягких тканей и тем самым ускорять развитие почечной недостаточности.
Концентрация l,25-(OH) 2 -D в сыворотке снижена или неадекватно возрастает при некоторых расстройствах, сопровождающихся нарушением регуляции синтеза этого соединения в почках. Низкий уровень l,25-(OH) 2 -D в сыворотке отмечается у больных с послеоперационным или идиопатическим гипопаратиреозом. Введение таким больным экстракта околощитовидных желез нормализует содержание этого соединения в сыворотке, что может объясняться как непосредственным действием ПТГ, так и сопутствующей фосфатурией и уменьшением концентрации фосфата в сыворотке. У больных с псевдогипопаратиреозом уровень l,25-(OH) 2 -D в сыворотке также снижен, но он не повышается после введения экстракта околощитовидных желез. Однако, введение дибутирил-цАМФ больным с псевдогипопаратиреозом I типа увеличивает сывороточную концентрацию l,25-(OH) 2 -D. Дибутирил-цАМФ действует, но всей вероятности, за счет «обхода» имеющегося у таких вольных дефекта белка, сопрягающего взаимодействие рецептора ПТГ с аденилатциклазой, Снижение уровня 1,25-(OH) 2 -D в сыворотке крови у больных с гипопаратиреозом и псевдогипопаратиреозом, по-видимому, играет роль в патогенезе возникающей при этом гипокальциемии, так как его введение может в таких случаях поддерживать нормальную концентрацию кальция в сыворотке.
Возможность нарушения метаболизма витамина D изучали также при состояниях, связанных с гипофосфатемией, сопровождающейся рахитом или остеомаляцией. У больных с Х-сцепленным гипофосфатемическим рахитом концентрация l,25-(OH) 2 -D в сыворотке может быть ниже, чем у здоровых людей соответствующего возраста, что свидетельствует о нарушении синтеза этого вещества в дополнение к известному основному дефекту в транспорте фосфата. Существует экспериментальная модель Х-сцепленного гипофосфатемического рахита у мышей, у которых также обнаруживают несколько пониженную концентрацию l,25-(OH) 2 -D в плазме. Больше того, при ограничении фосфата в их пище эта концентрация резко снижается, тогда как при ограничении Са она повышается. Эти данные свидетельствуют в пользу точки зрения, согласно которой при Х-сцепленном гипофосфатемическом рахите нарушается регуляция активности 1α-гидроксилазы фосфатом. Состояние скелета у таких больных улучшается при введении им (наряду с добавками фосфата) физиологических доз l,25-(OH) 2 -D. Аналогичное нарушение регуляции почечного синтеза l,25-(OH) 2 -D фосфатом может происходить у больных с приобретенной гипофосфатемической остеомаляцией, наблюдаемой при мезенхимальных опухолях.
Ткани-мишени
За последние несколько лет появились описания случаев рахита на фоне повышенного уровня l,25-(OH) 2 -D в сыворотке у детей. У некоторых больных, помимо поражения костей, отмечаются алопеция и (или) аномалии зубов. Недавно проведенные исследования на культуре фибробластов кожи от таких больных выявили отсутствие или нарушение рецепторов l,25-(OH) 2 -D, которые определяются в культивируемых фибробластах у здоровых лиц. Эти примеры, таким образом, доказывают существование болезни, которая может быть следствием аномалии рецепторов, опосредующих действие метаболитов витамина D.
ИЗБЫТОК ВИТАМИНА D
Интоксикация витамином D
Избыточное потребление витамина D - 100 000 ЕД/сут или более (свыше 6,5 мкмоль, или 2,5 мг/сут) сопровождается гиперкальциемией и метастазирующей кальцификацией многих органов. Эта патология является, по-видимому, результатом непосредственного действия витамина D или, что более вероятно, 25-ОН-D 3 на ткани-мишени, так как содержание l,25-(OH) 2 -D в плазме остается нормальным. Гиперкальциемия часто сохраняется даже после отмены витамина D, что объясняется, очевидно, длительностью периода полужизни 25-OH-D, равно как и накоплением витамина D в жировой ткани, мышцах и печени. При терапевтическом использовании 25-OH-D 3 или l,25-(OH) 2 -D 3 также имеется опасность возникновения гипергкальциемии и кальцификации мягких тканей, но при отмене 1,25-(OH) 2 -D 3 она вскоре исчезает вследствие быстрого клиренса этого метаболита.
Первичный гиперпаратиреоз
Гиперпаратиреоз иногда сопровождается повышением уровня l,25-(OH) 2 -D в плазме, что отражает стимулирующее влияние ПТГ на почечный синтез этого соединения. С увеличением его концентрации в плазме у таких больных усиливается всасывание кальция в кишечнике и экскреция кальция с мочой. Имеются данные, что у больных первичным гиперпаратиреозом с повышенным уровнем l,25-(OH) 2 -D в плазме частота нефролитиаза как осложнения основного заболевания возрастает вследствие более выраженной гиперкальциурии. Однако по этому вопросу еще сохраняются противоречия.
Идиопатическая гиперкальциурия
У ряда больных с нефролитиазом гиперкальциурия регистрируется при отсутствии гиперкальциемии. В таких случаях говорят об идиопатической гиперкальциурии. Известно, что у этих больных всасывание кальция в кишечнике ускорено, а в недавних исследованиях у них отмечается также повышение уровря. l,25-(OH) 2 -D в плазме, что, вероятно, и обусловливает усиление всасывания кальция. По поводу действия механизма активации почечного синтеза l,25-(OH) 2 -D у таких больных сохраняются противоречивые мнения. У некоторых из них, возможно, имеется первичный дефект, заключающийся в потер0 кальция через почки, а также легкий вторичный гиперпаратиреоз; у других - наличие гипофосфатемии и, следовательно, какое-то нарушение метаболизма фосфата, приводящее к активации синтеза l,25-(OH) 2 -D. Возможность существования иных, механизмов активации его синтеза у больных этой группы остается неизвестной.
Саркоидоз
Саркоидоз может сопровождаться гиперкальциурией, гиперкальциемией и реже нефролитиазом или нефрокальцинозом. Показано, что гиперкальциурия и гиперкальциемия при саркоидозе сопровождают усиление всасывания в кишечнике и повышение чувствительности этого процесса к витамину D. Уровень 1,25-(OH) 2 -D в сыворотке у таких больных может быть исходно повышенным или чрезмерно возрастать при введении витамина D 2 . Так как у здоровых людей введение витамина D 2 не увеличивает содержания l,25-(OH) 2 -D в сыворотке, данные наблюдения указывают на нарушение регуляции синтеза последнего при саркоидозе, при котором он оказывается зависимым от доступности предшественников. Недавнее сообщение о лишенном почек и находящемся на диализе больном с саркоидозом и гиперкальциемией, у которого содержание l,25-(OH) 2 -D в сыворотке было повышенным, свидетельствует о возможности внепочечной продукции l,25-(OH) 2 -D при саркоидозе (предположительно - при саркоидной гранулеме).
Запись на прием к эндокринологу
Уважаемые пациенты, Мы предоставляем возможность записаться напрямую на прием к доктору, к которому вы хотите попасть на консультацию. Позвоните по номеру,указанному вверху сайта, вы получите ответы на все вопросы. Предварительно, рекомендуем Вам изучить раздел .
Как записаться на консультацию врача?
1) Позвонить по номеру 8-863-322-03-16 .
1.1) Или воспользуйтесь звонком с сайта:
Заказать звонок
Позвонить врачу
1.2) Или воспользуйтесь контактной формой.


