Селективная недостаточность IgA является самым часто встречающимся первичным иммунодефицитным состоянием (ПИДС). Встречаемость больных с селективным дефицитом IgА составляет от 1:400 до 1:1000 в европеоидной популяции и значительно ниже, от 1:4000 до 1:20000, в монголоидной . В США распространенность заболевания колеблется в пределах 1 на 223-1000 в группе исследованных до 1 на 400-3000 у здоровых доноров крови . В России подобные исследования не проводились.
Для этого состояния характерно избирательное снижение сывороточной концентрации IgA ниже 0,05 г/л (у детей старше четырех лет) при нормальном уровне других сывороточных иммуноглобулинов, нормальной реакции антител сыворотки крови и обычном клеточно-опосредованном иммунном ответе . В большинстве исследований частота встречаемости среди представителей мужского и женского пола была примерно одинаковой.
Люди с неспособностью производить IgA могут переносить свое заболевание бессимптомно за счет механизмов компенсации либо страдать частыми инфекциями дыхательной, пищеварительной или мочеполовой системы, гастроэнтерологической патологией (например, целиакией), склонностью к атопическим расстройствам, таким как поллиноз, бронхиальная астма, атопический дерматит, IgЕ-опосредованная пищевая аллергия, а также неврологическими и аутоиммунными заболеваниями (чаще всего это ревматоидный артрит, системная красная волчанка, идиопатическая тромбоцитопеническая пурпура, синдром Шегрена). При селективной недостаточности IgA аллергические заболевания, такие как атопический дерматит и бронхиальная астма, встречались в 40% случаев (Consilium Medicum, 2006). Также характерны для большинства таких пациентов анафилактические реакции при переливании компонентов крови и введении внутривенных иммуноглобулинов, что связано с наличием IgА в этих продуктах.
Клиническая симптоматика селективного дефицита IgА может проявиться в раннем детстве, с возрастом же частота и тяжесть переносимых инфекций может снизиться за счет компенсаторного повышения антител субклассов IgG1 и G3, IgМ. Другим объяснением отсутствия клинических симптомов может являться нормальный уровень секреторного IgA, несмотря на сокращение уровня сывороточного иммуноглобулина. Либо, напротив, некоторые пациенты с изначально диагностированным селективным дефицитом IgA могут развить клинику общей вариабельной иммунной недостаточности .
Терапия селективного дефицита IgА в настоящее время состоит в выявлении сопутствующих заболеваний, проведении профилактических мероприятий по снижению риска инфицирования, а также быстром и эффективном лечении инфекций.
Специфического лечения нет. Прогноз у пациентов с дефицитом IgA в целом хороший, если нет выраженных клинических проявлений. Недостаточность IgA у детей может восполниться с течением времени.
Будучи генетически обусловленными, иммунодефицитные состояния возникают из-за дефектов генетического аппарата. Пациенты с общей вариабельной иммунной недостаточностью и таковые с селективным дефицитом IgA часто выявляются в одной семье и имеют общий HLA-гаплотип; у многих имеются редкие аллели и делеции генов внутри класса МСН — класс 3 на хромосоме 6. Недавно было доказано, что некоторые семейные случаи общей вариабельной иммунной недостаточности и селективного дефицита IgA вызываются мутацией гена TNFRSF13B, который кодирует белок, известный как TACI (transmembrane activator and calcium-modulator and cyclophilin-ligand interactor). Вероятно, что в тех случаях, когда мутации TACI обнаружено не было, причиной возникновения заболеваний могли служить спонтанные или наследственные мутации других генов, до сих пор не зафиксированные.
В настоящее время достаточно подробно описаны возможные клинические проявления селективного дефицита IgА, варианты течения, возможные сопутствующие заболевания. Решающим в диагностике заболевания является избирательное снижение сывороточной концентрации IgA у детей начиная с 4 лет ниже 0,05 г/л при нормальном уровне других сывороточных иммуноглобулинов в повторных иммунограммах. Лечение состоит в выявлении сопутствующих заболеваний, проведении профилактических мер по снижению риска инфицирования, а также необходимо быстрое и эффективное лечение инфекционных заболеваний.
Информация о частоте встречаемости данного первичного иммунодефицитного состояния в российской популяции отсутствует, что не дает возможности сравнить распространенность заболевания в нашей стране с другими странами, где подобные исследования уже проводились.
Основной проблемой является отсутствие единых рекомендаций по тактике ведения больных с селективным дефицитом IgА.
С целью оценить частоту встречаемости селективного дефицита IgА среди детей группы диспансерного наблюдения «часто болеющие дети» и охарактеризовать спектр его клинических проявлений в Российской Федерации на базе ФГБУ «ФНКЦ ДГОИ имени Дмитрия Рогачева» МЗ РФ и ГБУЗ ДГКБ № 9 им. Г. Н. Сперанского ДЗМ была выполнена данная работа.
Материалы и методы исследования
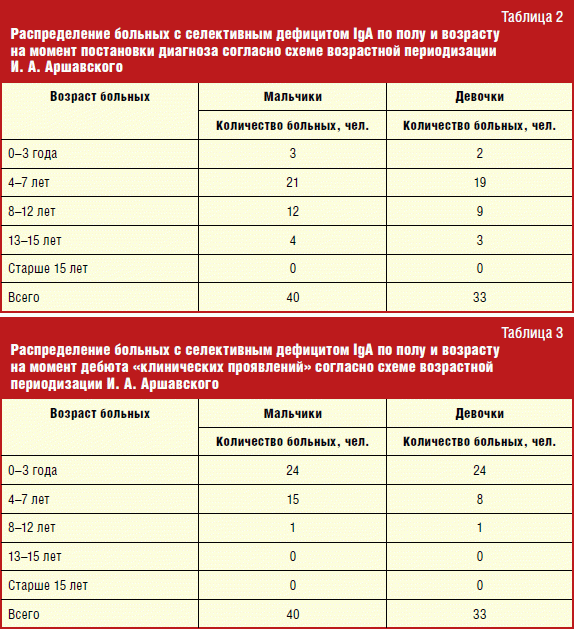
Объектом исследования стали дети с селективным дефицитом IgА, наблюдавшиеся в ГБУЗ ДГКБ № 9 им. Г. Н. Сперанского ДЗМ. Кроме того, ретроспективно был проведен анализ медицинской документации за период с 2003 по 2010 гг. 9154 пациентов из группы диспансерного наблюдения «часто болеющие дети» (табл. 1-3).
При обследовании применялись следующие методы:
- клинико-анамнестические;
- общий и биохимический анализы крови;
- иммунологическое исследование состава крови методами нефелометрии и проточной цитометрии;
- скарификационные пробы;
- определение специфических IgЕ методом иммуноблотинга;
- исследование функции внешнего дыхания;
- риноцитологическое исследование.
Диагноз селективного дефицита IgА ставился на основании избирательного снижения сывороточной концентрации IgA ниже 0,05 г/л при нормальных показателях других сывороточных иммуноглобулинов в повторных иммунограммах и исключении других возможных причин их недостаточности детям старше 4 лет.
При сборе анамнеза особое внимание уделялось частоте и спектру клинических проявлений, сопутствующей патологии, а также подробно изучался семейный анамнез. Клинический осмотр детей проводился в соответствии с общепринятыми методами. Содержание иммуноглобулинов классов A, G, M, E в сыворотке определялось методом нефелометрии на нефелометре BN 100 (Dade Bering, ФРГ) с использованием набора Dade Behring. Фенотипирование лимфоцитов проводилось методом проточной цитометрии на приборе FacsScan (Becton Dickenson, США) с использованием флюоресцентно меченых моноклональных антител Simultest (Becton Dickenson, США). Пациентам с какими-либо проявлениями атопии, а также всем пациентам с повышенным уровнем IgЕ, который был выявлен в результате оценки показателей иммунного статуса методом нефелометрии, проводилось аллергологическое дообследование методом скарификационных тестов у детей старше 4 лет либо методом определения специфических IgЕ в сыворотке крови пациентам, не достигшим 4-летнего возраста. Детям с установленным диагнозом «бронхиальная астма» или наличием бронхообструктивного синдрома в анамнезе проводилось исследование функции внешнего дыхания на аппарате Spirovit SP-1 (Schiller AG, Швейцария). Также проводилось все необходимое дообследование и консультации смежных специалистов с учетом имеющихся жалоб.
Результаты и их обсуждение
Ретроспективный анализ медицинской документации пациентов с направительными диагнозами «рецидивирующие ОРВИ», «ЧБД», «ЧБР», а также «ЭБД» позволил установить, что частота селективного дефицита IgА у этой группы детей в два, а то и в три раза выше, чем в популяции.
Абсолютное количество, а также процентную долю детей с этим первичным иммунодефицитом по годам можно увидеть в табл. 4.
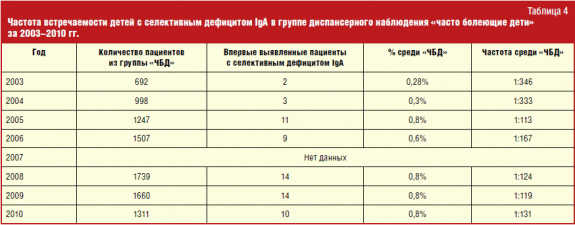
К сожалению, данные за 2007 г. недоступны. В 2003 и 2004 гг. было проконсультировано 692 и 998 детей. Среди них было выявлено в общей сложности 5 пациентов с селективным дефицитом IgА, что чуть чаще, чем в среднем по популяции — 1:346 и 1:333 соответственно против 1:400-600. Начиная же с 2005 г. частота впервые выявленных пациентов с этим ПИДС резко увеличилась: 1:113 в 2005 г., 1:167 в 2006 г., 1:124 в 2008 г., 1:119 в 2009 г. и, наконец, 1:131 в 2010 г. В ходе исследования частота встречаемости менялась с 1:346 в 2003 г. до 1:131 в 2010, когда она оказалась максимальной в сравнении с предыдущими годами. Повышение частоты встречаемости пациентов с селективным дефицитом IgА на третий год после начала работы следует связать с повышенной настороженностью докторов в отношении этой патологии, а также с совершенствованием лабораторной диагностики. Необходимо продолжать расширять знания докторов о данном заболевании, поскольку поток детей, которых родители приводят к иммунологу с жалобами на частые заболевания, увеличивается из года в год.
В ходе данной работы также было проспективно обследовано 235 детей и 32 взрослых.
Основная группа составила 73 ребенка с диагностированным селективным дефицитом IgА.
Вторая группа пациентов включила в себя 153 ребенка с идиопатической тромбоцитопенической пурпурой (ИТП). Оценка иммунного статуса пациентам с ИТП проводилась с целью выявить среди них селективный дефицит IgA, поскольку данная корреляция описана в мировой литературе и такие же данные были получены в ходе данного исследования. Ни одного ребенка с отсутствием IgА среди них нами выявлено не было. Несмотря на то, что при обследовании иммунного статуса пациентов с ИТП нам не удалось выявить среди них селективный дефицит IgA, были выявлены другие малые гуморальные дефекты: дефицит субклассов IgG, младенческая гипогаммаглобулинемия, парциальное снижение IgА.
Третья группа включила в себя 32 взрослых в возрасте от 20 до 54 лет, а также 8 детей в возрасте от 4 до 10 лет, являющихся ближайшими родственниками пациентов с селективным дефицитом IgА, которым производилась оценка иммунного статуса с целью поиска и описания семейных случаев.
В ходе обследования и анализа полученных данных были получены описанные далее результаты.
Соотношение мужского и женского пола среди пациентов с селективным дефицитом IgА было примерно одинаковым. Обследовано 40 мальчиков и 33 девочки. Это соответствует данным мировой литературы.
Пик выявляемости селективного дефицита IgА приходился на возраст 4-7 лет. Повторные инфекционные заболевания, как правило, возникали в раннем возрасте либо с началом посещения детского дошкольного учреждения. Как правило, прежде чем попасть к иммунологу, дети накапливали определенный инфекционный анамнез, поскольку есть определенные признаки, позволяющие заподозрить у них ПИДС. И, кроме того, даже если исследование проводилось в более раннем возрасте и выявлялось отсутствие IgА до 4 лет, это не позволяло нам поставить однозначный диагноз ПИДС, мы не могли до конца исключить незрелость системы синтеза иммуноглобулинов. Поэтому до 4 лет диагноз выставлялся по вопросам и рекомендовалось наблюдение в динамике. Отсюда и интервал 4-7 лет соответственно.
Ведущими жалобами при обращении у детей с селективным дефицитом IgA были частые респираторные вирусные инфекции с неосложненным течением. Дебют рецидивирующих респираторных заболеваний, как правило, приходился на возраст до 3 лет. Это также соответствует данным мировой литературы. Поскольку динамический контроль за большинством пациентов нашего исследования осуществлялся длительно, в течение нескольких лет, порой до перехода пациента во взрослую сеть, можно утверждать, что с возрастом частота и тяжесть переносимых инфекций снижалась. Предположительно это происходило за счет компенсаторного повышения антител субклассов IgG1 и IgG3, IgМ, однако этот вопрос требует дальнейшего изучения. Второй по частоте жалобой при обращении были частые ОРВИ, протекающие с осложнениями. Частота осложненных, атипично протекавших ОРВИ с возрастом у наших пациентов, как показало динамическое наблюдение, также снижалась.
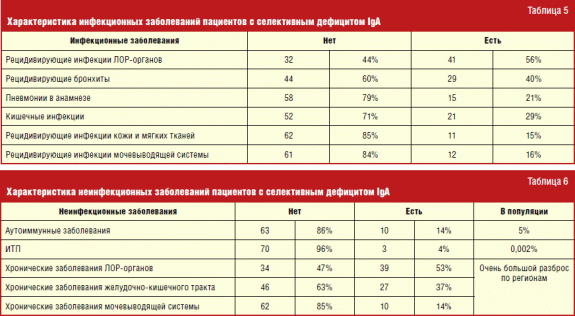
Из спектра инфекционных заболеваний у больных с селективным дефицитом IgА ведущее место занимали инфекционные заболевания ЛОР-органов и инфекции нижних дыхательных путей. Это связано с тем, что снижение секреторного IgA, являющегося частью местного иммунитета, приводит к легкому инфицированию и размножению микроорганизмов на слизистых, наиболее уязвимых при контактах с инфекционными заболеваниями, передающимися воздушно-капельным путем.
В спектре неинфекционных заболеваний была выявлена очевидная корреляция с аутоиммунными заболеваниями, которые являются наиболее важными проявлениями селективного дефицита IgА, в частности, с идиопатической тромбоцитопенической пурпурой (1,5-2 на 100 тысяч).
Из аутоиммунных заболеваний у пациентов с селективным дефицитом IgА наиболее часто встречались ювенильный ревматоидный артрит (4 раза), хроническая идиопатическая тромбоцитопеническая пурпура (3 раза), аутоиммунный гепатит (3 раза). Помимо этого, по данным мировой литературы, у пациентов с селективным дефицитом IgА отмечается повышенная частота аутоиммунных состояний среди ближайших родственников. Но, по данным нашего исследования, их число не превысило общепопуляционных значений.
Частота атопических заболеваний среди пациентов с селективным дефицитом IgА оказалась значительно выше, чем в популяции (табл. 4). Только частота аллергического ринита сравнима с общепопуляционной. Подобные наблюдения отражены в ряде ранее проводимых исследований. Нельзя сказать, что аллергические заболевания у большинства пациентов с дефицитом IgА протекают более тяжело, чем у людей без данного иммунологического дефекта. Однако большая распространенность атопии дает повод поставить вопрос о проведении иммунологического обследования с целью выявления форм селективного дефицита IgА, которые пока клинически никак себя не проявили. Хоть это, возможно, и не будет иметь решающей роли в плане подхода к терапии по текущему атопическому состоянию, но поможет своевременно поставить диагноз и снизить возможные риски для людей, у которых селективный дефицит IgА будет обнаружен.
При анализе повторных иммунограмм в ходе динамического наблюдения у детей с селективным дефицитом IgА, в связи со стойкими изменениями лабораторных показателей, были выделены две большие группы пациентов. В группе А отмечалось отсутствие IgА без каких-либо других изменений. В группе В отсутствие IgА сочеталось со стойким повышением уровня IgG. Был проведен сравнительный анализ этих групп пациентов.

Возраст дебюта клинических проявлений в этих группах достоверно не отличался.
Было выявлено, что у пациентов с селективным дефицитом IgА повышение уровня IgG коррелирует с повторными инфекционными заболеваниями кожи и мягких тканей. Этот вопрос требует дальнейшего изучения.
При сравнении указанных групп пациентов значимых отличий в спектре аллергопатологии выявлено не было.
В ходе работы была проведена оценка иммунного статуса в 20 семьях пациентов с селективным дефицитом IgА. Было выявлено 4 семейных случая. Кроме того, собирался подробный семейный анамнез. Среди взрослых родственников с отягощенным инфекционным анамнезом, которым удалось провести обследование, имели место те или иные нарушения гуморального иммунитета. Соответственно, при выявлении малых гуморальных дефектов (в частности, селективного дефицита IgA) обследование ближайших родственников, особенно при наличии отягощенного инфекционного анамнеза, является обязательным.
В связи с тем что селективный дефицит IgА среди детей группы диспансерного наблюдения «часто болеющие дети» встречается значительно чаще, чем в общей детской популяции, практикующим педиатрам необходимо быть настороженными относительно этого заболевания. Заподозрить его не всегда просто, поскольку клинические проявления очень вариабельны: от бессимптомных форм до рецидивирующих бактериальных инфекций с потребностью в частой антибактериальной терапии. Рекомендуется расширять знания педиатров и узких специалистов амбулаторного и стационарного звена о малых дефектах гуморального звена иммунитета.
Поскольку среди пациентов с селективным дефицитом IgА значительно выше частота аллергической патологии (бронхиальная астма, атопический дерматит, пищевая аллергия), выше частота аутоиммунных заболеваний и гематологических заболеваний, а также частота хронических заболеваний (ЛОР-органов, мочеполовой системы, желудочно-кишечного тракта), чем в популяции, его выявление является обязательным с целью оказания полноценной и свое-временной медицинской помощи пациентам.
Рекомендуется обязательно направлять на консультацию к иммунологу/иммунологическое обследование детей с отягощенным инфекционным анамнезом, пациентов с гематологическими и аутоиммунными заболеваниями, проводить скрининговое обследование уровня общего IgА пациентам с наличием аллергических заболеваний.
В ходе исследования было установлено, что у большинства детей с селективным дефицитом IgА отмечалась корреляция наличия аутоиммунной патологии и стойкого повышения IgG в повторных иммунограммах. При других заболеваниях такой корреляции установлено не было. Подобные изменения показателей являются фактором риска развития у ребенка аутоиммунной патологии и требуют особенного внимания.
Несмотря на то, что корреляции между наличием семейной истории селективного дефицита IgА и тяжестью клинических проявлений у пациентов установлено не было, для данных пациентов обследование ближайших родственников, особенно при наличии отягощенного инфекционного анамнеза, является обязательным.
Литература
- Hammarstrom L., Lonnqvist B., Ringden O., Smith C. I., Wiebe T. Transfer of IgA deficiency to a bone-marrow-grafted patient with aplastic anaemia // Lancet. 1985; 1 (8432): 778-781.
- Latiff A. H., Kerr M. A. The clinical significance of immunoglobulin A deficiency // Annals of Clinical Biochemistry. 2007; 44 (Pt 2): 131-139.
- Al-Attas R. A., Rahi A. H. Primary antibody deficiency in Arabs: first report from eastern Saudi Arabia // Journal of Clinical Immunology. 1998; 18 (5): 368-371.
- Carneiro-Sampaio M. M., Carbonare S. B., Rozentraub R. B., de Araujo M. N., Riberiro M. A., Porto M. H. Frequency of selective IgA deficiency among Brazilian blood donors and healthy pregnant women // Allergology Immunopathology (Madr). 1989; 17 (4): 213-216.
- Ezeoke A. C. Selective IgA deficiency (SIgAD) in Eastern Nigeria // African Journal of Medicine and Medical Sciences. 1988; 17 (1): 17-21.
- Feng L. Epidemiological study of selective IgA deficiency among 6 nationalities in China // Zhonghua Yi Xue Za Zhi. 1992; 72 (2): 88-90, 128.
- Pereira L. F., Sapina A. M., Arroyo J., Vinuelas J., Bardaji R. M., Prieto L. Prevalence of selective IgA deficiency in Spain: more than we thought // Blood. 1997; 90 (2): 893.
- Wiebe V., Helal A., Lefranc M. P., Lefranc G. Molecular analysis of the T17 immunoglobulin CH multigene deletion (del A1-GP-G2-G4-E) // Human Genetics. 1994; 93 (5): 5.
Л. А. Федорова*,
Е. С. Пушкова*
И. А. Корсунский** , 1 ,
кандидат медицинских наук
А. П. Продеус*,
доктор медицинских наук, профессор
Иммунодефицит - снижение количественных показателей и/или функциональной активности основных компонентов иммунной системы, приводящее к нарушению защиты организма от патогенных микроорганизмов и проявляющееся повышенной инфекционной заболеваемостью.
Как известно, основная функция системы иммунитета - распознавание и элиминация чужеродных веществ антигенной природы, проникающих в организм из окружающей среды (микроорганизмы) или возникающих эндогенно (опухолевые клетки). Эта функция реализуется с помощью факторов врождённого иммунитета (фагоцитоза, противомикробных пептидов, белков системы комплемента, системы NK-клеток и др.) и приобретённого, или адаптивного иммунитета, осуществляемого с помощью клеточного и гуморального иммунных ответов. Регуляция активности компонентов иммунной защиты организма и их взаимодействие происходит с помощью цитокинов и межклеточных контактов.
В каждом из перечисленных компонентов иммунной системы, а также в механизмах их регуляции могут возникнуть нарушения, приводящие к развитию иммунодефицита, основное клиническое проявление которого - повышенная чувствительность к возбудителям инфекционных заболеваний. Различают 2 вида иммунодефицитов: первичные и вторичные.
Первичные иммунодефициты (ПИД) - наследственные заболевания, обусловленные дефектами генов, контролирующих иммунный ответ. ПИД - заболевания, разнообразные по характеру и выраженности иммунных дефектов, клинических проявлений и молекулярных нарушений. Для клинической картины ПИД характерны повторные и хронические, тяжело протекающие инфекционные процессы, в большей степени бронхолёгочной системы
и ЛОР-органов, кожи и слизистых оболочек; могут развиться гнойные лимфадениты, абсцессы, остеомиелит, менингит и сепсис. При некоторых формах имеются проявления аллергии, аутоиммунных заболеваний и возможно развитие некоторых злокачественных опухолей. Следует обращать внимание на отставание по возрастным показателям физического развития. В настоящее время описано около 80 ПИД, выявлены гены, ответственные за развитие большинства этих заболеваний. Адекватные лабораторные анализы позволяют дифференцировать патологию на уровне лимфоцитов и патологию на уровне нелимфоцитарных механизмов деструкции и выведения антигенов.
Распространённость ПИД зависит от формы заболевания и в среднем составляет от 1:10 000 до 1:100 000 новорождённых. Селективный дефицит IgA, например, встречается гораздо чаще от 1:500 до 1:1500 человек общей популяции. Распространённость различных форм ПИД варьирует в разных странах. Наиболее часто встречаются дефекты антителообразования - 50-60% случаев, комбинированные ПИД - 10-30%, дефекты фагоцитоза - 10-20%, дефекты комплемента - 1-6%. Большинство ПИД манифестируют в раннем детстве, хотя возможно и более позднее начало некоторых форм ПИД, в частности общей вариабельной иммунологической недостаточности (ОВИН).
По механизмам развития выделяют 4 основные группы ПИД:
1-я группа - преимущественно гуморальные, или В-клеточные
ПИД;
2-я группа - комбинированные ПИД (при всех Т-клеточных иммунодефицитах есть нарушение функции В-клеток);
3-я группа - ПИД, обусловленные дефектами фагоцитоза;
4-я группа - ПИД, обусловленные дефектами в системе комплемента.
Принципы диагностики первичных иммунодефицитов
Ранняя диагностика и своевременное начало лечения определяют прогноз заболевания. Постановка диагноза на уровне участковых педиатров представляет определённые трудности, что нередко обусловлено отсутствием возможности своевременного консультирования больного врачом-иммунологом и проведения специального лабораторного иммунологического обследования (табл. 11-1). Хотя знание особенностей клинической картины ПИД и измене-
ния в общеклинических лабораторных анализах позволяют заподозрить ПИД и направить больного к специалистам. Европейское общество по иммунодефицитам разработало протоколы ранней диагностики ПИД, а также создало электронную базу данных Европейского регистра ПИД. Алгоритм диагностики ПИД показан на рис. 11-1.
Таблица 11-1. Этапы иммунологического обследования при подозрении на иммунодефицит
Рис. 11-1. Алгоритм диагностики первичных иммунодефицитов
Общие особенности клинической картины первичных иммунодефицитов
Ведущим в клинической картине ПИД является так называемый инфекционный синдром - повышенная восприимчивость к возбудителям инфекционных заболеваний в целом, необычно тяжёлое рекуррентное (рецидивирующее) их клиническое течение, наличие в этиологии заболевания атипичных возбудителей (часто оппортунистических). Тип возбудителя определяется характером иммунного дефекта. При дефектах антителообразования удаётся выявить устойчивую к антибактериальным препаратам флору - стафилококков, стрептококков, гемофильную палочку. При Т-клеточной иммунной недостаточности помимо бактерий выявляют вирусы (например, семейство герпесвирусов), грибки (Candida spp., Aspergillus и др.), а при фагоцитарных дефектах - стафилококки, грамотрицательные бактерии, грибки и т.д.
Лабораторные исследования
Если клинические данные позволяют заподозрить ПИД, то следует провести следующие исследования:
Определение развёрнутой формулы крови (особенно важны количественные и процентные показатели лимфоцитов);
Определение уровней IgG, IgA и IgM в сыворотке крови;
Подсчёт субпопуляций T- и B-лимфоцитов;
◊ анализ функционального состояния фагоцитов (наиболее простой и информативный анализ - тест на восстановление тетразолиевого синего);
◊ анализ на содержание основных компонентов комплемента (начинают с C3 и C4);
◊ анализ на ВИЧ-инфекцию (если есть возможные факторы риска);
◊ молекулярно-генетические исследования при показаниях.
Принципы лечения первичных иммунодефицитов
Главная цель терапии ПИД - лечение осложнений заболевания и их профилактика. Этот подход вызван тем, что дефекты иммунной системы при ПИД заложены на генетическом уровне. В настоящее время проводят интенсивные исследования по ген-
ной терапии иммунодефицитов, что может привести к появлению более радикальных методов их лечения.
В зависимости от формы ПИД лечение заключается в проведении заместительной терапии, лечении и профилактике инфекционных, аутоиммунных проявлений заболевания, лечении злокачественных новообразований и применении специальных методов, включая трансплантацию гемопоэтических стволовых клеток (в зависимости от типа ПИД).
ДЕФЕКТЫ ИММУНОГЛОБУЛИНОВ
Транзиторная гипогаммаглобулинемия у детей
Транзиторная гипогаммаглобулинемия у детей связана с физиологической особенностью поэтапного формирования системы иммуноглобулинов. В наибольшей степени «запаздывает» созревание IgM и IgA антителообразования. У здоровых детей содержание материнских IgG постепенно снижается и после полугода возрастает выработка собственных IgG-антител. У некоторых детей, однако, нарастание уровня иммуноглобулинов задерживается. Такие дети могут страдать рекуррентными бактериальными инфекционными заболеваниями. В этих случаях не следует прибегать к инфузиям препаратов донорских иммуноглобулинов (введению внутривенного иммуноглобулина).
Селективный дефицит иммуноглобулина A
Селективный дефицит иммуноглобулина A (SD IgA - Selective Deficiency of IgA) развивается в результате дефекта гена tnfrsf13b
или р). Дефицит IgA при наличии иммуноглобулинов других классов - самый частый иммунодефицит, выявляемый в общей популяции с частотой 1:500-1500 человек (у больных, страдающих аллергией, ещё чаще). Различают недостаточность IgA селективную, т.е. заключающуюся в дефиците одного из подклассов (30% случаев), и полную (70% случаев). Дефицит подкласса IgA2 приводит к более выраженной клинической картине, чем дефицит подкласса IgA1. Возможны и сочетания дефицита IgA с другими нарушениями: с дефектом биосинтеза IgG и с аномалиями T-лимфоцитов. Подавляющее большинство лиц с селективным
дефицитом IgA практически здоровы. Для детей моложе 2 лет дефицит IgA - физиологическое состояние.
Выявляют снижение концентрации сывороточного IgA до <5 мг/дл у детей старше 4 лет; IgG и IgM в норме, количество и соотношение субпопуляций лимфоцитов и их функциональная активность могут быть в норме.
Клиническая картина. При дефиците IgA могут развиваться 3 группы патологических синдромов: инфекционный, аутоиммунный и аллергический. Пациенты с дефицитом IgA предрасположены к рецидивирующим инфекционным заболеваниям верхних дыхательных путей и органов пищеварения. Наиболее частыми и тяжело протекающими являются разнообразные аутоиммунные заболевания (ревматоидный артрит, анкилозирующий спондилит, синдром Шегрена, васкулит с поражением сосудов мозга, аутоиммунный тиреоидит, СКВ, гломерулонефрит, гемолитическая анемия, сахарный диабет I типа, витилиго и др.). Частота встречаемости целиакии превышает таковую у детей с нормальным IgA в 10 раз. Наиболее часто выявляемые аллергические проявления: непереносимость белка коровьего молока, атопический дерматит (АтД), бронхиальная астма.
Лечение. Случаи бессимптомного течения не требуют никакого специального лечения; при наличии клинических проявлений инфекционных, аутоиммунных и аллергических заболеваний проводят лечение в соответствии со стандартами.
Заместительная терапия донорскими иммуноглобулинами не показана ни при селективном, ни при полном дефиците IgA, поскольку высока вероятность образования у реципиента антиизотипических антител к IgA и развития обусловленных ими трансфузионных осложнений.
Агаммаглобулинемия с дефицитом В-клеток
X-сцепленная агаммаглобулинемия (болезнь Брутона) составляет 90% всех случаев агаммаглобулинемии. Болеют мальчики, сыновья (אּ, ρ) носительниц дефектного гена btk (Xq21.3-q22), кодирующего специфичную для B-лимфоцитов протеинтирозинкиназу Btk (Bruton"s tyrosine kinase - тирозинкиназа Брутона). В результате дефекта происходит нарушение внутриклеточных сигнальных путей, рекомбинация тяжёлых цепей иммуноглобулинов, диффе-
ренцировка пре B-клеток в B-лимфоциты. У 10% больных агаммаглобулинемия с дефицитом В-клеток наследуется аутосомнорецессивно. В настоящее время описано 6 генетических дефектов, включая молекулы пре-В-клеточного рецептора, цитоплазматического адапторного протеина В-клеток (BLNK) и гена Leucine-Rich Repeat-Containing 8 (LRRC8).
Данные лабораторных исследований. Отсутствуют периферические B-лимфоциты. В костном мозге присутствуют пре-B-клетки с μ-цепью в цитоплазме. Число T-лимфоцитов и функциональные тесты на T-лимфоциты могут быть норме. IgM и IgA в крови выявить не удаётся; IgG может присутствовать, но в малых количествах (0,4-1,0 г/л). Нет антител к антигенам групп крови и к вакцинным антигенам (столбнячному, дифтерийному токсинам и др.). Может развиваться нейтропения. Гистологическое исследование лимфоидной ткани: в лимфоидных фолликулах нет герминативных (зародышевых) центров и плазматических клеток.
Клиническая картина. Если семейный анамнез неизвестен, то диагноз становится очевидным в среднем к возрасту 3,5 лет. Для заболевания характерны гипоплазия лимфоидной ткани, тяжело протекающие гнойные инфекции, инфекционные заболевания верхних (синуситы, отиты) и нижних (бронхиты, пневмонии) дыхательных путей; возможны гастроэнтериты, пиодермии, септические артриты (бактериальные или хламидиозные), септицемия, менингит, энцефалит, остеомиелит. В качестве возбудителей заболеваний дыхательных путей чаще всего выступают Haemophilus influenzae, Streptococcus pneumoniae, Staphylococcus aureus, диареи кишечные бактерии или лямблии Giardia lamblia. Также пациенты с агаммаглобулинемией подвержены инфекционным заболеваниям, вызванным микоплазмами и уреаплазмами, являющимися причиной развития хронических пневмоний, гнойных артритов, циститов и абсцессов подкожной клетчатки. Из вирусов типичны нейротропные вирусы ECHO-19 и коксаки, вызывающие как тяжёлые острые, так и хронические энцефалиты и энцефаломиелиты. Проявлениями энтеровирусных инфекций могут быть дерматомиозитоподобный синдром, атаксия, головные боли, нарушения поведения. У больных детей при иммунизации живой полиовакциной, как правило, выявляют продолжительное выделение через слизистые оболочки вируса полиомиелита, причём с восстановленной и нарастающей вирулентностью (т.е. в детском коллекти-
ве реальна опасность заражения здоровых детей полиомиелитом в результате контакта с вакцинированным иммунодефицитным ребёнком). Аутоиммунные нарушения при агаммаглобулинемии могут быть представлены ревматоидным артритом, склеродермоподобным синдромом, склередемой, неспецифическим язвенным колитом, сахарным диабетом I типа (обусловлены преобладанием Th1 иммунного ответа).
Физикальный осмотр. Обращают внимание на отставание в физическом развитии, на форму пальцев (пальцы в виде барабанных палочек), изменения формы грудной клетки, характерные для заболеваний нижних дыхательных путей, гипоплазию лимфатических узлов и миндалин.
Лечение.
Заместительная терапия: препараты внутривенного иммуноглобулина вводят каждые 3-4 нед пожизненно. Дозы иммуноглобулинов подбирают так, чтобы создать в сыворотке больного их концентрацию, перекрывающую нижнюю границу возрастной нормы.
Обсуждают возможность генной терапии - ген Btk клонирован, однако его гиперэкспрессия ассоциирована со злокачественной трансформацией кроветворной ткани.
В случае упорной нейтропении применяют ростовые факторы. При появлении признаков аутоиммунной патологии возможно назначение препаратов моноклональных антител (инфликсимаб и др.).
Общая вариабельная иммунная недостаточность
Общая вариабельная иммунная недостаточность (ОВИН) - группа синдромов, характеризующихся дефектом синтеза антител и клеточного иммунитета. Достоверный диагностический критерий ОВИН - значительное снижение содержания иммуноглобулинов двух или трёх основных изотипов у лиц обоего пола в сочетании с одним из нижеперечисленных признаков:
Дебютом заболевания в возрасте старше 2 лет;
Отсутствием изогемагглютининов и/или низким ответом на вакцинацию;
Исключении других причин агаммаглобулинемии.
У некоторых больных причина развития ОВИН - мутации генов, кодирующих молекулы, вовлечённые в процессы созревания и выживания В-клеток: BAFF-R (B-cell Activating Factor Receptor), Blimp-1 (B-lymphocyte induced maturation protein-1) и ICOS (Inducible costimulator). Происходит нарушение способности B-лимфоцитов дифференцироваться в плазматические клетки, развиваются дефекты антителообразования, возможна дисфункция T-лимфоцитов, наблюдается повышенная склонность к инфекционным заболеваниям. Синдром может проявляться в раннем детстве, в подростковом возрасте или у молодых людей.
Данные лабораторных исследований. Существенно снижены уровни IgG и IgA (примерно у 50% больных) и IgM (вплоть до невыявляемых количеств). Число B-лимфоцитов в крови соответствует норме или снижено. Число T-лимфоцитов у большинства больных в норме. У тяжёлых больных возможно развитие лимфопении (менее 1500x10 3 клеток в 1 л крови). Число NK-клеток снижено. Выработка специфических антител в ответ на иммунизацию снижена или отсутствует. Пролиферация лимфоцитов и образование ИЛ-2 под действием митогенов и антигенов значительно нарушены.
Клиническая картина. Выявляют рекуррентные бактериальные инфекционные заболевания с локализацией преимущественно в дыхательных путях и околоносовых пазухах. К моменту постановки диагноза инфекции дыхательных путей могут прогрессировать до бронхоэктазов и разлитых поражений лёгочной ткани. Возможно инфекционное поражение органов пищеварения, проявляющееся диареей, стеатореей и мальабсорбцией (и соответственно потерей массы тела). Часто выявляют инфекции, вызванные Giardia lamblia, Pneumocystis carinii или вирусами семейства Herpetoviridae. Больные ОВИН склонны к развитию гнойных артритов, вызываемых микоплазмами и уреаплазмами. Проявлениями энтеровирусных инфекций могут быть энцефаломиелиты, полиемиелито- и дерматомиозитоподобный синдромы, поражения кожи и слизистых оболочек. Аутоиммунные заболевания протекают тяжело и могут определять прогноз ОВИН. Иногда первыми клиническими проявлениями ОВИН являются артрит, неспецифический язвенный колит и болезнь Крона, склерозирующий холангит, мальабсорбция, СКВ, нефрит, миозит, аутоиммунное поражение лёгких в виде лимфоидного интерстициального пневмонита, нейтропения,
тромбоцитопеническая пурпура, гемолитическая анемия, пернициозная анемия, тотальная алопеция, васкулит сетчатки, фотосенсибилизация. У больных ОВИН значительно повышена частота (в 15% случаев), саркоидозоподобных гранулём и незлокачественной лимфопролиферации. Лечение.
Противобактериальная химиотерапия.
Заместительная терапия: препараты внутривенного иммуноглобулина вводят каждые 3-4 нед пожизненно.
При аутоиммунных осложнениях - иммуносупрессивная терапия (глюкокортикоиды, азатиоприн, циклоспорин А) и возможно назначение препаратов моноклональных антител (инфликсимаб и др.).
Гипер-IgМ-синдромы
Гипер-IgM-синдромы - довольно редкие заболевания, характеризуемые выраженным снижением или полным отсутствием IgG, IgA и нормальной или повышенной концентрацией сывороточного IgM. Это вызвано неспособностью В-лимфоцитов осуществлять переключение классов иммуноглобулинов и гипермутагенез вариабельных доменов. К настоящему времени идентифицировано 6 генетических дефектов, приводящих к развитию гипер-IgMсиндрома.
. Тип 1 (HIGM 1). Х-сцепленный дефицит CD40 лиганда (70% случаев гипер-IgM-синдромов), приводящий к неспособности Т-клеток эффективно взаимодействовать с В-лимфоцитами.
. Тип 2 (HIGM 2). Аутосомно-рецессивный, связанный с дефектом AID - индуцированной активацией цитидин дезаминазы (ген Aicda, 12р13) - фермента, участвующего в переключении классов иммуноглобулинов и гипермутагенезе.
. Тип 3 (HIGM 3). Аутосомно-рецессивный, связанный с мутацией гена молекулы CD40. При этом В-клетки сами по себе не способны эффективно взаимодействовать с Т-лимфоцитами. Фенотипические проявления сходны с таковыми для типа 1.
. Тип 4 (HIGM 4). Аутосомно-рецессивный; в некоторых случаях мутации возникают de novo. Cвязан с дефектом UNG - урацил-ДНК-гликозилазы - фермента, тоже участвующего
в переключении классов иммуноглобулинов, но уже после действия AID. В этом случае гипермутагенез не затронут и синдром протекает с меньшей тяжестью.
. Тип 5 (HIGM 5). Дефект только в переключении классов, гипермутагенез не затронут. Причинная мутация пока не выявлена, но, очевидно, дефект в ферменте, действующем после
AID.
. Тип 6 (HIGM-ED). Х-сцепленный, ассоциированный с дисгидротической эктодермальной дисплазией, вызван дефицитом NEMO (модулятора NF-kB), приводящим к нарушению передачи сигнала с CD40.
X-сцепленный гипер-IgM-синдром выявляют чаще других. Развивается при дефекте гена, кодирующего CD40L (CD154, ген расположен на Xq26-q27.2) - лиганд для CD40. Недостаточность экспрессии CD40L T-лимфоцитами приводит к невозможности переключения классов иммуноглобулинов в B-лимфоцитах с IgM на другие изотипы, а также к нарушению формирования B-клеток памяти, Т-клеточного репертуара и Th1-клеточного ответа, направленного против внутриклеточных микроорганизмов. Болеют мальчики
Данные лабораторных исследований. IgG, IgA, IgE определить не удаётся или выявляются в очень малых количествах. Уровень IgM в норме (в 50% случаев) или повышен, зачастую значительно. Количество Т- и В-клеток в норме; снижен пролиферативный ответ Т-клеток, индуцированный антигенами. IgM поликлональны, иногда моноклональны. Выявляют аутоантитела IgM изотипа (антиэритроцитарные, антитромбоцитарные, антитиреоидные, антитела к антигенам гладкомышечной ткани). В лимфоидной ткани отсутствуют герминативные центры, но есть плазматические клетки.
Клиническая картина. Первые проявления возникают в младенческом и раннем детском возрасте. Характерны повторные инфекции различной локализации (в первую очередь респираторного тракта), в том числе оппортунистические (вызванные Pneumocystis carinii). Также характерны поражения вирусами (цитомегаловирус и аденовирусы), Criptococcus neoformans, микоплазмами и микобактериями. Криптоспоридиальная инфекция может быть причиной острой и хронической диареи (развивающейся у 50% больных) и склерозирующего холангита. Часто развиваются анемии, нейтропении, изъязвление слизистой полости рта, гингивит, язвенные
поражения пищевода, различных отделов кишечника, неспецифический язвенный колит. Выявляют предрасположенность к аутоиммунным расстройствам (серонегативный артрит, гломерулонефрит и др.) и злокачественным новообразованиям (преимущественно лимфоидной ткани, печени и билиарного тракта). Могут развиваться лимфаденопатия, гепато- и спленомегалия. Лечение
Регулярная заместительная терапия внутривенным иммуноглобулином.
Противобактериальная химиотерапия. Для профилактики и лечения пневмоцистных пневмоний применяют ко-тримоксазол [сульфаметоксазол+триметоприм] и пентамидин.
Для предупреждения поражения печени и билиарного тракта следует употреблять только кипяченую или фильтрованную воду, проводить регулярное обследование (ультразвуковое исследование, биопсию печени по показаниям).
При лечении нейтропении и изъязвлений полости рта применяют глюкокортикоиды и препараты гранулоцитарного колониестимулирующего фактора.
При развитии аутоиммунных осложнений назначают иммуносупрессивную терапию (глюкокортикоиды, азатиоприн, циклоспорин А), а также препараты на основе моноклональных антител.
Оптимальный метод лечения - трансплантация костного мозга от HLA-совместимых доноров (уровень выживания 68%, лучше проводить в возрасте до 8 лет).
КОМБИНИРОВАННЫЕ ИММУНОДЕФИЦИТЫ С ПРЕИМУЩЕСТВЕННЫМ ДЕФЕКТОМ Т-ЛИМФОЦИТОВ
Тяжёлая комбинированная иммунная недостаточность
ТКИН (SCID - Severe Combined Immune Deficiency) - группа синдромов, характеризующихся снижением уровня Т-лимфоцитов или полным их отсутствием и нарушением адаптивного иммунитета. . Ретикулярная дисгенезия, характеризующаяся нарушением созревания лимфоидных и миелоидных предшественников на ранних этапах: нейтропения и T - B - NK - .
. X-сцепленная ТКИН, развивающаяся в результате мутации гена IL-2RG [(CD132, общая у -цепь рецептора для ИЛ-2, ИЛ-4, ИЛ-7, ИЛ-9, ИЛ-15 и ИЛ-21), Xq13.1-q21.1, אּ], что приводит к блокаде рецепторов и неспособности клеток-мишеней ответить на действие соответствующих интерлейкинов (более 50% всех случаев ТКИН); T - B + NK - .
. Недостаточность тирозинкиназы Janus3 [ген JAK3 (19p13.1), ρ]; при дефектах гена нарушается передача активационного сигнала от общей у -цепи ИЛ-2, ИЛ-4, ИЛ-7, ИЛ-9, ИЛ-15, ИЛ-21 к ядру клетки, что приводит к нарушению дифференцировки Т- и NK-клеток; T - B+NK - .
. Недостаточность протеинтирозинфосфатазы (CD45, ген PTPRC, 1q31-q32); при дефекте гена происходит усиление ингибирующей активности киназы Csk на протеинтирозинкиназу Src с нарушением фосфорилирования ITAM-доменов TCR и BCR; T - B+NK+.
. Полный дефицит ферментов RAG1 и RAG2, активирующих рекомбинацию V(D)J-сегментов иммуноглобулинов и TCR [гены RAG1 и RAG2 (11р13), ρ]; T - B - NK + .
. Синдром Оменна (неполный дефицит ферментов RAG1 и
RAG2) [гены RAG1 и/или RAG2 (11p13-p12), р]. Благодаря
невысокой остаточной активности этих ферментов всё же развивается некоторое количество клонов T-лимфоцитов, специфичных к антигенам эпителиальных тканей кожи и пищеварительного тракта, где они и размножаются и продуцируют большие количества ИЛ-4 и ИЛ-5, вызывая гиперэозинофилию и образование IgE остаточными B-лимфоцитами (при отсутствии иммуноглобулинов других классов). Характерна эритродермия и пахидермия с алопецией в области скальпа и бровей, изнуряющая диарея, угрожающий жизни инфекционный синдром; гепатоспленомегалия и гиперплазия лимфатических узлов.
. ТКИН с повышенной чувствительностью к ионизирующей радиации. Дефект ядерного белка Artemis [ген DCLRE1C, (10p), р], входящего в комплекс ферментов, необходимых для репарации ДНК (участвует в соединении двухцепочечных разрывов), при мутации гена происходит нарушение V(D)J-рекомбинации; T - B - NK + .
. Дефицит ИЛ-2 [ген IL-2, 4q26-q27].
Мутации гена а-цепи рецептора ИЛ-2 (CD25) (10р15-р14); T - B + NK + .
Мутации гена а-цепи рецептора ИЛ-7 (CD127) (5р13); T - B + NK + .
Дефицит ТАР (Transporter for Antigen Presentation), необходимого для транспорта антигенных пептидов в эндоплазматический ретикулум гена а-цепи рецептора ИЛ-7 (CD127) (5р13); T - B + NK + .
Мутации генов цепей CD3 (CD3γ, CDδ и CDε), приводящие к снижению количества зрелых Т-лимфоцитов, нарушению их дифференцировки; T - B + NK + .
Недостаточность протеинтирозинкиназы ZAP-70 [ген ZAP-70 (2q12), р]. При мутации гена страдает фосфорилирование доменов ITAM ζ-цепи TCR и ITAM-содержащих рецепторов NK-клеток, развивается селективный дефицит CD8 + Т-клеток (содержание CD4 + Т-лимфоцитов в норме, но выражены функциональные нарушения в виде отсутствия образования этими клетками ИЛ-2 и пролиферации).
Недостаточность аденозиндезаминазы [ген ada (20q12-q13.11 , р)], приводящая к накоплению в клетках метаболитов (дезоксиаденозинтрифосфата и S-аденозилгомоцистеина), ингибирующих пролиферацию Т- и В-лимфоцитов (описаны варианты с поздним дебютом заболевания); T - B - NK - .
Недостаточность пуриннуклеозидфосфорилазы [ген pnp (14q11.2), р], приводящая к накоплению в клетках дезоксигуанозинтрифосфата, ингибирующего пролиферацию Т-лимфоцитов (сопутствующие синдромы - урикемия и урикурия); T - B + NK - .
Данные лабораторных исследований. Выявляют вариабельную, иногда глубокую лимфопению; лимфоциты неспособны пролиферировать в ответ на специфический антиген; часто выражено снижение уровня иммуноглобулинов в сыворотке крови. На рентгенограмме грудной клетки отсутствует тень тимуса.
Клиническая картина. Обычно клинический диагноз становится ясен в первые 6 мес жизни, когда исчезают материнские IgG антитела. В клинической картине на первый план выходят тяжёлый инфекционный синдром, гипоплазия лимфоидной ткани и отставание в развитии. Инфекционный синдром характеризуется оральным кандидозом, хронической диареей, пневмонией, лихорадкой,
сепсисом бактериальной этиологии, вирусными инфекциями. Возбудители инфекций принадлежат к разным таксономическим группам: бактерии, вирусы, грибки, условно-патогенные микроорганизмы (Pneumocystis carinii). Пневмония часто бывает вызвана P. carinii, диарея - ротавирусами, Campylobacter, Giardia lamblia. Нередко манифестирует вирусный гепатит. Характерно развитие регионарного или генерализованного БЦЖита после вакцинации.
Лечение предусматривает назначение поддерживающей терапии, включающей парентеральное питание, введение внутривенного иммуноглобулина, назначение антибиотиков, противогрибковых и противовирусных препаратов. Один из основных методов лечения, позволяющих достичь выздоровления - трансплантация костного мозга, без которой дети с ТКИН, как правило, умирают на 1-м году жизни. Описаны единичные случаи, когда ребёнок в особо санированных условиях доживал до 2-3 лет. Важно как можно раньше распознать ТКИН у новорождённых, так как для них фатальна, например, иммунизация живыми вакцинами. Сразу после постановки диагноза таких детей нужно поместить в гнотобиологические условия (стерильный бокс). В случае присоединения инфекционных заболеваний проводят интенсивную противобактриальную, противовирусную и противогрибковую терапию, заместительную терапию внутривенным иммуноглобулином. Для профилактики пневмоцисных пневмоний назначают ко-тримоксазол. В случае развития БЦЖита необходимо проведение длительной интенсивной противотуберкулёзной терапии. Для переливания компонентов крови надо использовать только облучённые и отфильтрованные препараты. Есть риск развития посттрансфузионной реакции «трансплантат против хозяина» в связи с трансплацентарной передачей материнских лимфоцитов.
Синдром «голых лимфоцитов»
Так называют патологию, когда в организме не экспрессируются молекулы MHC-I или МНС-II. В отсутствие экспрессии молекул MHC-I снижено содержание CD8 + Т-лимфоцитов и отсутствует активность NK-клеток; при отсутствии МНС-II снижен уровень CD4 + T-лимфоцитов. Охарактеризовано несколько генетических дефектов. Однако эти дефекты локализованы не в генах MHC, а в нескольких разных факторах, ответственных за регуляцию их
экспрессии. Клиническая картина синдрома «голых» лимфоцитов и лечение аналогичны таковым при остальных ТКИН.
Синдром ДиДжорджи
При синдроме ДиДжорджи, или синдроме дефекта третьего и четвёртого глоточных карманов [делеции в 22q11, в том числе гена TBX1 (22q11.2), выявляют гипоплазию или аплазию тимуса, гипоплазию паращитовидной железы, пороки сердца, дефицит T-лимфоцитов, вариабельные количества B-лимфоцитов.
Данные лабораторных исследований. Значительное уменьшение количества CD3+, CD4+ и CD8+ Т-клеток и резкое снижение их пролиферативной активности, индуцированной митогенами и антигенами. Количество B- и NK-клеток в норме. Концентрации сывороточных иммуноглобулинов в большинстве случаев в пределах нормы, возможны различные варианты дисгаммаглобулинемии.
Клиническая картина. Иммунодефицитный компонент представлен гипоплазией или аплазией тимуса и рекуррентными, тяжело протекающими инфекционными заболеваниями. Выявляют также гипопаратиреоидизм (гипокальциемию и, как следствие, - тетанию, заметную на 1-2-й дни после рождения); пороки кровеносной системы (правый разворот дуги аорты, стеноз правого желудочка, дефекты в межжелудочковой и межпредсердной перегородках, тетрада Фалло, атрезия или гипоплазия лёгочной артерии); впадину нёба; аномалии лицевого скелета (увеличенное расстояние между парными органами, челюсти уменьшенного размера, особенно нижняя, низко посаженные ушные раковины, короткий подносовой желобок). Выражены аномалии строения гортани, глотки, трахеи, внутреннего уха, пищевода; нарушение развития почек, ЦНС и другие пороки развития (полидактилия, отсутствие ногтей, атрезия ануса, анальные фистулы). Характерна задержка речевого и психомоторного развития. Отмечают предрасположенность к аутоиммунным расстройствам (цитопения, аутоиммунный тиреоидит) и злокачественным новообразованиям.
Лечение. . Антибактериальная и противовирусная терапия. . Заместительная терапия препаратами внутривенного иммуноглобулина. . Хирургическое лечение с целью коррекции пороков развития. . При аутоиммунных осложнениях - иммуносупрессивная терапия. . При наличии эндокринопатий - коррекция соответствующих нарушений. . Трансплантация костного мозга неэффек-
тивна. . Оправдана трансплантация эпителиальной ткани тимуса. Коррекция функции паращитовидных желёз.
X-сцепленный лимфопролиферативный синдром
Х-сцепленный лимфопролиферативный синдром характеризуется нарушением иммунного ответа на вирус Эпштейна-Барр [обусловлен дефектами гена SH2D1A (SAP) в Xq25, אּ], приводящим к неконтролируемой пролиферации В-лимфоцитов, трансформированных вирусом Эпштейна-Барр, и заражению вирусом новых клеток-мишеней.
Клиническая картина. Описано 4 наиболее распространённых фенотипа: тяжёлый инфекционный мононуклеоз, злокачественные лимфопролиферативные состояния (лимфомы, лейкозы, преимущественно В-клеточные), анемия или панцитопения (в том числе и вследствие вирус-индуцированного гемофагоцитарного синдрома), дисгаммаглобулинемия. Инфицирование вирусом Эпштейна-Барр - триггерный (пусковой) механизм формирования наиболее тяжёлых, быстропрогрессирующих и фатальных заболеваний: фульминантный инфекционный мононуклеоз (в 58% случаев приводит к летальному исходу), гемофагоцитарный синдром (без лечения в 100% случаев приводит к летальному исходу). В 10% случаев фенотип проявляется до инфицирования вирусом Эпштейна-Барр (при этом, как правило, развиваются дисгаммаглобулинемия и лимфомы). Наиболее часто выявляют различные виды гипогаммаглобулинемий. Иммунодефицит приводит к развитию бактериальных, грибковых и вирусных инфекционных заболеваний. Предположить заболевание можно у мальчиков с характерным семейным анамнезом и сероили ПЦР-позитивным тестом на вирус Эпштейна-Барр. Для диагностики рекомендуется использовать сочетание генетического анализа SH2D1A и оценки уровня экспрессии SAP.
Лечение
С целью профилактики рекомендуется использовать противовирусные препараты - ацикловир, валацикловир (их раннее назначение подавляет репликацию вируса Эпштейна-Барр в ротоглотке) и внутривенный иммуноглобулин (с высоким титром антител к вирусу Эпштейна-Барр).
При гипогаммаглобулинемиях применяют внутривенный иммуноглобулин ежемесячно в сочетании с антибактериальной терапией.
Для лечения фульминантного инфекционного мононуклеоза назначают высокие дозы ацикловира и метилпреднизолона, высокодозовая терапия внутривенным иммуноглобулином с высоким титром антител к вирусу Эпштейна-Барр и ИФНа.
При развитии гемофагоцитарного синдрома сочетают высокие дозы дексаметазона с вепезидом ♠ (этопозид).
При лечении злокачественных заболеваний используют стандартные протоколы терапии.
Радикальный метод лечения - трансплантация костного мозга от HLA-совместимых доноров.
Аутоиммунный лимфопролиферативный синдром
Аутоиммунный лимфопролиферативный синдром - группа заболеваний, характеризующихся доброкачественной лимфопролиферацией, гипериммуноглобулинемией, аутоиммунными нарушениями, повышенным содержанием CD3 + CD4 - CD8 - Т-лимфоцитов (двойных негативных) в периферической крови и дефектом апоптоза [дефект гена Fas (CD95) - TNFRSF6 (10q24.1), гена каспазы-10, Fas-лиганда - FasL (1q23)].
Данные лабораторных исследований. Содержание CD3 + CD4 - CD8 - Т-лимфоцитов в периферической крови или в лимфоидных тканях составляет больше 1%. Уровень IgG, IgA и IgM может быть нормальным, повышенным или даже сниженным. С возрастом гипергаммаглобулинемия сменяется низкой концентрацией сывороточных иммуноглобулинов, вплоть до агаммаглобулинемии. Выявляют аутоантитела к эритроцитам, тромбоцитам, нейтрофилам, гладким мышцам, к фактору VIII; антинуклеарные и антифосфолипидные аутоантитела, а также ревматоидный фактор и др. Характерен лимфоцитоз.
Клиническая картина. У всех больных увеличены печень, лимфатические узлы (в первые 5 лет жизни) и селезёнка. Лимфопролиферация не сопровождается повышением температуры и ночным потоотделением. Дебют аутоиммунных реакций может не совпадать с лимфопролиферацией и наступает позже. С возрастом тяжесть аутоиммунных реакций нарастает. Чаще развиваются аутоиммунные реакции против клеток крови (гемолитическая анемия, тромбоцитопения, нейтропения), реже затрагиваются другие органы. Повышен риск развития злокачественных новообразований (Т- и В-лимфомы, лимфома Беркитта, атипичная лимфома, лимфогранулёматоз и др.).
Лечение. . Химиотерапевтические средства (циклофосфамид, азатиоприн, метотрексат, хлорамбуцил). . Глюкокортикоиды. . Спленэктомия при выраженном гиперспленизме и гемоцитопении. . В тяжёлых случаях возможна трансплантация костного мозга.
Синдром гипериммуноглобулинемии Е
Гипер-IgЕ-синдром характеризуется существенным повышением уровня сывороточного IgE, повторными абсцессами кожи и подкожной клетчатки стафилококковой этиологии, пневмонией с формированием пневмоцеле, аномалиями строения лицевого скелета, АтД. Молекулярно-генетическая природа гипер-IgЕ-синдрома до сих пор не установлена. В некоторых случаях выявлено аутосомнодоминантное, в других - аутосомно-рецессивное наследование. Предполагают, что дефекты затрагивают сигнальные молекулы цитокиновых рецепторов (в аутосомно-доминантной форме этого синдрома уже выявлены мутации в Stat3) и, возможно, связаны с нарушением функционирования субпопуляции Th17-клеток. Другой ген, ответственный за формирование гипер-IgЕ-синдрома, локализован на хромосоме 4 (4q).
Данные лабораторных исследований. Выявляют разнообразные иммунологические нарушения: повышение уровня IgE в сыворотке, нарушение хемотаксиса нейтрофилов, дефект образования антител; снижение реакции ГЗТ на кандидин, дифтерийный и столбнячный анатоксины; ослабление пролиферативной активности Т-клеток в ответ на Candida и столбнячный анатоксин при сохранении ответа на митогены. Эозинофилия в периферической крови и жидкости кожных абсцессов. Количество Т- и В-клеток в норме.
Клиническая картина. Экзема среднетяжелого течения в раннем возрасте. Характерные черты лица (широкая переносица, широкий курносый нос, асимметрия лицевого скелета, выступающий лоб, глубоко посаженные глаза, высокое нёбо). Выявляют аномалии развития скелета, сколиоз, повышенную подвижность суставов, склонность к переломам костей после незначительных травм, нарушение смены зубов. Возникают абсцессы кожи, подкожной клетчатки и лимфатических узлов. Пневмония развивается в более старшем возрасте (наиболее частые возбудители S. aureus и H. in-
fluenzae), в 77% случаев формируется пневмоцеле, присоединяется инфекция, обусловленная P. aeruginosa и A. fumigatus. Пневмония может протекать без повышения температуры. Хронический кандидоз слизистых оболочек и ногтей развивается в 83% случаев.
Лечение. . Длительная (с целью профилактики - пожизненная) антибактериальная и противогрибковая терапия. . Для лечения дерматита применяют топические средства, в тяжёлых случаях - низкие дозы циклоспорина А. . Трансплантация костного мозга неэффективна.
СИНДРОМЫ ПОЛОМОК ХРОМОСОМ
Для синдромов с хромосомной нестабильностью: атаксиятелеангиэктазия [дефект гена ДНК-топоизомеразы АТМ (11q22), р] и синдром Ниймеген [дефект гена нибрина NBS1 (8q21)] - характерны повышенная частота злокачественных опухолей, спонтанная хромосомная нестабильность и хромосомные поломки. Оба белка участвуют в репарации двунитевых разрывов ДНК и регуляции клеточного цикла. В норме двунитевые разрывы ДНК происходят в процессе V(D)J рекомбинации генов иммуноглобулинов и TCR, переключении классов иммуноглобулинов, во время кроссинговера и при мейозе. Аналогичные процессы происходят при созревании нейронов головного мозга. Дефекты репарации ДНК при атаксии-телеангиэктазии и синдрома Ниймеген обусловливают такие клинические проявления, как нарушения синтеза иммуноглобулинов, функции половых органов и нервной системы.
Атаксия-телеангиэктазия
Этот синдром (частота 1:300 тыс. новорождённых) с весьма гетерогенным фенотипом описала французский врач Д. Луи-Бар. Симптомы атаксии можно обнаружить у ребёнка уже в возрасте 2-4 мес. Атаксия обусловлена прогрессирующей дегенерацией клеток Пуркинье в мозжечке. Телеангиэктазии на коже носа, ушных раковин, на конъюнктиве появляются несколько позже, к 3-6 годам. Часто на коже возникают пятна типа «кофе с молоком». Характерны гипоплазия тимуса, лимфатических узлов, селезёнки, миндалин. Иммунодефицит проявляется снижением (нередко дисбалансом) выработки IgA, IgE, IgG2, IgG4. У 80% больных развива-
ется соответствующая инфекционная клиническая симптоматика. Снижены количество и функциональная активность Т-клеток (в основном CD4 + Т-клеток). Общее число T-лимфоцитов у большинства пациентов нормальное. Необычайно высока (в 200 раз выше, чем в общей популяции) частота новообразований (преимущественно лимфомы и карциномы), нередко приводящих к летальному исходу к 10-12 годам. Лечение симптоматическое.
Синдром Ниймеген
Синдром Ниймеген (по названию города в Голландии, где впервые описано заболевание) проявляется микроцефалией, специфическими нарушениями лицевого скелета (скошенный лоб, выступающая средняя часть лица, длинный нос, гипоплазия нижней челюсти, монголоидный разрез глаз, эпикант, большие уши), отставанием физического развития, наличием пятен «кофе с молоком» на коже; клинодактилией и синдактилией, дисгенезией яичников и др. Большинство детей страдают от рецидивирующих и хронических бактериальных инфекционных заболеваний дыхательных путей, ЛОР-органов и мочевыводящей системы. В 50% случаев развиваются злокачественные новообразования, преимущественно В-клеточные лимфомы. Выявляют различные формы дисгаммаглобулинемии, снижение CD4 + Т-клеток.
Лечение. . Симптоматическая терапия неврологических расстройств. . Заместительная терапия внутривенным иммуноглобулином. . По показаниям применяют антибактериальную, противовирусную, противогрибковую терапию. . При лечении злокачественных новообразований учитывают повышенную чувствительность к радиации и химиопрепаратам.
Синдром Вискотта-Олдрича
Синдром Вискотта-Олдрича [дефект гена WASP (Xp11.23p11.22), אּ; также ρ и Ʀ] Ген WASP (от Wiskott-Aldrich syndrome) экспрессируется в лимфоцитах, ткани селезёнки и тимоцитах. Мутации этого гена ассоциированы с аномальной экспрессией в нейтрофилах и T-лимфоцитах (CD4 и CD8) молекулы CD43 (лиганд для ICAM-1, выполняет антиадгезивную функцию).
Данные лабораторных исследований. Тромбоцитопения (менее 10% от нормы) обусловлена повышенным разрушением клеток.
Тромбоциты меньшего размера, чем у здоровых людей. Уровень IgM в сыворотке крови снижен при нормальном уровне IgG и повышении содержания IgA и IgE. Снижены титры изогемагглютининов, нарушено образование антител к полисахаридным антигенам пневмококка, стрептококка, кишечной палочки, сальмонеллы, а также противовирусных антител. В раннем возрасте, как правило, количество лимфоцитов нормальное, после 6 лет выявляют лимфопению (менее 1х10 9 /л), снижение CD3 + и CD4 + Т-клеток при нормальном уровне В- и NK-клеток. Возможны эозинофилия и развитие постгеморрагической анемии. Снижается пролиферативный ответ Т-клеток на митогены и антигены, ослабляется ГЗТ. В селезёнке нормальные структуры герминативных центров и Т-клеточные зоны не выявляются.
Клиническая картина. Заболевание характеризуется триадой признаков: тромбоцитопенией, экземой и рекуррентными инфекционными заболеваниями. Геморрагический синдром проявляется рано, уже в период новорождённости (петехиальная сыпь, кефалогематомы, кровотечения из пупочной ранки, кишечные кровотечения). Экзема проявляется с раннего возраста у 80% больных. С возрастом нарастают признаки иммунодефицита: бактериальные инфекционные заболевания ЛОР-органов, дыхательной системы, органов пищеварения, кожи; распространённая или генерализованная герпетическая инфекция (Herpes simplex и Varicella zoster), цитомегаловирусные, а также грибковые (кандидоз слизистых оболочек), реже оппортунистические инфекционные заболевания. У 70% больных выявляют аутоиммунные заболевания (гемолитическая анемия, нейтропения, артрит, кожный васкулит, неспецифический язвенный колит, церебральный васкулит, гломерулонефрит, аутоиммунная тромбоцитопения). У больных старше 5 лет повышена частота злокачественных новообразований (преимущественно опухоли лимфоидной ткани).
Лечение. . Трансплантация аллогенного костного мозга или стволовых клеток (успешность операции достигает 90% при использовании трансплантата от гистосовместимого донора и 50% - при гаплоидентичной трансплантации). . Заместительная терапия внутривенным иммуноглобулином. . Профилактическое назначение антибактериальных, противогрибковых и противовирусных препаратов. . Для уменьшения геморрагического синдрома проводят спленэктомию. . При аутоиммунных осложнениях назначают иммуносупрессивную терапию.
ДЕФЕКТЫ ФАГОЦИТОЗА
Хроническая гранулёматозная болезнь
Хроническая гранулёматозная болезнь характеризуется нарушением функциональной активности фагоцитов (образования активных форм кислородных радикалов, внутриклеточного киллинга и фрагментации фагоцитированных патогенов), постоянными бактериальными и грибковыми инфекционными заболеваниями и развитием гранулёматозного воспаления. Развивается хроническая гранулёматозная болезнь у лиц с различными генетическими дефектами [в 65% случаев - Х-сцепленный вариант заболевания: ген gp91-phox (Xp21.1), אּ; в 35% случаев - аутосомно-рецессивный: ген f47-phox (7q11.23), ρ; ген p67-phox (1q25), ρ; ген p22-phox (16q24), р], приводящими к нарушениям в системе НАДФ-оксидазы. При гибели короткоживущих (несколько часов) нейтрофилов неубитые бактерии «вытекают» в очаг воспаления. Макрофаги - долгоживущие клетки, и их предшественники (моноциты) мигрируют в очаг в повышенных количествах (что приводит к формированию гранулёмы), фагоцитируют микроорганизмы, но не способны их убить.
Данные лабораторных исследований. Характерны нормальные значения сывороточных иммуноглобулинов и субпопуляций лимфоцитов. Образование перекисных радикалов нейтрофилами, оцениваемое в тестах (люминолзависимой хемилюминесценции или восстановления тетразолиевого синего), резко снижено или отсутствует. На фоне инфекционных заболеваний характерны лейкоцитоз, нейтрофилёз, повышение СОЭ, анемия, гипергаммаглобулинемия.
Клиническая картина. Заболевание в большинстве случаев проявляется на первом году жизни инфекционным синдромом (инфекции внутри- и внеклеточными патогенами) и образованием гранулём. Наиболее типичны: поражение лёгких (рецидивирующие пневмонии, поражение прикорневых лимфатических узлов, абсцессы лёгких, гнойные плевриты), пищеварительного тракта, кожные абсцессы и лимфадениты. Наиболее частые возбудители - каталаза-позитивные микроорганизмы: S. aureus, Aspergillus spp., кишечные грамотрицательные бактерии (E. coli, Salmonella spp., Serratia marcescens), реже - Burkholderia cepacia и Nocardia farcinica. Характерно развитие печёночных и поддиафрагмальных абсцессов, остеомиелитов, параректальных абсцессов, сепсиса.
Самое тяжёлое, жизнеугрожающее инфекционное осложнение - аспергиллёз, который может протекать в виде диффузного поражения лёгких и других органов (жировой клетчатки, головного мозга, костей, суставов, эндокарда). У больных хронической гранулёматозной болезнью после вакцинации БЦЖ часто развивается вакциноассоциированная инфекция, вовлекающая регионарные лимфатические узлы. Микобактериальное поражение у больных хронической гранулёматозной болезнью может иметь как лёгочную, так и внелёгочную локализацию и носит затяжное течение. Для больных хронической гранулёматозной болезнью характерно отставание в физическом развитии.
Лечение. . Противомикробная терапия: профилактическое постоянное использование ко-тримоксазола и противогрибковых препаратов (итраконазола и др.); при возникновении инфекционных осложнений парентерально проводится комбинированная антибактериальная терапия (2-3 бактерицидных антибиотика, проникающих внутриклеточно) в сочетании с противогрибковой терапией. При развитии аспергиллёза показано длительное применение амфотерицина В или каспофунгина. При микобактериальной инфекции применяют сочетание длительной специфической терапии противотуберкулёзными препаратами с антибиотиками широкого спектра действия. . Хирургическое лечение часто сопровождается нагноением послеоперационной раны и формированием новых очагов. Возможно пункционное дренирование абсцесса под контролем ультразвука. . Для лечения тяжёлых инфекционных осложнений при неэффективности антибактериальной терапии возможно использование гранулоцитарной массы, высоких доз ИФНу и G-CSF. . Трансплантация костного мозга или трансплантация клеток пуповинной крови от совместимого сиблинга может быть успешной в раннем возрасте, когда минимален риск смерти от инфекционных осложнений и реакции «трансплантат против хозяина».
Дефекты адгезии лейкоцитов
На сегодняшний день описано 3 дефекта адгезии лейкоцитов . Все они имеют
аутосомно-рецессивный тип наследования, характеризуются повторными и хроническими бактериальными и грибковыми инфекционными заболеваниями. Для I типа характерно отсутствие или снижение экспрессии CD11/CD18 на лейкоцитах, нарушение хемотаксиса нейтрофилов, лейкоцитоз (более 25х10 9), позднее отпадание пуповинного остатка и развитие омфалита, плохое заживление ран, отсутствие формирования гноя в месте проникновения патогена в организм.
Лечение. . Антибактериальная терапия: инфекционных эпизодов и профилактическая. . При тяжёлом течении назначают трансплантацию костного мозга от HLA-совместимого донора.
ДЕФЕКТЫ СИСТЕМЫ КОМПЛЕМЕНТА
Болезни с дефицитом компонентов комплемента
Проявления генных дефектов отдельных компонентов системы комплемента приведены в табл. 11-2.
Наследственный АО. Болезни, обусловленные дефицитом компонентов комплемента, выявляют редко, поскольку для их манифестации необходимо гомозиготное состояние по аутосомным аллелям. Есть единственное исключение, связанное с C1inh (ингибитор C1-эстеразы): мутация гена C1inh, приводящая к дефициту ингибитора, в гетерозиготном состоянии проявляется фенотипом, известным как наследственный АО (см. подробнее главу 13, ангиоотёки).
Болезни иммунных комплексов. Недостаточность C1-C4 проявляется развитием болезней иммунных комплексов - системных васкулитов и повреждений почек, что обобщённо называют синдромом системной красной волчанки (СКВ).
Пиогенные инфекции. Дефицит C3 (также факторов H и I) ассоциирован с повышенной восприимчивостью к пиогенным инфекциям. Дефицит компонентов, участвующих в альтернативном пути активации комплемента, а также дефицит компонентов C5-C8 ассоциированы с повышенной восприимчивостью к инфекции, вызываемой Neisseria spp. Дефицит C9 обычно клинически бессимптомен.
Таблица 11-2. Клинические проявления дефектов отдельных компонентов системы комплемента
Дефицит лектина, связывающего маннозу
Дефицит лектина, связывающего маннозу (другое название: маннансвязывающий лектин - МСЛ), обусловлен дефектом гена MBL (разные точечные мутации и делеции в гене MBL выявляют у 17% людей европеоидной расы). При дефектах гена нарушается активация протеаз, расщепляющих компоненты комплемента C2 и C4, и активация системы комплемента по лектиновому пути. Клинически эта патология проявляется инфекционным синдромом.
Данные лабораторных исследований. Анализ субпопуляций лимфоцитов, лейкоцитов, а также изотипов иммуноглобулинов не показывает существенных отклонений, адекватных клиническим симптомам. В сыворотке крови отсутствует МСЛ.
Лечение. Это заболевание не является классическим иммунодефицитом. Следовательно, иммунокоррекция иммунотропными средствами противопоказана. Рекомбинантный МСЛ можно использовать как фармакологический препарат для этиопатогенетической заместительной терапии пациентов с этим наследственным дефектом. В настоящее время этот препарат проходит клинические испытания.
Транзиторная гипогаммаглобулинемия у детей
Транзиторная гипогаммаглобулинемия у детей связана с физиологической особенностью поэтапного формирования системы иммуноглобулинов. В наибольшей степени «запаздывает» созревание IgM и IgA антителообразования. У здоровых детей содержание материнских IgG постепенно снижается и после полугода возрастает выработка собственных IgG-антител. У некоторых детей, однако, нарастание уровня иммуноглобулинов задерживается. Такие дети могут страдать рекуррентными бактериальными инфекционными заболеваниями. В этих случаях не следует прибегать к инфузиям препаратов донорских иммуноглобулинов (введению внутривенного иммуноглобулина).
Селективный дефицит иммуноглобулина A
Селективный дефицит иммуноглобулина A (SD IgA - Selective Deficiency of IgA) развивается в результате дефекта гена tnfrsf13b
или р). Дефицит IgA при наличии иммуноглобулинов других классов - самый частый иммунодефицит, выявляемый в общей популяции с частотой 1:500-1500 человек (у больных, страдающих аллергией, ещё чаще). Различают недостаточность IgA селективную, т.е. заключающуюся в дефиците одного из подклассов (30% случаев), и полную (70% случаев). Дефицит подкласса IgA2 приводит к более выраженной клинической картине, чем дефицит подкласса IgA1. Возможны и сочетания дефицита IgA с другими нарушениями: с дефектом биосинтеза IgG и с аномалиями T-лимфоцитов. Подавляющее большинство лиц с селективным
дефицитом IgA практически здоровы. Для детей моложе 2 лет дефицит IgA - физиологическое состояние.
Выявляют снижение концентрации сывороточного IgA до <5 мг/дл у детей старше 4 лет; IgG и IgM в норме, количество и соотношение субпопуляций лимфоцитов и их функциональная активность могут быть в норме.
Клиническая картина. При дефиците IgA могут развиваться 3 группы патологических синдромов: инфекционный, аутоиммунный и аллергический. Пациенты с дефицитом IgA предрасположены к рецидивирующим инфекционным заболеваниям верхних дыхательных путей и органов пищеварения. Наиболее частыми и тяжело протекающими являются разнообразные аутоиммунные заболевания (ревматоидный артрит, анкилозирующий спондилит, синдром Шегрена, васкулит с поражением сосудов мозга, аутоиммунный тиреоидит, СКВ, гломерулонефрит, гемолитическая анемия, сахарный диабет I типа, витилиго и др.). Частота встречаемости целиакии превышает таковую у детей с нормальным IgA в 10 раз. Наиболее часто выявляемые аллергические проявления: непереносимость белка коровьего молока, атопический дерматит (АтД), бронхиальная астма.
Лечение. Случаи бессимптомного течения не требуют никакого специального лечения; при наличии клинических проявлений инфекционных, аутоиммунных и аллергических заболеваний проводят лечение в соответствии со стандартами.
Заместительная терапия донорскими иммуноглобулинами не показана ни при селективном, ни при полном дефиците IgA, поскольку высока вероятность образования у реципиента антиизотипических антител к IgA и развития обусловленных ими трансфузионных осложнений.
Агаммаглобулинемия с дефицитом В-клеток
X-сцепленная агаммаглобулинемия (болезнь Брутона) составляет 90% всех случаев агаммаглобулинемии. Болеют мальчики, сыновья (אּ, ρ) носительниц дефектного гена btk (Xq21.3-q22), кодирующего специфичную для B-лимфоцитов протеинтирозинкиназу Btk (Bruton"s tyrosine kinase - тирозинкиназа Брутона). В результате дефекта происходит нарушение внутриклеточных сигнальных путей, рекомбинация тяжёлых цепей иммуноглобулинов, диффе-
ренцировка пре B-клеток в B-лимфоциты. У 10% больных агаммаглобулинемия с дефицитом В-клеток наследуется аутосомнорецессивно. В настоящее время описано 6 генетических дефектов, включая молекулы пре-В-клеточного рецептора, цитоплазматического адапторного протеина В-клеток (BLNK) и гена Leucine-Rich Repeat-Containing 8 (LRRC8).
Данные лабораторных исследований. Отсутствуют периферические B-лимфоциты. В костном мозге присутствуют пре-B-клетки с μ-цепью в цитоплазме. Число T-лимфоцитов и функциональные тесты на T-лимфоциты могут быть норме. IgM и IgA в крови выявить не удаётся; IgG может присутствовать, но в малых количествах (0,4-1,0 г/л). Нет антител к антигенам групп крови и к вакцинным антигенам (столбнячному, дифтерийному токсинам и др.). Может развиваться нейтропения. Гистологическое исследование лимфоидной ткани: в лимфоидных фолликулах нет герминативных (зародышевых) центров и плазматических клеток.
Клиническая картина. Если семейный анамнез неизвестен, то диагноз становится очевидным в среднем к возрасту 3,5 лет. Для заболевания характерны гипоплазия лимфоидной ткани, тяжело протекающие гнойные инфекции, инфекционные заболевания верхних (синуситы, отиты) и нижних (бронхиты, пневмонии) дыхательных путей; возможны гастроэнтериты, пиодермии, септические артриты (бактериальные или хламидиозные), септицемия, менингит, энцефалит, остеомиелит. В качестве возбудителей заболеваний дыхательных путей чаще всего выступают Haemophilus influenzae, Streptococcus pneumoniae, Staphylococcus aureus, диареи кишечные бактерии или лямблии Giardia lamblia. Также пациенты с агаммаглобулинемией подвержены инфекционным заболеваниям, вызванным микоплазмами и уреаплазмами, являющимися причиной развития хронических пневмоний, гнойных артритов, циститов и абсцессов подкожной клетчатки. Из вирусов типичны нейротропные вирусы ECHO-19 и коксаки, вызывающие как тяжёлые острые, так и хронические энцефалиты и энцефаломиелиты. Проявлениями энтеровирусных инфекций могут быть дерматомиозитоподобный синдром, атаксия, головные боли, нарушения поведения. У больных детей при иммунизации живой полиовакциной, как правило, выявляют продолжительное выделение через слизистые оболочки вируса полиомиелита, причём с восстановленной и нарастающей вирулентностью (т.е. в детском коллекти-
ве реальна опасность заражения здоровых детей полиомиелитом в результате контакта с вакцинированным иммунодефицитным ребёнком). Аутоиммунные нарушения при агаммаглобулинемии могут быть представлены ревматоидным артритом, склеродермоподобным синдромом, склередемой, неспецифическим язвенным колитом, сахарным диабетом I типа (обусловлены преобладанием Th1 иммунного ответа).
Физикальный осмотр. Обращают внимание на отставание в физическом развитии, на форму пальцев (пальцы в виде барабанных палочек), изменения формы грудной клетки, характерные для заболеваний нижних дыхательных путей, гипоплазию лимфатических узлов и миндалин.
Лечение.
Заместительная терапия: препараты внутривенного иммуноглобулина вводят каждые 3-4 нед пожизненно. Дозы иммуноглобулинов подбирают так, чтобы создать в сыворотке больного их концентрацию, перекрывающую нижнюю границу возрастной нормы.
Обсуждают возможность генной терапии - ген Btk клонирован, однако его гиперэкспрессия ассоциирована со злокачественной трансформацией кроветворной ткани.
В случае упорной нейтропении применяют ростовые факторы. При появлении признаков аутоиммунной патологии возможно назначение препаратов моноклональных антител (инфликсимаб и др.).
Общая вариабельная иммунная недостаточность
Общая вариабельная иммунная недостаточность (ОВИН) - группа синдромов, характеризующихся дефектом синтеза антител и клеточного иммунитета. Достоверный диагностический критерий ОВИН - значительное снижение содержания иммуноглобулинов двух или трёх основных изотипов у лиц обоего пола в сочетании с одним из нижеперечисленных признаков:
Дебютом заболевания в возрасте старше 2 лет;
Отсутствием изогемагглютининов и/или низким ответом на вакцинацию;
Исключении других причин агаммаглобулинемии.
У некоторых больных причина развития ОВИН - мутации генов, кодирующих молекулы, вовлечённые в процессы созревания и выживания В-клеток: BAFF-R (B-cell Activating Factor Receptor), Blimp-1 (B-lymphocyte induced maturation protein-1) и ICOS (Inducible costimulator). Происходит нарушение способности B-лимфоцитов дифференцироваться в плазматические клетки, развиваются дефекты антителообразования, возможна дисфункция T-лимфоцитов, наблюдается повышенная склонность к инфекционным заболеваниям. Синдром может проявляться в раннем детстве, в подростковом возрасте или у молодых людей.
Данные лабораторных исследований. Существенно снижены уровни IgG и IgA (примерно у 50% больных) и IgM (вплоть до невыявляемых количеств). Число B-лимфоцитов в крови соответствует норме или снижено. Число T-лимфоцитов у большинства больных в норме. У тяжёлых больных возможно развитие лимфопении (менее 1500x103 клеток в 1 л крови). Число NK-клеток снижено. Выработка специфических антител в ответ на иммунизацию снижена или отсутствует. Пролиферация лимфоцитов и образование ИЛ-2 под действием митогенов и антигенов значительно нарушены.
Клиническая картина. Выявляют рекуррентные бактериальные инфекционные заболевания с локализацией преимущественно в дыхательных путях и околоносовых пазухах. К моменту постановки диагноза инфекции дыхательных путей могут прогрессировать до бронхоэктазов и разлитых поражений лёгочной ткани. Возможно инфекционное поражение органов пищеварения, проявляющееся диареей, стеатореей и мальабсорбцией (и соответственно потерей массы тела). Часто выявляют инфекции, вызванные Giardia lamblia, Pneumocystis carinii или вирусами семейства Herpetoviridae. Больные ОВИН склонны к развитию гнойных артритов, вызываемых микоплазмами и уреаплазмами. Проявлениями энтеровирусных инфекций могут быть энцефаломиелиты, полиемиелито- и дерматомиозитоподобный синдромы, поражения кожи и слизистых оболочек. Аутоиммунные заболевания протекают тяжело и могут определять прогноз ОВИН. Иногда первыми клиническими проявлениями ОВИН являются артрит, неспецифический язвенный колит и болезнь Крона, склерозирующий холангит, мальабсорбция, СКВ, нефрит, миозит, аутоиммунное поражение лёгких в виде лимфоидного интерстициального пневмонита, нейтропения,
тромбоцитопеническая пурпура, гемолитическая анемия, пернициозная анемия, тотальная алопеция, васкулит сетчатки, фотосенсибилизация. У больных ОВИН значительно повышена частота злокачественных новообразований (в 15% случаев), саркоидозоподобных гранулём и незлокачественной лимфопролиферации. Лечение.
Противобактериальная химиотерапия.
Заместительная терапия: препараты внутривенного иммуноглобулина вводят каждые 3-4 нед пожизненно.
При аутоиммунных осложнениях - иммуносупрессивная терапия (глюкокортикоиды, азатиоприн, циклоспорин А) и возможно назначение препаратов моноклональных антител (инфликсимаб и др.).
Гипер-IgМ-синдромы
Гипер-IgM-синдромы - довольно редкие заболевания, характеризуемые выраженным снижением или полным отсутствием IgG, IgA и нормальной или повышенной концентрацией сывороточного IgM. Это вызвано неспособностью В-лимфоцитов осуществлять переключение классов иммуноглобулинов и гипермутагенез вариабельных доменов. К настоящему времени идентифицировано 6 генетических дефектов, приводящих к развитию гипер-IgMсиндрома.
. Тип 1 (HIGM 1). Х-сцепленный дефицит CD40 лиганда (70% случаев гипер-IgM-синдромов), приводящий к неспособности Т-клеток эффективно взаимодействовать с В-лимфоцитами.
. Тип 2 (HIGM 2). Аутосомно-рецессивный, связанный с дефектом AID - индуцированной активацией цитидин дезаминазы (ген Aicda, 12р13) - фермента, участвующего в переключении классов иммуноглобулинов и гипермутагенезе.
. Тип 3 (HIGM 3). Аутосомно-рецессивный, связанный с мутацией гена молекулы CD40. При этом В-клетки сами по себе не способны эффективно взаимодействовать с Т-лимфоцитами. Фенотипические проявления сходны с таковыми для типа 1.
. Тип 4 (HIGM 4). Аутосомно-рецессивный; в некоторых случаях мутации возникают de novo. Cвязан с дефектом UNG - урацил-ДНК-гликозилазы - фермента, тоже участвующего
в переключении классов иммуноглобулинов, но уже после действия AID. В этом случае гипермутагенез не затронут и синдром протекает с меньшей тяжестью.
. Тип 5 (HIGM 5). Дефект только в переключении классов, гипермутагенез не затронут. Причинная мутация пока не выявлена, но, очевидно, дефект в ферменте, действующем после
. Тип 6 (HIGM-ED). Х-сцепленный, ассоциированный с дисгидротической эктодермальной дисплазией, вызван дефицитом NEMO (модулятора NF-kB), приводящим к нарушению передачи сигнала с CD40.
X-сцепленный гипер-IgM-синдром выявляют чаще других. Развивается при дефекте гена, кодирующего CD40L (CD154, ген расположен на Xq26-q27.2) - лиганд для CD40. Недостаточность экспрессии CD40L T-лимфоцитами приводит к невозможности переключения классов иммуноглобулинов в B-лимфоцитах с IgM на другие изотипы, а также к нарушению формирования B-клеток памяти, Т-клеточного репертуара и Th1-клеточного ответа, направленного против внутриклеточных микроорганизмов. Болеют мальчики
Данные лабораторных исследований. IgG, IgA, IgE определить не удаётся или выявляются в очень малых количествах. Уровень IgM в норме (в 50% случаев) или повышен, зачастую значительно. Количество Т- и В-клеток в норме; снижен пролиферативный ответ Т-клеток, индуцированный антигенами. IgM поликлональны, иногда моноклональны. Выявляют аутоантитела IgM изотипа (антиэритроцитарные, антитромбоцитарные, антитиреоидные, антитела к антигенам гладкомышечной ткани). В лимфоидной ткани отсутствуют герминативные центры, но есть плазматические клетки.
Клиническая картина. Первые проявления возникают в младенческом и раннем детском возрасте. Характерны повторные инфекции различной локализации (в первую очередь респираторного тракта), в том числе оппортунистические (вызванные Pneumocystis carinii). Также характерны поражения вирусами (цитомегаловирус и аденовирусы), Criptococcus neoformans, микоплазмами и микобактериями. Криптоспоридиальная инфекция может быть причиной острой и хронической диареи (развивающейся у 50% больных) и склерозирующего холангита. Часто развиваются анемии, нейтропении, изъязвление слизистой полости рта, гингивит, язвенные
поражения пищевода, различных отделов кишечника, неспецифический язвенный колит. Выявляют предрасположенность к аутоиммунным расстройствам (серонегативный артрит, гломерулонефрит и др.) и злокачественным новообразованиям (преимущественно лимфоидной ткани, печени и билиарного тракта). Могут развиваться лимфаденопатия, гепато- и спленомегалия. Лечение
Регулярная заместительная терапия внутривенным иммуноглобулином.
Противобактериальная химиотерапия. Для профилактики и лечения пневмоцистных пневмоний применяют ко-тримоксазол [сульфаметоксазол+триметоприм] и пентамидин.
Для предупреждения поражения печени и билиарного тракта следует употреблять только кипяченую или фильтрованную воду, проводить регулярное обследование (ультразвуковое исследование, биопсию печени по показаниям).
При лечении нейтропении и изъязвлений полости рта применяют глюкокортикоиды и препараты гранулоцитарного колониестимулирующего фактора.
При развитии аутоиммунных осложнений назначают иммуносупрессивную терапию (глюкокортикоиды, азатиоприн, циклоспорин А), а также препараты на основе моноклональных антител.
Оптимальный метод лечения - трансплантация костного мозга от HLA-совместимых доноров (уровень выживания 68%, лучше проводить в возрасте до 8 лет).
Это наиболее распространенный первичный иммунодефицит,
встречается с частотой 1/300 — 1/700. Впервые был …
описан J. Heremans в 1960 году.
В большинстве случаев ясной картины наследования болезни не наблюдается, в более редких случаях семейной утраты IgA аутосомно-рецессивное наследование встречается чаще, чем доминантное. Дефицит IgA иногда связан с аномалиями хромосомы 18.
IgA отличается от других иммуноглобулинов содержанием углеводов и сиаловых кислот и способностью образовывать димеры, тримеры и даже тетрамеры. Различают 2 варианта молекул IgA:
— сывороточный IgA – всегда мономер;
— секреторный IgA – формирует ди-, три- и тетрамеры, прежде чем становится составной частью секретов (слюна, слеза, молоко, секреты пищеварительного, дыхательного и мочевыделительного трактов).
В образовании секреторного IgA принимает участие особая белковая цепь – J-цепь. Следовательно, это целая система белков. Отсюда – формы патологии IgA:
— общая недостаточность IgA связана с аномалиями синтеза мономера IgA. В итоге снижено содержание и сывороточного и секреторного IgA. Нарушается и местная и общая защита;
— дефект образования секреторных молекул – SIgA. Причиной может быть отсутствие J-цепи, что ведет к нарушению местного иммунитета;
— преимущественное нарушение синтеза сывороточного IgA, когда выделяются лишь секреторные формы IgA и практически не секретируются мономеры сывороточного IgA.
Клинические симптомы зависят от степени недостаточности IgA и могут проявляться в виде патологии отдельных органов и систем. Чаще всего встречаются инфекционные поражения слизистых оболочек.
Со стороны ЖКТ – это хронический гастрит, язвенный и геморрагический колиты, илеит, стоматиты. Со стороны органов дыхания – риниты, синуситы, бронхиты, быстро принимающие хронический характер. Часто встречаются хронические бронхопневмонии с исходом в бронхоэктазы и абсцессы легких. Обнаружена также связь пониженного содержания секреторного IgA с повышенной заболеваемостью атопической аллергией и с развитием аутоиммунных заболеваний (системная красная волчанка, ревматоидный артрит, аутоиммунный тиреоидит).
У лиц с избирательным дефицитом преимущественно сывороточного мономерного IgA никаких клинических проявлений иммунодефицита чаще всего не возникает.
Лабораторные исследования: показывают, что общее количество Т- и В-лимфоцитов в периферической крови у таких больных находится в пределах нормы. Уровни сывороточного и/или секреторного IgA резко снижены, в то время как содержание IgM и IgG находится в пределах нормы. У отдельных больных (с проявлениями атопической аллергии) может быть повышен уровень IgE.
Лечение: симптоматическое. Необходимо быть осторожным при применении заместительной терапии иммуноглобулинами, так как при повторном введении есть риск возникновения анафилактического шока из-за возможности повышенной продукции анти-иммуноглобулинов классов IgG и IgM.
Прогноз: течение заболевания в основном доброкачественное.
Диагностический критерий - снижение у пациентов старше 4 лет уровня сывороточного IgA меньше 0,07 г/л при нормальном содержании IgG и IgM и исключении других причин гипогаммаглобулинемии. Диагностически значимы:
Изолированное снижение уровня IgA в сыворотке (меньше 0,05 г/л) при нормальном уровне других изотипов иммуноглобулинов у детей старше 1 года, отсутствие IgAl и IgA2. Уровень IgM и IgG в норме. Однако у некоторых больных выявляют дефицит IgG2;
- если уровень IgA находится в пределах от 0,05 г/л до 0,2 г/л, то диагностируют частичную недостаточность IgA; нормальное количество Т-лимфоцитов и их субклассов;
- обычно нормальное количество В-лимфоцитов (CD19\CD20);
- нормальное количество NK-клеток (CD16 CD56).
У пациентов с дефицитом IgA
, особенно при отсутствии секреторного IgA, необходимо исследовать уровень субклассов IgA. У некоторых пациентов селективная недостаточность IgA может прогрессировать с развитием в дальнейшем ОВИН. Необходим длительный регулярный мониторинг содержания иммуноглобулинов (в том числе у бессимптомных пациентов).
Определение аутоантител (антинуклеарных, антитиреоидных и др.).
При пищевой непереносимости или мальабсорбции необходимо аллерготестирование и определение антител к молоку и антиглутеновых IgG-антител.
Лечение . Пациентам с бессимптомным селективным дефицитом IgA постоянное лечение не требуется. Пациентам с проявлениями инфекционных заболеваний назначают с профилактической целью антибиотики. Интенсивное антибактериальное лечение проводят у всех больных во время возникновения инфекционного заболевания. Пациентам не противопоказана рутинная иммунизация. Заместительная иммуноглобулиновая терапия противопоказана, когда у больного выявляют аутоантитела против IgA. Следует учитывать тот факт, что избирательный дефицит IgA относится к некорригируемым первичным иммунным дефектам. Лечебные мероприятия сводятся к симптоматической терапии инфекционных, аллергических и аутоиммунных заболеваний. Иммунотропные препараты назначают главным образом в связи с проявлением повышенной инфекционной заболеваемости.
Прогноз . У пациентов с селективным IgA-дефицитом прогноз зависит от наличия сопутствующего дефекта специфических антител, аллергии или аутоиммунных заболеваний. Нередко бессимптомное течение заболевания может нарушаться в связи с действием внешних поражающих факторов, например, в стрессовой ситуации, при иммуносупрессии, химиотерапии и т.д.


