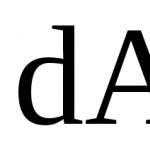17.3. Поверхностное натяжение. Энергия поверхностного слоя жидкости
Силы взаимодействия между молекулами жидкости быстро убывают и действуют только внутри сферы молекулярного действия с центром в данной молекуле. При этом если молекула находится внутри жидкости, то результирующая сил молекулярного взаимодействия равна нулю. Это не относится к молекулам, находящимся у поверхности жидкости, в ее поверхностном слое. На молекулы поверхностного слоя действует сила направленная внутрь жидкости, перпендикулярно ее поверхности Объясняется это тем, что концентрация молекул жидкости над ее поверхностью (в паре или газе, с которым граничит жидкость) мала (рис.17.3).
Эта равнодействующая стремится втянуть внутрь данную молекулу во внутренние слои жидкости. Следовательно, весь поверхностный слой жидкости находится в особом состоянии. Он оказывает на жидкость некоторое давление. В соответствии с этим молекулы жидкости в поверхностном слое обладают дополнительной потенциальной энергией.
Перемещение молекулы из поверхностного слоя внутрь жидкости сопровождается совершением работы, при этом потенциальная энергия молекул поверхностного слоя уменьшается, переходит в кинетическую энергию этих молекул. Переход молекулы из глубины жидкости в поверхностный слой требует совершения работы по преодолению результирующей силы. Эта работа может совершаться за счет дополнительной энергии за счет ее кинетической энергии. Потенциальная энергия молекулы, перешедшей в поверхностный слой, увеличивается. С течением времени, при неизменных внешних условиях, устанавливается равновесие (число молекул, покинувших поверхностный слой, будет равно числу молекул вновь оказавшихся в этом слое). Число молекул в поверхностном слое будет неизменным.
Кроме сил, действующих на молекулы поверхностного слоя в перпендикулярном направлении к поверхности, на них действуют силы в горизонтальном направлении (по касательной к поверхности жидкости). Они вызывают стремление жидкости сократить (уменьшить) свою поверхность. Эти силы получили название сил поверхностного натяжения. Следовательно, силы поверхностного натяжения направлены по касательной к поверхности жидкости, перпендикулярно к участку контура, охватывающего поверхность жидкости.
Изменение внешних условий может изменить поверхность жидкости, в результате нарушается равновесие, и некоторое количество молекул может перейти в поверхностный слой. В этом случае будет совершаться работа dA пропорциональная изменению поверхности жидкости на dS
 ,
(17.10)
,
(17.10)
где "минус" показывает, что увеличение поверхности жидкости сопровождается совершением работы;
- коэффициент поверхностного натяжения, который характеризует свойства поверхности жидкости и показывает, какую работу необходимо совершить, чтобы увеличить поверхность жидкости на единицу поверхности.
Работа
по изменению поверхности жидкости может
совершаться либо за счет изменения
потенциальной энергии поверхностного
слоя жидкости, (поверхностной энергии
жидкости dW ps),
либо внешними силами. При этом
 ,
но
,
но
 тогда
тогда

 или
или
 .
(17.11)
.
(17.11)
Потенциальная энергия поверхностного слоя жидкости W ps является составной частью внутренней энергии жидкости и ее свободной энергии.
Известно, что при неизменных внешних условиях, в частности при постоянной температуре, любая термодинамическая система стремится к состоянию с свободной минимальной энергией. А так как W ps S, то, следовательно, W ps к минимальному значению, при минимальном значении поверхности S. Таким образом, при постоянной температуре жидкость стремится к такому состоянию, при котором ее поверхность минимальна. Данное утверждение позволяет предсказать, как будет вести себя жидкость в тех или иных условиях.
Предположим, что поверхностный слой жидкости занимает некоторую поверхность. Этот слой стремится уменьшить свою поверхность. Чтобы система находилась в равновесии, к границе слоя необходимо приложить силу, численно равную силе поверхностного натяжения F (рис.17.3).
Если
под действием этой силы граница
поверхностного слоя сместится на dx,
то будет совершена работа
 .
.
Эта работа

 a
a
 .
(17.13)
.
(17.13)
Следовательно, коэффициент поверхностного натяжения, численно равен силе поверхностного натяжения, которая стремится изменить длину (величину) контура, охватывающего поверхность жидкости, на единицу.
Силами поверхностного натяжения определяется форма капель жидкости. Так как обычно жидкость находится в поле земного тяготения, то ее капли принимают форму, соответствующую минимальной сумме поверхностной энергии и потенциальной энергии в поле тяготения в зависимости от соотношения этих энергий. У капель жидкости, обладающих достаточным объемом, форма типа эллипсоида. По мере уменьшения размеров капли поверхностная энергия начинает играть существенную роль, т.к. объем и масса капли уменьшаются пропорционально кубу, а ее поверхность - квадрату радиуса. Поэтому очень малые капли принимают шарообразную форму. В условиях невесомости жидкость принимает сферическую форму при любом объеме.
Установить зависимость коэффициента поверхностного натяжения от температуры можно, применив к растяжению жидкой пленки первое начало термодинамики.
П редположим,
что пленка состоит из чистой жидкости,
(хотя такая пленка неустойчива) и в ней
совершается некоторый замкнутый цикл,
состоящий из изотермического и
адиабатического расширений и таких же
процессов сжатия. Пусть в начальном
состоянии пленка находится в некотором
состоянии "1" и характеризуется
температуройT.
Сообщив ей некоторое количество тепла
dQ,
можно изотермически перевести (растянуть)
ее в состояние "2". Произойдет
изменение площади пленки на
редположим,
что пленка состоит из чистой жидкости,
(хотя такая пленка неустойчива) и в ней
совершается некоторый замкнутый цикл,
состоящий из изотермического и
адиабатического расширений и таких же
процессов сжатия. Пусть в начальном
состоянии пленка находится в некотором
состоянии "1" и характеризуется
температуройT.
Сообщив ей некоторое количество тепла
dQ,
можно изотермически перевести (растянуть)
ее в состояние "2". Произойдет
изменение площади пленки на
 ,
за счет совершенной работы (рис. 17.4). При
этом
,
за счет совершенной работы (рис. 17.4). При
этом
 . (17.14)
. (17.14)
Поверхностное натяжение в этом случае не изменится.
Если из состояния "2" пленку адиабатически перевести в состояние "3" (растянуть), то за счет работы внешних сил, температура понизится на dT, что приведет к изменению коэффициента поверхностного натяжения на d.
При изотермическом сокращении пленки, она перейдет в состояние "4", а при адиабатическом - вернется в состояние "1".
Работа такого цикла равна разности работ при расширении и сжатии. Можно показать, что она в этом случае будет равна
 . (17.15)
. (17.15)
Если учесть, что вначале пленкой было получено dQ теплоты, то коэффициент полезного действия цикла
 ,
(17.16)
,
(17.16)
где "минус" указывает на то, что при сокращении пленки выделяется некоторое количество тепла. Тогда
 (17.17)
(17.17)
где r = dQ/S - количество тепла, затраченное на изменение пленки на единицу.
Таким образом, с повышением температуры величина коэффициента поверхностного натяжения уменьшается.
Подобно упругой пленке поверхностный слой жидкости стремится принять форму плоскости. Поэтому в изогнутом слое жидкости появляются силы, создающие дополнительное давление, увеличивающее или уменьшающее молекулярное давление. С учетом данного утверждения полное молекулярное давление будет равно
 ,
(17.18)
,
(17.18)
где p o - молекулярное давление жидкости с плоской поверхностью;
p - дополнительное давление, возникающее за счет кривизны поверхности;
"плюс" - соответствует выпуклой поверхности;
"минус" – соответствует вогнутой поверхности.
П оверхностное
натяжение жидкости обуславливает
дополнительное давление в жидкости,
величина которого зависит от радиуса
кривизны поверхности и коэффициента
поверхностного натяжения. Получим
формулу для расчета дополнительного
давления под искривленной поверхностью
жидкости (твердого тела), называемую
формулой Лапласа.
оверхностное
натяжение жидкости обуславливает
дополнительное давление в жидкости,
величина которого зависит от радиуса
кривизны поверхности и коэффициента
поверхностного натяжения. Получим
формулу для расчета дополнительного
давления под искривленной поверхностью
жидкости (твердого тела), называемую
формулой Лапласа.
Пусть площадь элемента поверхности равна ∆S. Вычислим силы поверхностного натяжения, приложенные к линиям "АВ" и "СД", которыми ограничен этот элемент поверхности F и F". Составляющие этих сил направлены к центру кривизны и обуславливают дополнительное давление. Эти составляющие, перпендикулярны к ∆S и направлены параллельно радиусу кривизны. Если поверхность плоская, то нормальной составляющей силы нет, дополнительного давления также нет. (Вторая составляющая F || на давление влияния не оказывает.) Итак, имеем:

 (17.19)
(17.19)
Сила
 имеет такую же составляющую
имеет такую же составляющую
 ;
;
 (17.20)
(17.20)
То
же получим и для участков "АС" и
"ВД" (только
 )
)
 ;
;
 (17.21)
(17.21)
 ;
;
 (17.22)
(17.22)
Сложив все четыре компонента, будем иметь
Откуда для дополнительного давления находим

 (17.24)
(17.24)
Полученное соотношение (17.24) называют формулой Лапласа. Из формулы Лапласа вытекает:
1)
при R 1
= R 2
= R,
 ,
что справедливо для сферической
поверхности;
,
что справедливо для сферической
поверхности;
2)
при R 2
,
 ,
что справедливо для цилиндрической
поверхности;
,
что справедливо для цилиндрической
поверхности;
3) силы, создающие дополнительное давление, всегда направлены к центру кривизны поверхности жидкости. В случае выпуклой поверхности, радиус кривизны R положителен, следовательно, дополнительное давление увеличивает молекулярное давление. В случае вогнутой поверхности, радиус кривизны R отрицателен, дополнительное давление уменьшает молекулярное давление.
Надо отметить, что полученный вывод справедлив для капли, которая полностью заполнена жидкостью, или для пузырька внутри жидкости.
Если имеется пузырек, например мыльный, то давление, которое оказывает поверхность пузырька на заключенный на него газ, вдвое больше. Это объясняется тем, что у такого пузырька две поверхности: наружная и внутренняя, каждая из которых создает почти одинаковые дополнительные давления. В этом случае:
а) для сферической поверхности
 ;
(17.25)
;
(17.25)
б) для цилиндрической поверхности
 .
(17.26)
.
(17.26)
Поверхностное натяжение жидкости.
Поверхностный слой жидкости.
Все жидкости и твёрдые тела ограничены внешней поверхностью, на которой они соприкасаются с фазами другого состава и структуры, например, с паром, другой жидкостью или твёрдым телом.
Свойства вещества в этой межфазовой поверхности , толщиной в несколько поперечников атомов или молекул, отличаются от свойств внутри объёма фазы .
Внутри объёма чистого вещества в твёрдом, жидком или газообразном состоянии любая молекула окружена себе подобными молекулами.
В пограничном слое молекулы находятся во взаимодействии или с другим числом молекул (другим в сравнении с взаимодействием внутри объёма вещества). Это происходит, например, на границе жидкости с их паром.
Среднее значение равнодействующей молекулярных сил притяжения, приложенных к молекуле, которая находится внутри жидкости, близко к нулю. На рисунке ниже эта молекула обозначена М1 .
Случайные флуктуации этой равнодействующей заставляют молекулу М1 совершать лишь хаотическое движение внутри жидкости.
Иначе обстоит дело с молекулами, находящимися в поверхностном слое жидкости .
Рассмотрим молекулу, находящуюся непосредственно на границе раздела фаз . На рисунке обозначим её М2 .
Если вокруг молекулы М2 описать сферу молекулярного действия, то внутри этой сферы окажутся центры многих других молекул, которые будут взаимодействовать с нашей молекулой. Радиус такой сферы составляет примерно 10 -9 м .
Для молекулы М2 в нижней полусфере окажется много молекул, а в верхней – значительно меньше, так как снизу находится жидкость, а сверху – пар или воздух.
Поэтому для молекулы М2 равнодействующая молекулярных сил притяжения в нижней полусфере много больше равнодействующей молекулярных сил в верхней полусфере. Силы, действующие в верхней полусфере так малы, что ими можно пренебречь.
Если рассмотреть ещё одну молекулу, которая, в сравнении с М2 будет немного больше «утоплена» в жидкость, но также находится в поверхностном слое. Обозначим её М3 .
Поскольку в верней полусфере М3 будут находиться другие молекулы жидкости, то они будут притягивать М3 к себе и частично уравновешивать силы притяжение молекул, находящихся в нижней полусфере М3 .
В результате общая равнодействующая сил, действующих на М3 окажется меньше общей равнодействующей М2 .
Обе равнодействующие будут направлены внутрь жидкости перепендикулярно к её поверхности.
Таким образом, все молекулы жидкости, находящиеся в поверхностном слое толщиной, равной радиусу молекулярного действия, втягиваются внутрь жидкости .
Но пространство внутри жидкости занято другими молекулами, поэтому поверхностный слой создаёт давление на жидкость, которое называют молекулярным давлением .
Энергия поверхностного слоя жидкости.
Поскольку молекулы жидкости, находящиеся в её поверхностном слое, втягиваются внутрь жидкости, их потенциальная энергия больше, чем у молекул внутри жидкости .
Эту дополнительную потенциальную энергию молекул поверхностного слоя жидкости называют свободной энергией . За счёт неё может быть произведена работа, связанная с уменьшением свободной поверхности жидкости.
И, наоборот, для того, чтобы вывести молекулы, находящиеся внутри жидкости, на её поверхность, нужно преодолеть противодействие молекулярных сил, т.е. произвести работу, которая нужна для увеличения свободной энергии поверхностного слоя жидкости.
При этом, изменение свободной энергии прямо пропорционально изменению площади поверхности жидкости.
Так как всякая система самопроизвольно переходит в состояние, при котором её потенциальная энергия минимальна, то жидкость должна самопроизвольно переходить в такое состояние, при котором площадь её свободной поверхности имеет наименьшую величину .
Например, капля дождя или тумана в воздухе приобретают форму шара, форму, соответствующую наименьшему уровню свободной энергии.
Коэффициент поверхностного натяжения
Коэффициент поверхностного натяжения – это величина, характеризующая зависимость работы молекулярных сил, идущих на изменение площади свободной поверхности жидкости и самой площади изменения этой поверхности.
σ = А/ΔS
σ - коэффициент поверхностного натяжения
А – работа молекулярных сил по изменению площади поверхности жидкости
ΔS - изменение площади поверхности жидкости
σ измеряется работой молекулярных сил при уменьшении площади свободной поверхности жидкости на единицу.
Коэффициент поверхностного натяжения зависит от рода жидкости и внешних условий, например, температуры.
Молекула М1 , которая расположена на поверхности жидкости, взаимодействует не только с молекулами, находящимися внутри жидкости, но и с молекулами на поверхности жидкости, расположенными в пределах сферы молекулярного действия.

Для молекулы М1 равнодействующая R молекулярных сил, направленных вдоль поверхности жидкости, равна нулю, а для молекулы М2 , расположенной у края поверхности, R отлична от нуля.
Из рисунка видно, что сила R направлена перпендикулярно к границе свободной поверхности и по касательной к самой поверхности.
Молекулярные силы, направленные вдоль поверхности жидкости, действуют на любую замкнутую линию на свободной поверхности жидкости по нормали к этой линии таким образом, что стремятся сократить площадь поверхности жидкости, ограниченную замкнутой линией.
Это можно показать на следующем опыте.
На проволочном кольце укрепляется нитка длиной L .

Если затянуть кольцо мыльной плёнкой, то нитка свободно расположится на этой плёнке (Рис. А). Площадь поверхности мыльной плёнки будет определяться контуром рамки.
Если прорвать мыльную плёнку с нижней стороны нитки, то молекулярные силы сократят поверхность, огрниченную теперь верхней частью контура и ниткой. При этом нитка натянется (Рис. В).
Сила, обусловленная взаимодействием молекул жидкости, вызывающая сокращение площади её свободной поверхности и направленная по касательной к этой поверхности, называется силой поверхностного натяжения .
Силы молекулярного давления втягивают молекулы с поверхности внутрь жидкости, а сокращают площадь свободной поверхности, т.е. закрывают образовавшиеся «окна» на этой поверхности.
Итак, поверхностный слой жидкости всегда находится в состоянии натяжения. Однако, это состояние нельзя сравнивать с натяжением упругой растянутой плёнки. Упругие силы возрастают по мере увеличения площади растянутой плёнки, а силы поверхностного натяжения от площади поверхности жидкости не зависят.
Опыт показывает, что на на коэффициент поверхностного натяжения влияет среда и температура жидкости. При повышении температуры жидкости её поверхностное натяжение уменьшается и при критической температуре становится равной нулю.
Поскольку молекулы жидкости, находящиеся в ее поверхностном слое, втягиваются внутрь жидкости, их потенциальная энергия больше, чем у молекул внутри жидкости. К этому выводу можно также прийти, если вспомнить, что потенциальная энергия взаимодействия молекул отрицательна (§ 2.4), и учесть, что молекулы в поверхностном слое жидкости на рис. 10.1) взаимодействуют с меньшим числом молекул, чем молекулы внутри жидкости

Эту дополнительную потенциальную энергию молекул поверхностного слоя жидкости называют свободной энергией; за счет нее может быть произведена работа, связанная с уменьшением свободной поверхности жидкости. Наоборот, для того чтобы вывести молекулы, находящиеся внутри жидкости, на ее поверхность, нужно преодолеть противодействие молекулярных сил, т. е. произвести работу, которая нужна для увеличения свободной энергии поверхностного слоя жидкости. Нетрудно сообразить, что при этом изменение свободной энергии прямо пропорционально изменению площади свободной поверхности жидкости
![]()
Так как то имеем
Итак, работа молекулярных сил А при уменьшении площади свободной поверхности жидкости прямо. пропорциональна Но эта работа должна еще зависеть от рода жидкости и внешних условий, например от температуры. Эту зависимость и выражает коэффициент .
Величина а, характеризующая зависимость работы молекулярных сил при изменении площади свободной поверхности жидкости от рода жидкости и внешних условий, называется коэффициентом поверхностного натяжения жидкости (или просто поверхностным натяжением), а измеряется работой молекулярных сил при уменьшении площади свободной поверхности жидкости на единицу:
Выведем единицу поверхностного, натяжения в СИ:
В СИ за единицу а принимается такое поверхностное натяжение, при котором молекулярные силы совершают работу в 1 Дж, уменьшая площадь свободной поверхности жидкости на .
Так как всякая система самопроизвольно переходит в состояние, при котором ее потенциальная энергия минимальна, то жидкость должна самопроизвольно переходить в такое состояние, при котором площадь ее свободной поверхности имеет наименьшую величину. Это можно показать с помощью следующего опыта.
На проволоке, изогнутой в виде буквы П, укрепляют подвижную поперечину I (рис. 10.2). Полученную таким образом рамку затягивают мыльной пленкой, опуская рамку в мыльный раствор. После вынимания рамки из раствора поперечина I перемещается вверх, т. е. молекулярные силы действительно уменьшают площадь свободной поверхности жидкости. (Подумайте, куда девается при этом освободившаяся энергия.)

Поскольку при одном и том же объеме наименьшая площадь поверхности имеется у шара, жидкость в состоянии невесомости принимает форму шара. По этой же причине маленькие капли жидкости имеют шарообразную форму. Форма мыльных пленок на различных каркасах всегда соответствует наименьшей площади свободной поверхности жидкости.
Когда вода из опрокинутого стакана разливается по полу или когда мы выдуваем мыльный пузырь, поверхность жидкости увеличивается. При этом возникают новые участки разреженного поверхностного слоя. Среднее расстояние между молекулами при их переходе из глубины жидкости на ее поверхность возрастает. Силы притяжения между молекулами жидкости совершают при этом отрицательную работу. В соответствии с законами механики это означает увеличение потенциальной энергии молекул, перешедших из глубины жидкости на поверхность.
Молекулы поверхностного слоя жидкости обладают избытком потенциальной энергии по сравнению с энергией, которой эти молекулы обладали бы, находясь внутри жидкости.
Избыточную потенциальную энергию, которой обладают молекулы на поверхности жидкости, называют поверхностной энергией.
С макроскопической (термодинамической) точки зрения поверхностная энергия - это один из видов внутренней энергии, отсутствующая у газов, но имеющаяся у жидкостей*.
* Поверхностной энергией обладают также твердые тела. Ведь особые условия, в которых находятся молекулы на поверхности жидкости, характерны и для поверхности твердых тел.
При растекании воды из опрокинутого стакана по полу увеличение энергии молекул поверхностного слоя происходит за счет работы силы тяжести. А при выдувании мыльного пузыря увеличение потенциальной энергии молекул поверхностного слоя происходит за счет работы сил давления воздуха в пузыре. Ведь для того чтобы пузырь раздувался, давление воздуха в нем должно быть больше атмосферного.
Поверхностное натяжение
Молекулы на всех участках поверхностного слоя жидкости находятся в одинаковых условиях, и два участка одинаковой площади обладают одинаковой поверхностной энергией. Это означает, что поверхностная энергия прямо пропорциональна площади поверхности жидкости. Поэтому отношение поверхностной энергии U n участка поверхности жидкости к площади S этого участка есть величина постоянная, не зависящая от площади S . Эту величину называют коэффициентом поверхностного натяжения или просто поверхностным натяжением и обозначают буквой σ:
Поверхностное натяжение представляет собой удельную поверхностную энергию, т. е. энергию, приходящуюся на поверхность единичной площади.
В СИ поверхностное натяжение выражается в джоулях на квадратный метр (Дж/м 2). Так как 1 Дж = 1 Н · м, то поверхностное натяжение можно выражать ив ньютонах на метр (Н/м).
Поверхностное натяжение а зависит от природы граничащих сред и от температуры. По мере повышения температуры различие между жидкостью и ее насыщенным паром постепенно стирается и при критической температуре исчезает совсем. Соответственно поверхностное натяжение для границы жидкость - насыщенный пар с повышением температуры уменьшается и при критической температуре становится равным нулю.
Из формулы (7.3.1) следует, что
 (7.3.2)
(7.3.2)
Следовательно, при уменьшении площади поверхности поверхностная энергия уменьшается. Молекулярные силы совершают при этом положительную работу, так как расстояния между молекулами при переходе их из поверхностного слоя в глубь жидкости уменьшаются. В состоянии равновесия жидкости поверхностная энергия имеет минимальное значение. Это соответствует минимальной при заданном объеме площади поверхности. Поэтому, как говорилось в § 7.1, жидкость принимает форму шара, если нет других сил, искажающих ее естественную сферическую форму.
В поверхностном слое жидкости запасена энергия, прямо пропорциональная площади поверхности. Поверхностная энергия - одна из форм внутренней энергии.
Наиболее характерным свойством жидкости, отличающим ее от газа, является то, что на границе с газом жидкость образует свободную поверхность, наличие которой приводит к возникновению явлений особого рода, называемых поверхностными. Своим возникновением они обязаны особым физическим условиям, в которых находятся молекулы вблизи свободной поверхности.
На каждую молекулу жидкости действуют силы притяжения со стороны окружающих ее молекул, расположенных от нее на расстоянии порядка 10 -9 м (радиус молекулярного действия). На молекулу M 1 , расположенную внутри жидкости (рис. 1), действуют силы со стороны таких же молекул, и равнодействующая этих сил близка к нулю.
Для молекул M 2 равнодействующие сил отличны от нуля и направлены внутрь жидкости, перпендикулярно к ее поверхности. Таким образом, все молекулы жидкости, находящиеся в поверхностном слое, втягиваются внутрь жидкости. Но пространство внутри жидкости занято другими молекулами, поэтому поверхностный слой создает давление на жидкость (молекулярное давление) .
Чтобы переместить молекулу M 3 , расположенную непосредственно под поверхностным слоем, на поверхность, необходимо совершить работу против сил молекулярного давления. Следовательно, молекулы поверхностного слоя жидкости обладают дополнительной потенциальной энергией по сравнению с молекулами внутри жидкости. Эту энергию называют поверхностной энергией .
Очевидно, что величина поверхностной энергии тем больше, чем больше площадь свободной поверхности.
Пусть площадь свободной поверхности изменилась на ΔS , при этом поверхностная энергия изменилась на \(~\Delta W_p = \alpha \Delta S\), где α - коэффициент поверхностного натяжения.
Так как для этого изменения необходимо совершить работу
\(~A = \Delta W_p ,\) то \(~A = \alpha \cdot \Delta S .\)
Отсюда \(~\alpha = \frac{A}{\Delta S}\) .
Единицей коэффициента поверхностного натяжения в СИ является джоуль на квадратный метр (Дж/м 2).
Коэффициент поверхностного натяжения - величина, численно равная работе, совершенной молекулярными силами при изменении площади свободной поверхности жидкости на единицу при изотермическом процессе.
Так как любая система, предоставленная сама себе, стремится занять такое положение, в котором ее потенциальная энергия наименьшая, то жидкость обнаруживает стремление к сокращению свободной поверхности.
Поверхностный слой жидкости ведет себя подобно растянутой резиновой пленке, т.е. все время стремится сократить площадь своей поверхности до минимальных размеров, возможных при данном объеме.
Пример : капля жидкости в состоянии невесомости имеет сферическую форму.
Литература
Аксенович Л. А. Физика в средней школе: Теория. Задания. Тесты: Учеб. пособие для учреждений, обеспечивающих получение общ. сред, образования / Л. А. Аксенович, Н.Н.Ракина, К. С. Фарино; Под ред. К. С. Фарино. - Мн.: Адукацыя i выхаванне, 2004. - C. 178-179.