Строение алканов
Алканы - углеводороды, в молекулах которых атомы связаны одинарными связями и которые соответствуют общей формуле C n H 2n+2 . В молекулах алканов все атомы углерода находятся в состоянии sр 3 -гибридизации .
Это означает, что все четыре гибридные орбитали атома углерода одинаковы по форме, энергии и направлены в углы равносторонней треугольной пирамиды - тетраэдра . Углы между орбиталями равны 109° 28′. Вокруг одинарной углерод-углеродной связи возможно практически свободное вращение, и молекулы алканов могут приобретать самую разнообразную форму с углами при атомах углерода, близкими к тетраэдрическому (109° 28′), например, в молекуле н-пентан.

Особо стоит напомнить о связях в молекулах алканов. Все связи в молекулах предельных углеводородов одинарные. Перекрывание происходит по оси, соединяющей ядра атомов, т. е. это σ-связи . Связи углерод - углерод являются неполярными и плохо поляризуемыми. Длина С-С связи в алканах равна 0,154 нм (1,54 10 10 м). Связи С-Н несколько короче. Электронная плотность немного смещена в сторону более электроотрицательного атома углерода, т. е. связь С-Н является слабополярной .
Гомологический ряд метана
Гомологи - вещества, сходные по строению и свойствам и отличающиеся на одну или более групп СН 2 .


Предельные углеводороды составляют гомологический ряд метана.
Изомерия и номенклатура алканов
Для алканов характерна так называемая структурная изомерия . Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкан, для которого характерны структурные изомеры, - это бутан.
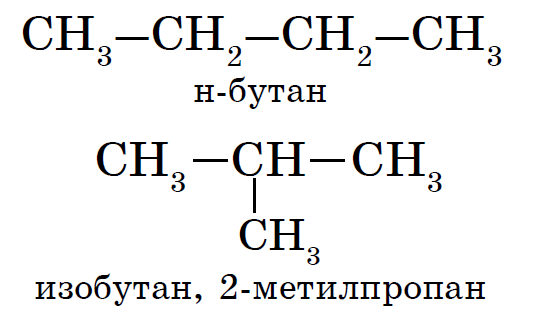
Рассмотрим подробнее для алканов основы номенклатуры ИЮПАК .
1. Выбор главной цепи . Формирование названия углеводорода начинается с определения главной цепи - самой длинной цепочки атомов углерода в молекуле, которая является как бы ее основой.
2. Нумерация атомов главной цепи . Атомам главной цепи присваивают номера. Нумерация атомов главной цепи начинается с того конца, к которому ближе стоит заместитель (структуры А, Б). Если заместители находятся на равном удалении от конца цепи, то нумерация начинается от того конца, при котором их больше (структура В). Если различные заместители находятся на равном удалении от концов цепи, то нумерация начинается с того конца, к которому ближе старший (структура Г). Старшинство углеводородных заместителей определяется по тому, в каком порядке следует в алфавите буква, с которой начинается их название: метил (-СН 3), затем пропил (-СН 2 -СН 2 -СН 3), этил (-СН 2 -СН 3) и т. д.
Обратите внимание на то, что название заместителя формируется заменой суффикса -ан на суффикс -ил в названии соответствующего алкана.
3. Формирование названия . В начале названия указывают цифры - номера атомов углерода, при которых находятся заместители. Если при данном атоме находятся несколько заместителей, то соответствующий номер в названии повторяется дважды через запятую (2,2-). После номера через дефис указывают количество заместителей (ди - два, три - три, тетра - четыре, пента - пять) и название заместителя (метил, этил, пропил). Затем без пробелов и дефисов - название главной цепи. Главная цепь называется как углеводород - член гомологического ряда метана (метан, этан, пропан и т. д.).




Названия веществ, структурные формулы которых приведены выше, следующие:
Структура А: 2-метилпропан;
Структура Б: 3-этилгексан;
Структура В: 2,2,4-триметилпентан;
Структура Г: 2-метил 4-этилгексан.
Отсутствие в молекулах предельных углеводородов полярных связей приводит к тому, что они плохо растворяются в воде , не вступают во взаимодействие с заряженными частицами (ионами) . Наиболее характерными для алканов являются реакции, протекающие с участием свободных радикалов .
Физические свойства алканов
Первые четыре представителя гомологического ряда метана - газы . Простейший из них - метан - газ без цвета, вкуса и запаха (запах «газа», почувствовав который, надо звонить 04, определяется запахом меркаптанов - серосодержащих соединений, специально добавляемых к метану, используемому в бытовых и промышленных газовых приборах для того, чтобы люди, находящиеся рядом с ними, могли по запаху определить утечку).
Углеводороды состава от С 5 Н 12 до С 15 Н 32 - жидкости; более тяжелые углеводороды - твердые вещества. Температуры кипения и плавления алканов постепенно увеличиваются с возрастанием длины углеродной цепи. Все углеводороды плохо растворяются в воде, жидкие углеводороды являются распространенными органическими растворителями.


Химические свойства алканов
Реакции замещения.
Наиболее характерными для алканов являются реакции свободнорадикального замещения , в ходе которого атом водорода замещается на атом галогена или какую-либо группу.
Приведем уравнения характерных реакций галогенирования :
В случае избытка галогена хлорирование может пойти дальше, вплоть до полного замещения всех атомов водорода на хлор :

Полученные вещества широко используются как растворители и исходные вещества в органических синтезах.
Реакция дегидрирования (отщепления водорода).
В ходе пропускания алканов над катализатором (Pt, Ni, Al 2 O 3 , Cr 2 O 3) при высокой температуре (400-600 °C) происходит отщепление молекулы водорода и образование алкена :
Реакции, сопровождающиеся разрушением углеродной цепи. Все предельные углеводороды горят с образованием углекислого газа и воды. Газообразные углеводороды, смешанные с воздухом в определенных соотношениях, могут взрываться.
1. Горение предельных углеводородов - это свободнорадикальная экзотермическая реакция, которая имеет очень большое значение при использовании алканов в качестве топлива:
В общем виде реакцию горения алканов можно записать следующим образом:
2. Термическое расщепление углеводородов .
Процесс протекает по свободнорадикальному механизму . Повышение температуры приводит к гомолитическому разрыву углерод-углеродной связи и образованию свободных радикалов.
Эти радикалы взаимодействуют между собой, обмениваясь атомом водорода, с образованием молекулы алкана и молекулы алкена :
Реакции термического расщепления лежат в основе промышленного процесса - крекинга углеводородов . Этот процесс является важнейшей стадией переработки нефти.
3. Пиролиз . При нагревании метана до температуры 1000 °С начинается пиролиз метана - разложение на простые вещества:
При нагревании до температуры 1500 °С возможно образование ацетилена :
4. Изомеризация . При нагревании линейных углеводородов с катализатором изомеризации (хлоридом алюминия) происходит образование веществ с разветвленным углеродным скелетом :

5. Ароматизация . Алканы с шестью или более углеродными атомами в цепи в присутствии катализатора циклизуются с образованием бензола и его производных:

Алканы вступают в реакции, протекающие по свободнорадикальному механизму, т. к. все атомы углерода в молекулах алканов находятся в состоянии sp 3 -гибридизации. Молекулы этих веществ построены при помощи ковалентных неполярных С-С (углерод - углерод) связей и слабополярных С-Н (углерод - водород) связей. В них нет участков с повышенной и с пониженной электронной плотностью, легко поляризуемых связей, т. е. таких связей, электронная плотность в которых может смещаться под действием внешних факторов (электростатических полей ионов). Следовательно, алканы не будут реагировать с заряженными частицами, т. к. связи в молекулах алканов не разрываются по гетеролитическому механизму.
Химические свойства. Физические свойства алканов
Физические свойства алканов
В обычных условиях первые четыре члена гомологического ряда алканов (С 1 - С 4) - газы. Нормальные алканы от пентана до гептадекана (С 5 - С 17) - жидкости, начиная с С 18 и выше - твердые вещества. По мере увеличения числа атомов углерода в цепи, т.е. с ростом относительной молекулярной массы, возрастают температуры кипения и плавления алканов.
При одинаковом числе атомов углерода в молекуле алканы с разветвленным строением имеют более низкие температуры кипения, чем нормальные алканы.
Алканы практически нерастворимы в воде, т.к. их молекулы малополярны и не взаимодействуют с молекулами воды. Жидкие алканы легко смешиваются друг с другом. Они хорошо растворяются в неполярных органических растворителях, таких, как бензол, тетрахлорметан и т.п.
Строение
Молекула простейшего алкана - метана - имеет форму правильного тетраэдра, в центре которого находится атом углерода, а в вершинах - атомы водорода. Углы между осями связей С-Н составляют 109°28" (рис. 29).
В молекулах других предельных углеводородов углы между связями (как С-Н, так и С-С) имеют такое же значение. Для описания формы молекул используется понятие гибридизации атомных орбиталей (см. часть I, §6).
В алканах все атомы углерода находятся в состоянии sp 3 - гибридизации (рис. 30).
Таким образом, атомы углерода в углеродной цепи не находятся на одной прямой. Расстояние между соседними атомами углерода (между ядрами атомов) строго фиксировано - это длина химической связи (0,154 нм). Расстояние С 1 - С 3 , С 2 - С 4 и т.д. (через один атом) тоже постоянны, т.к. постоянен угол между связями -валентный угол.

Расстояния между более удаленными атомами углерода могут изменяться (в некоторых пределах) в результате вращения вокруг s-связей. Такое вращение не нарушает перекрывания орбиталей, образующих s-связь, поскольку эта связь имеет осевую симметрию.


Разные пространственные формы одной молекулы, образующиеся при вращении групп атомов вокруг s-связей, называют конформациями (рис. 31).
Конформации различают по энергии, но это различие невелико (12-15 кДж/моль). Более устойчивы такие конформации алканов, в которых атомы расположены возможно дальше друг от друга (отталкивание электронных оболочек). Переход от одной конформации к другой осуществляется за счет энергии теплового движения. Для изображения конформации используют специальные пространственные формулы (формулы Ньюмена).
Не путать!
Следует различать понятия конформация и конфигурация.
Разные конформации могут превращаться друг в друга без разрыва химических связей. Для превращения молекулы с одной конфигурацией в молекулу с другой конфигурацией требуется разрыв химических связей.
Из четырех видов изомерии для алканов характерны два: изомерия углеродного скелета и оптическая изомерия (см. часть
Химические связи в алканах, их разрыв и образование определяют химические свойства алканов. Связи С-С и С-Н ковалентные, простые (s-связи), практически неполярные, достаточно прочные, поэтому:
1) алканы вступают чаще всего в такие реакции, которые идут с гемолитическим разрывом связей;
2) по сравнению с органическими соединениями других классов алканы обладают низкой реакционной способностью (их за это называют парафинами - «лишенными свойства»). Так, алканы устойчивы к действию водных растворов кислот, щелочей и окислителей (например, перманганата калия) даже при кипячении.
Алканы не вступают в реакции присоединения к ним других молекул, т.к. алканы не имеют в своих молекулах кратных связей.
Алканы подвергаются разложению при сильном нагревании в присутствии катализаторов в виде платины или никеля, при этом от алканов отщепляется водород.
Алканы могут вступать в реакции изомеризации. Характерной реакцией для них является реакция замещения, протекающая по радикальному механизму.
Химические свойства
Реакции радикального замещения
В качестве примера рассмотрим взаимодействие алканов с галогенами. Фтор реагирует очень энергично (как правило, со взрывом) - при этом рвутся все С-Н и С-С связи, и в результате образуются соединения CF 4 и HF. Практического значения реакция не имеет. Иод с алканами не взаимодействует. Реакции с хлором или бромом идут либо при освещении, либо при сильном нагревании; при этом происходит образование от моно- до полигалогензамещенных алканов, например:
СН 3 -СН 3 +Сl 2 ® hv СН 3 -СН 2 -Сl+НСl
Образование галогенопроизводных метана протекает по цепному свободнорадикальному механизму. Под действием света молекулы хлора распадаются на неорганические радикалы:
Неорганический радикал Сl . отрывает от молекулы метана атом водорода с одним электроном, образуя НС1 и свободный радикал СН 3
![]()
Свободный радикал взаимодействует с молекулой хлора Сl 2 , образуя галогенопроизводное и радикал хлора.
![]()
Реакция окисления начинается с отрыва атома водорода молекулой кислорода (которая представляет собой бирадикал) и далее идет как разветвленная цепная реакция. Количество радикалов в ходе реакции увеличивается. Процесс сопровождается
выделением большого количества теплоты, рвутся уже не только С-Н, но и С-С связи, так что в результате образуется оксид углерода (IV) и вода. Реакция может протекать как горение или приводит к взрыву.
2С n Н2 n+2 +(3n+1)О 2 ®2nСO 2 +(2n+2)Н 2 O
При обычной температуре реакция окисления не идет; ее можно инициировать либо поджиганием, либо действием электрического разряда.
При сильном нагревании (свыше 1000°С) алканы полностью разлагаются на углерод и водород. Эта реакция называется пиролизом.
СН 4 ® 1200° С+2Н 2
При мягком окислении алканов, в частности метана, кислородом воздуха в присутствии различных катализаторов могут быть получены метиловый спирт, формальдегид, муравьиная кислота.

Если метан пропускать через нагретую зону очень быстро, а затем сразу охлаждать водой, то в результате образуется ацетилен.
Эта реакция - основа промышленного синтеза, который называется крекингом (неполным разложением) метана.
Крекинг гомологов метана проводят при более низкой температуре (около 600°С). Например, крекинг пропана включает следующие стадии:

Итак, крекинг алканов приводит к образованию смеси алканов и алкенов меньшей молекулярной массы.
Нагревание алканов до 300-350°С (крекинг еще не идет) в присутствии катализатора (Pt или Ni) приводит к дегидрированию - отщеплению водорода.

При действии разбавленной азотной кислоты на алканы при 140°С и небольшом давлении протекает радикальная реакция:
СН 3 -СН 3 + HNO 3 ®CH 3 -CH 2 -NO 2 + Н 2 О Изомеризация
При определенных условиях алканы нормального строения могут превращаться в алканы с разветвленной цепью.
Получение алканов
Рассмотрим получение алканов на примере получения метана. Метан широко распространен в природе. Он является главной составной частью многих горючих газов, как природных (90-98%), так и искусственных, выделяющихся при сухой перегонке дерева, торфа, каменного угля, а также при крекинге нефти. Природные газы, особенно попутные газы нефтяных месторождений, помимо метана содержат этан, пропан, бутан и пентан.
Метан выделяется со дна болот и из каменноугольных пластов в рудниках, где он образуется при медленном разложении растительных остатков без доступа воздуха. Поэтому метан часто называют болотным газом или рудничным газом.
В лаборатории метан получают при нагревании смеси ацетата натрия с гидроксидом натрия:
CH 3 COONa+NaOH® 200° Na 2 CO 3 +CH 4
или при взаимодействии карбида алюминия с водой: Аl 4 Сl 3 +12H 2 O®4Аl(ОН) 3 +3CH 4
В последнем случае метан получается весьма чистым.
Метан может быть получен из простых веществ при нагревании в присутствии катализатора:
С+2Н 2 ® Ni СН 4 8 также синтезом на основе водяного газа
CO+3H 2 ® Ni CH 4 +H 2 O
Этот способ имеет промышленное значение. Однако используют обычно метан природных газов или газов, образующихся при коксовании каменных углей и при переработке нефти.
Гомологи метана, как и метан, в лабораторных условиях получают прокаливанием солей соответствующих органических кислот с щелочами. Другой способ - реакция Вюрца, т.е. нагревание моногалогенопроизводных с металлическим натрием, например:
С 2 Н 5 Br+2Na+BrC 2 H 6 ® С 2 Н 5 -С 2 Н 5 +2NaBr
В технике для получения технического бензина (смесь углеводородов, содержащих 6-10 атомов углерода) применяют синтез
из оксида углерода (II) и водорода в присутствии катализатора (соединения кобальта) и при повышенном давлении. Процесс
можно выразить уравнением
nСО+(2n+1)Н 2 ® 200° C n H 2n+2 +nН 2 O
I Итак, основным источником алканов служат природный газ и нефть. Однако некоторые предельные углеводороды синтезируют из других соединений.
Применение алканов
Большая часть алканов используется как топливо. Крекинг и
Дегидрирование их приводит к непредельным углеводородам, на
базе которых получают множество других органических веществ.
Метан - основная часть природных газов (60-99%). В состав
природных газов входят пропан и бутан. Жидкие углеводороды
применяются в качестве горючего в двигателях внутреннего сгорания а автомашинах, самолетах и др. Очищенная смесь жидких
и твердых алканов образует вазелин. Высшие алканы являются
исходными веществами при получении синтетических моющих средств. Алканы, полученные путем изомеризации, используются в производстве высококачественных бензинов и каучука. Ниже приведена схема применения метана

Циклоалканы
Строение
Циклоалканы - насыщенные углеводороды, в молекулах которых имеется замкнутое кольцо из углеродных атомов.
Циклоалканы (циклопарафины) образуют гомологический ряд с общей формулой С n Н 2 n , в котором первым членом является
циклопропан С 3 Н 6 , т.к. для образования кольца необходимо наличие не менее трех атомов углерода.
Циклоалканы имеют несколько названий: циклопарафины, нафтены, цикланы, полиметилены. Примеры некоторых соединений:

Формула С n Н 2 n характерна для циклопарафинов, и точно такая же формула описывает гомологический ряд алкенов (непредельных углеводородов, имеющих одну кратную связь). Из этого можно сделать вывод, что каждому циклоалкану изомерен соответствующий алкен - это пример «межклассовой» изомерии.
Циклоалканы по размеру цикла делятся на ряд групп, из которых рассмотрим две: малые (С 3 , С 4) и обычные (С 5 -С 7) циклы.
Названия циклоалканов строятся путем добавления приставки цикло- к названию алкана с соответствующим числом атомов углерода. Нумерацию в цикле проводят так, чтобы заместители получили наименьшие номера.
Структурные формулы циклоалканов обычно записываются в сокращенном виде, используя геометрическую форму цикла и опуская символы атомов углерода и водорода. Например:

Структурная изомерия циклоалканов обусловлена размером цикла (циклобутан и метилциклопропан - изомеры) и положением заместителей в цикле (например, 1,1- и 1,2-диметилбутан), а также их строением.
Пространственная изомерия также характерна для циклоалканов, т.к. она связана с различным расположением заместителей относительно плоскости цикла. При расположении заместителей по одну сторону от плоскости цикла получаются цис-изомеры, по разные стороны - транс-изомеры.
Алканами в химии называют предельные углеводороды, у которых углеродная цепь является незамкнутой и состоит из углерода, связанных друг с другом при помощи одинарных связей. Также характерной особенностью алканов есть то, что они совсем не содержат двойных либо тройных связей. Порой алканы называют парафинами, дело в том, что парафины собственно и являются смесью предельных углеродов, то есть алканов.
Формула алканов
Формулу алкана можно записать как:
При этом n больше или равно 1.
Алканам свойственна изомерия углеродного скелета. При этом соединения могут принимать разные геометрические формы, как например это показано на картинке ниже.

Изомерия углеродного скелета алканов
С увеличением роста углеродной цепи увеличивается и количество изомеров. Так, например, у бутана есть два изомера.

Получение алканов
Алкан как правило получают различными синтетическими методами. Скажем, один из способов получения алкана предполагает реакцию «гидрирования», когда алканы добываются из ненасыщенных углеводов под воздействием катализатора и при температуре.
Физические свойства алканов
Алканы от других веществ отличаются полным отсутствием цвета, также они не растворим в воде. Температура плавления алканов повышается с увеличением их молекулярной массы и длины углеводородной цепи. То есть чем более разветвленным является алкан, тем у него большая температура горения и плавления. Газообразные алканы и вовсе горят бледно-голубым или бесцветным пламенем, при этом выделяя много тепла.
Химические свойства алканов
Алканы в химическом плане малоактивные вещества, по причине прочности крепких сигма связей С-С и С-Н. При этом связи С-С неполярны, а С-Н малополярны. А так как все это малополяризируемые виды связей, которые относятся к сигма виду, то разрываться они будут по механизму гомолитическому, в результате чего образуются радикалы. И как следствия химические свойства алканов представляют собой в основном реакции радикального замещения.
Так выглядит формула радикального замещения алканов (галогенирование алканов).
Помимо этого также можно выделить такие химические реакции как нитрирование алканов (реакция Коновалова).
Реакция эта протекает при температуре 140 С, причем лучше всего именно с третичным атомом углерода.
Крекинг алканов – эта реакция протекает при действии высоких температур и катализаторов. Тогда создаются условия, когда высшие алканы могут рвать свои связи образуя алканы более низкого порядка.
Предельные углеводороды - это такие соединения, которые представляют собой молекулы, состоящие из атомов углерода, находящихся в состоянии гибридизации sp 3 . Они связаны между собой исключительно ковалентными сигма-связями. Название «предельные» или «насыщенные» углеводороды исходит из того факта, что эти соединения не имеют возможности присоединять какие-либо атомы. Они предельны, полностью насыщены. Исключение составляют циклоалканы.
Что такое алканы?
Алканы - это углеводороды предельные, а их углеродная цепь незамкнута и состоит из атомов углерода, связанных между собой при помощи одинарных связей. Она не содержит иных (то есть двойных, как у алкенов, или же тройных, как у алкилов) связей. Алканы также называют парафинами. Это название они получили, так как общеизвестные парафины являются смесью преимущественно данных предельных углеводородов С 18 -С 35 с особой инертностью.
Общие сведения об алканах и их радикалах
Их формула: С n Р 2 n +2 , здесь n больше или равно 1. Молярная масса вычисляется по формуле: М = 14n + 2. Характерная особенность: окончания в их названиях - «-ан». Остатки их молекул, которые образуются в результате замещения водородных атомов на иные атомы, имеют название алифатических радикалов, или алкилов. Их обозначают буквой R. Общая формула одновалентных алифатических радикалов: С n Р 2 n +1 , здесь n больше или равно 1. Молярная масса алифатических радикалов вычисляется по формуле: М = 14n + 1. Характерная особенность алифатических радикалов: окончания в названиях «-ил». Молекулы алканов имеют свои особенности строения:
- связь С-С характеризуется длиной 0,154 нм;
- связь С-Н характеризуется длиной 0,109 нм;
- валентный угол (угол между связями углерод-углерод) равен 109 градусов и 28 минут.

Начинают гомологический ряд алканы: метан, этан, пропан, бутан и так далее.
Физические свойства алканов
Алканы - это вещества, которые не имеют цвета и нерастворимы в воде. Температура, при которой алканы начинают плавиться, и температура, при которой они закипают, повышаются в соответствии с увеличением молекулярной массы и длины углеводородной цепи. От менее разветвленных к более разветвленным алканам температуры кипения и плавления понижаются. Газообразные алканы способны гореть бледно-голубым либо бесцветным пламенем, при этом выделяется довольно много тепла. СН 4 -С 4 Н 10 представляют собой газы, у которых отсутствует также и запах. С 5 Н 12 -С 15 Н 32 - это жидкости, которые обладают специфическим запахом. С 15 Н 32 и так далее - это твердые вещества, которые также не имеют запаха.
Химические свойства алканов
Данные соединения являются малоактивными в химическом плане, что можно объяснить прочностью трудноразрываемых сигма-связей - С-С и С-Н. Также стоит учитывать, что связи С-С неполярны, а С-Н малополярны. Это малополяризуемые виды связей, относящиеся к сигма-виду и, соответственно, разрываться по наибольшей вероятности они станут по механизму гомолитическому, в результате чего будут образовываться радикалы. Таким образом, химические свойства алканов в основном ограничиваются реакциями радикального замещения.

Реакции нитрования
Алканы взаимодействуют только с азотной кислотой с концентрацией 10% либо с оксидом четырехвалентного азота в газовой среде при температуре 140°С. Реакция нитрования алканов носит название реакции Коновалова. В результате образуются нитросоединения и вода: CH 4 + азотная кислота (разбавленная) = CH 3 - NO 2 (нитрометан) + вода.
Реакции горения
Предельные углеводороды очень часто применяются как топливо, что обосновано их способностью к горению: С n Р 2n+2 + ((3n+1)/2) O 2 = (n+1) H 2 O + n СО 2 .
Реакции окисления
В химические свойства алканов также входит их способность к окислению. В зависимости от того, какие условия сопровождают реакцию и как их изменяют, можно из одного и того же вещества получить различные конечные продукты. Мягкое окисление метана кислородом при наличии катализатора, ускоряющего реакцию, и температуры около 200 °С может дать в результате следующие вещества:
1) 2СН 4 (окисление кислородом) = 2СН 3 ОН (спирт - метанол).
2) СН 4 (окисление кислородом) = СН 2 О (альдегид - метаналь или формальдегид) + Н 2 О.
3) 2СН 4 (окисление кислородом) = 2НСООН (карбоновая кислота - метановая или муравьиная) + 2Н 2 О.

Также окисление алканов может производиться в газообразной или жидкой среде воздухом. Такие реакции приводят к образованию высших жирных спиртов и соответствующих кислот.
Отношение к нагреванию
При температурах, не превышающих +150-250°С, обязательно в присутствии катализатора, происходит структурная перестройка органических веществ, которая заключается в изменении порядка соединения атомов. Данный процесс называется изомеризацией, а вещества, полученные в результате реакции - изомерами. Таким образом, из нормального бутана получается его изомер - изобутан. При температурах 300-600°С и наличии катализатора происходит разрыв связей С-Н с образованием молекул водорода (реакции дегидрирования), молекул водорода с замыканием углеродной цепи в цикл (реакции циклизации или ароматизации алканов):
1) 2СН 4 = С 2 Н 4 (этен) + 2Н 2.
2) 2СН 4 = С 2 Н 2 (этин) + 3Н 2.
3) С 7 Н 16 (нормальный гептан) = С 6 Н 5 - СН 3 (толуол) + 4Н 2 .

Реакции галогенирования
Такие реакции заключаются во введении в молекулу органического вещества галогенов (их атомов), в результате чего образуется связь С-галоген. При взаимодействии алканов с галогенами образуются галогенпроизводные. Данная реакция обладает специфическими особенностями. Она протекает по механизму радикальному, и чтобы ее проинициировать, необходимо на смесь галогенов и алканов воздействовать ультрафиолетовым излучением или же просто нагреть ее. Свойства алканов позволяют реакции галогенирования протекать, пока не будет достигнуто полное замещение на атомы галогена. То есть хлорирование метана не закончится одной стадией и получением метилхлорида. Реакция пойдет далее, будут образовываться все возможные продукты замещения, начиная с хлорметана и заканчивая тетрахлорметаном. Воздействие хлора при данных условиях на другие алканы приведет к образованию различных продуктов, полученных в результате замещения водорода у различных атомов углерода. От температуры, при которой идет реакция, будет зависеть соотношение конечных продуктов и скорость их образования. Чем длиннее углеводородная цепь алкана, тем легче будет идти данная реакция. При галогенировании сначала будет замещаться атом углерода наименее гидрированый (третичный). Первичный вступит в реакцию после всех остальных. Реакция галогенирования будет происходить поэтапно. На первом этапе заместиться только один атом водорода. C растворами галогенов (хлорной и бромной водой) алканы не взаимодействуют.

Реакции сульфохлорирования
Химические свойства алканов также дополняются реакцией сульфохлорирования (она носит название реакции Рида). При воздействии ультрафиолетового излучения алканы способны реагировать со смесью хлора и диоксида серы. В результате образуется хлороводород, а также алкильный радикал, который присоединяет к себе диоксид серы. В результате получается сложное соединение, которое становится стабильным благодаря захвату атома хлора и разрушения очередной его молекулы: R-H + SO 2 + Cl 2 + ультрафиолетовое излучение = R-SO 2 Cl + HCl. Образовавшиеся в результате реакции сульфонилхлориды находят широкое применение в производстве поверхностно-активных веществ.
ОПРЕДЕЛЕНИЕ
Алканы – предельные (алифатические) углеводороды, состав которых выражается формулой C n H 2 n +2 .
Алканы образуют гомологический ряд, каждое химическое соединение которого по составу отличается от последующего и предыдущего на одинаковое число атомов углерода и водорода – CH 2 , а вещества, входящие в гомологический ряд, называются гомологами. Гомологический ряд алканов представлен в таблице 1.
Таблица 1. Гомологический ряд алканов.
В молекулах алканов выделяют первичные (т.е. связанные одной связью), вторичные (т.е. связанные двумя связями), третичные (т.е. связанные тремя связями) и четвертичные (т.е. связанные четырьмя связями) атомы углерода.
C 1 H3 – C 2 H 2 – C 1 H 3 (1 – первичные, 2- вторичные атомы углерода)
CH 3 –C 3 H(CH 3) – CH 3 (3- третичный атом углерода)
CH 3 – C 4 (CH 3) 3 – CH 3 (4- четвертичный атом углерода)
Для алканов характерна структурная изомерия (изомерия углеродного скелета). Так, у пентана имеются следующие изомеры:
CH 3 -CH 2 -CH 2 -CH 2 -CH 3 (пентан)
CH 3 –CH(CH 3)-CH 2 -CH 3 (2-метилбутан)
CH 3 -C(CH 3) 2 -CH 3 (2,2 – диметилпропан)
Для алканов, начиная с гептана, характерна оптическая изомерия.
Атомы углерода в предельных углеводородах находятся в sp 3 –гибридизации. Углы между связями в молекулах алканов 109,5.
Химические свойства алканов
При обычных условиях алканы химически инертны — не реагируют ни с кислотами, ни со щелочами. Это объясняется высокой прочностью -связей С-С и С-Н. Неполярные связи С-С и С-Н способны расщепляться только гомолитически под действием активных свободных радикалов. Поэтому алканы вступают в реакции, протекающие по механизму радикального замещения. При радикальных реакция в первую очередь замещаются атомы водорода у третичных, затем у вторичных и первичных атомов углерода.
Реакции радикального замещения имеют цепной характер. Основные стадии: зарождение (инициирование) цепи (1) – происходит под действием УФ-излучения и приводит к образованию свободных радикалов, рост цепи (2) – происходит за счет отрыва атома водорода от молекулы алкана; обрыв цепи (3) – происходит при столкновении двух одинаковых или разных радикалов.
X:X → 2X . (1)
R:H + X . → HX + R . (2)
R . + X:X → R:X + X . (2)
R . + R . → R:R (3)
R . + X . → R:X (3)
X . + X . → X:X (3)
Галогенирование. При взаимодействии алканов с хлором и бромом при действии УФ-излучения или высокой температуры образуется смесь продуктов от моно- до полигалогензамещенных алканов:
CH 3 Cl +Cl 2 = CH 2 Cl 2 + HCl (дихлорметан)
CH 2 Cl 2 +Cl 2 = CHCl 3 + HCl (трихлорметан)
CHCl 3 +Cl 2 = CCl 4 + HCl (тетрахлорметан)
Нитрование (реакция Коновалова) . При действии разбавленной азотной кислоты на алканы при 140С и небольшом давлении протекает радикальная реакция:
CH 3 -CH 3 +HNO 3 = CH 3 -CH 2 -NO 2 (нитроэтан) + H 2 O
Сульфохлорирование и сульфоокисление. Прямое сульфирование алканов протекает с трудом и чаще всего сопровождается окислением, в результате чего образуются алкансульфонилхлориды:
R-H + SO 2 + Cl 2 → R-SO 3 Cl + HCl
Реакция сульфоокисления протекает аналогично, только в этом случае образуются алкансульфоновые кислоты:
R-H + SO 2 + ½ O 2 → R-SO 3 H
Крекинг – радикальный разрыв связей С-С. Протекает при нагревании и в присутствии катализаторов. При крекинге высших алканов образуются алкены, при крекинге метана и этана образуется ацетилен:
С 8 H 18 = C 4 H 10 (бутан)+ C 3 H 8 (пропан)
2CH 4 = C 2 H 2 (ацетилен) + 3H 2
Окисление . При мягком окислении метана кислородом воздуха могут быть получены метанол, муравьиный альдегид или муравьиная кислота. На воздухе алканы сгорают до углекислого газа и воды:
C n H 2 n +2 + (3n+1)/2 O 2 = nCO 2 + (n+1)H 2 O
Физические свойства алканов
При обычных условиях С 1 -С 4 – газы, С 5 -С 17 – жидкости, начиная с С 18 – твердые вещества. Алканы практически нерастворимы в воде, но, хорошо растворимы в неполярных растворителях, например, в бензоле. Так, метан СН 4 (болотный, рудничий газ) – газ без цвета и запаха, хорошо растворимый в этаноле, эфире, углеводородах, но плохо растворимый в воде. Метан используют в качестве высококалорийного топлива в составе природного газа, в качестве сырья для производства водорода, ацетилена, хлороформа и других органических веществ в промышленных масштабах.
Пропан С 3 Н 8 и бутан С 4 Н 10 – газы, применяемые в быту, в качестве балонных газов, за счет легкой сжижаемости. Пропан используется в качестве автомобильного топлива, поскольку является более экологически чистым, чем бензин. Бутан – сырье для получения 1,3 –бутадиена, использующегося в производстве синтетического каучука.
Получение алканов
Алканы получают из природных источников – природного газа (80-90% — метан, 2-3% — этан и другие предельные углеводороды), угля, торфа, древесины, нефти и горного воска.
Выделяют лабораторные и промышленные способы получения алканов. В промышленности алканы получают из битумного угля (1) или по реакции Фишера-Тропша (2):
nC + (n+1)H 2 = C n H 2 n +2 (1)
nCO + (2n+1)H 2 = C n H 2 n +2 + H 2 O (2)
К лабораторным способам получения алканов относят: гидрирование непредельных углеводородов при нагревании и в присутствии катализаторов (Ni, Pt, Pd) (1), взаимодействием воды с металлоорганическими соединениями (2), электролизом карбоновых кислот (3), по реакциям декарбоксилирования (4) и Вюрца (5) и другими способами.
R 1 -C≡C-R 2 (алкин) → R 1 -CH = CH-R 2 (алкен) → R 1 -CH 2 – CH 2 -R 2 (алкан) (1)
R-Cl + Mg → R-Mg-Cl + H 2 O → R-H (алкан) + Mg(OH)Cl (2)
CH 3 COONa↔ CH 3 COO — + Na +
2CH 3 COO — → 2CO 2 + C 2 H 6 (этан) (3)
CH 3 COONa + NaOH → CH 4 + Na 2 CO 3 (4)
R 1 -Cl +2Na +Cl-R 2 →2NaCl + R 1 -R 2 (5)
Примеры решения задач
ПРИМЕР 1
| Задание | Определите массу хлора, необходимого для хлорирования по первой стадии 11,2 л метана. |
| Решение |
Запишем уравнение реакции первой стадии хлорирования метана (т.е. в реакции галогенирования происходит замещения всего одного атома водорода, в результате чего образуется монохлорпроизводное):
CH 4 + Cl 2 = CH 3 Cl + HCl (хлорметан) Найдем количество вещества метана: v(CH 4) = V(CH 4)/V m v(CH 4) = 11,2/22,4 = 0,5 моль По уравнению реакции количество моль хлора и количество моль метана равны 1 моль, следовательно, практическое количество моль хлора и метана также будет одинаковым и будет равно: v(Cl 2) = v(CH 4) = 0,5 моль Зная количество вещества хлора можно найти его массу (что и поставлено в вопросе задачи). Масса хлора рассчитывается как произведение количества вещества хлора на его молярную массу (молекулярная масса 1 моль хлора; молекулярная масса рассчитывается с помощью таблицы химических элементов Д.И. Менделеева). Масса хлора будет равна: m(Cl 2) = v(Cl 2)×M(Cl 2) m(Cl 2) = 0,5×71 = 35,5 г |
| Ответ | Масса хлора равна 35,5 г |


