Una dintre cele mai importante generalizări în imunologie sfârşitul secolului al XX-lea şi începutul secolului al XXI-lea. a fost crearea unei doctrine bazate științific despre imunitatea congenitală (din engleză innate immunity) sau naturală, naturală și adaptativă (din engleză adaptive immunity) sau adaptivă, dobândită imunitate (din engleză acquired immunity). În practica imunologică, termenii de imunitate „înnăscută” și „adaptativă”, componente înnăscute și adaptative sunt adesea folosiți. sistem imunitar, răspunsul imun înnăscut și adaptativ. Ambele tipuri de imunitate se realizează prin factori celulari și umorali. Termeni precum „imunitate nespecifică”, „reactivitate imunologică nespecifică” și altele asemenea sunt de domeniul trecutului.
Imunitatea înnăscută și dobândită reprezintă două părți care interacționează ale unui sistem care asigură dezvoltarea unui răspuns imun la substanțele străine genetic.
Imunitatea înnăscută- un sistem ereditar de protecție a organismelor multicelulare împotriva oricăror microorganisme patogene și nepatogene, precum și a produselor endogene ale distrugerii țesuturilor.
Ca cel mai devreme forma apărării imune a organismului, s-a format imunitatea înnăscută pe etapele inițiale evoluția organismelor pluricelulare, până la apariția capacității de a rearanja genele imunoglobulinei și TCR, precum și posibilitatea recunoașterii memoriei imunitare „proprie” și cu drepturi depline. Dovadă în acest sens este prezența diferitelor gene de apărare înnăscute la animalele și plantele nevertebrate. Se știe că nevertebratele (de exemplu, artropodele) au elemente celulare, care au o funcție fagocitară, și factori umorali precum peptidele antimicrobiene, lectinele etc., care recunosc și atacă cu succes microorganismele patogene. Toate aceste componente sunt conservatoare, moștenite și nu sunt supuse modificărilor genetice în timpul vieții.
Sunt caracterizate principalele trăsături distinctive semne sisteme imunitatea înnăscută.
Imunitatea înnăscută asigură recunoașterea și eliminarea agenților patogeni în primele minute sau ore de la intrarea lor în organism, când mecanismele imunității adaptative sunt încă absente.
Funcția sistemului imunitar înnăscut realizat printr-o varietate de elemente celulare (macrofage, DC, neutrofile, mastocite, eozinofile, bazofile, celule NK, celule NKT, unele celule non-hematopoietice) și factori umorali (anticorpi naturali, citokine, complement, proteine de fază acută, cationice). peptide antimicrobiene, lizozimă etc.).
Celulele sistemului imunitar înnăscut:
nu formează clone. Lipsa clonalității în organizarea sistemului imunitar înnăscut este una dintre principalele sale diferențe față de sistemul imunitar adaptativ. În acest sens, fiecare celulă a imunității înnăscute acționează individual, în timp ce cu un răspuns imun adaptativ, toate celulele dintr-o clonă (comunitate) sunt supuse unui singur program determinat genetic;
nu sunt supuse selecției negative și pozitive;
participa la reacțiile de fagocitoză, citoliză, inclusiv bacterioliză, neutralizare, producție de citokine etc.
Recunoaştere agenți patogeni de către celulele sistemului imunitar înnăscut se realizează prin numeroase structuri de receptor, precum receptorii scavenger (receptori scavenger), receptorii de manoză, receptorii de complement (CRl, CR3, CR4), receptorii de lectină etc. Grup special Receptorii imuni înnăscuți sunt așa-numiții receptori de recunoaștere a modelelor (PRR).
Ei recunosc conservatori, structuri comune multor tipuri de microorganisme, așa-numitele Pathogen-Associated Molecular Patterns (PAMP). În prezent, sunt studiate intens structura și funcțiile receptorilor imunitari înnăscuți, cum ar fi receptorii Toll-like (TLR), NOD-1, NOD-2, RIG etc.. Receptorii sistemului imunitar înnăscut sunt conservați evolutiv.
Receptorii de taxare descoperit pentru prima dată în Drosophila. Receptorii Toll-like (TLR) la mamifere au o structură și o funcție similară. Receptorii acestei familii sunt larg reprezentați pe celule diferite sistemul imunitar (monocite, DC, leucocite etc.), precum și pe multe celule ale corpului (fibroblaste, endoteliu, epiteliu, cardiomiocite etc.). Sistemul TLR este discutat mai detaliat mai jos.
Factori ai imunității înnăscute nu se modifică în timpul vieții organismului, sunt controlate de genele liniei germinale și sunt moștenite.
Activarea imunității înnăscute nu formează memoria imunitară pe termen lung, ci servește condiție prealabilă dezvoltarea răspunsului imun adaptativ.
Toate aceste funcții sunt extrem de importante pentru protecția împotriva microorganismelor patogene, dar sunt insuficiente pentru viața organismelor multicelulare foarte organizate, cum ar fi vertebratele. În ei, în procesul de evoluție, au apărut noi componente imunitare și s-a format un sistem imunitar, a cărui funcție principală a fost controlul constanței genetice a mediului intern al unui organism multicelular. Sistemul imunitar s-a confruntat cu sarcina de a-și recunoaște și a-și aminti „al său”. Tot ceea ce este „sine” antigenic trebuie păstrat și tot ceea ce este „străin” antigenic trebuie îndepărtat din organism. În contextul diversității de milioane de dolari a structurilor antigenice străine, este imposibil să te descurci cu un set mic de gene transmise prin moștenire (așa-numitele gene ale liniei germinale).
Sistemul imunitar general uman este împărțit în două subsisteme mari - imunitatea naturală înnăscută nespecifică și imunitatea specifică (adaptativă) dobândită. Să ne dăm seama ce este imunitatea înnăscută cum funcționează și de ce o persoană are nevoie de el. La nastere, copilul intra intr-un mediu diferit de viata intrauterina sterila. Chiar dacă sunt respectate toate regulile de asepsie și antisepsie, literalmente din prima secundă de viață este supus atacului microorganismelor. Cu toate acestea, bebelușul nu se îmbolnăvește în momentul nașterii! De ce se întâmplă asta? Totul este despre imunitatea înnăscută, care poate proteja un nou-născut de pericolul infecției. Imunitatea înnăscută este persistentă, este moștenită, ceea ce este asociat cu proprietățile biologice ale organismului. De exemplu, animalele nu suferă de boli venerice umane, iar oamenii nu suferă de pesta bovină. Sistemul imunitar înnăscut creează o barieră puternică împotriva pătrunderii bacteriilor, virușilor, ciupercilor și așa mai departe în organism.
Celulele fagocitare
Imunitatea înnăscută asigură 60% din apărarea totală a corpului nostru. Asigură recunoașterea și eliminarea agenților patogeni în primele minute sau ore de la intrarea în organism. Imunitatea înnăscutăîncepe să se formeze la mijlocul primului trimestru de sarcină cu fagocite. Fagocitele sunt celule care sunt capabile să înghită organisme străine. Ei „cresc” din celule stem și sunt supuși unui „antrenament” în splină, datorită căruia pot distinge ulterior între ei și ceilalți. Celulele fagocitare de obicei circulă în tot corpul în căutarea unor materiale străine, dar pot fi chemați într-o anumită locație de către citokine. Fagocitoza este o caracteristică importantă a componentei celulare a imunității înnăscute și, după toate probabilitățile, reprezintă cea mai uniforma veche protecția organismului, deoarece fagocitele se găsesc atât la vertebrate, cât și la nevertebrate.
Factori ai imunității înnăscute
Imunitatea înnăscută- Aceasta este capacitatea înnăscută de a distruge tot ce este străin corpului. Este prima linie de apărare a organismului mamiferelor împotriva tumorilor și a bolilor infecțioase. Principala barieră externă de protecție care împiedică pătrunderea microorganismelor în corpul uman este pielea și mucoasele. Proprietățile protectoare ale pielii sunt, în primul rând, impermeabilitatea acesteia ( barieră fizică) și prezența inhibitorilor de microorganisme la suprafață (acid lactic și acizi grași în transpirație și secreții glande sebacee, pH scăzut de suprafață). Membrana mucoasă are un mecanism de apărare multicomponent. Mucusul secretat de celulele sale împiedică microorganismele să se atașeze de el, iar mișcarea cililor ajută la „măturarea” substanțelor străine din tractul respirator. Lacrimile, saliva și urina îndepărtează în mod activ substanțele străine de pe membranele mucoase. Multe fluide secretate de organism au proprietăți bactericide specifice. De exemplu, acid clorhidric stomac, spermină și zinc în material seminal, lactoperoxidază în laptele matern și lizozim în multe secreții externe (nazal, lacrimi, bilă, conținut duodenal, lapte matern etc.) au proprietăți bactericide puternice. Unele enzime au, de asemenea, un efect bactericid, de exemplu, hialuronidază, α1-antitripsină, lipoproteinază.
Celulele imune înnăscute
Celulele imune înnăscute nu formează clone. Fiecare celulă a sistemului imunitar înnăscut acționează individual. Factorii imunității înnăscute nu se modifică în timpul vieții organismului, sunt controlați de genele liniei germinale și sunt moșteniți. Celulele imune înnăscute, celulele NK sau celulele ucigașe naturale, sunt capabile să omoare o gamă largă de celule - de la celule infectate cu virus până la celule tumorale. O scădere a activității celulelor NK și o scădere a numărului de celule din populația de celule NK sunt asociate cu dezvoltarea și progresia rapidă a unor boli precum cancerul, hepatita virală, SIDA, sindromul de oboseală cronică, sindromul imunodeficienței și o serie de boală autoimună. O serie de studii au arătat că niveluri scăzute Populația de celule NK se corelează cu răspândirea mai rapidă a tumorilor, cu o durată de viață mai scurtă a pacienților și cu o mortalitate mai mare. O creștere a activității funcționale a celulelor natural killer este direct legată de manifestarea efectelor antivirale și antitumorale. Căutarea de medicamente care să mărească activitatea acestei părți a sistemului imunitar înnăscut pare promițătoare din punct de vedere strategic pentru dezvoltare. medicamente antivirale spectru larg de acțiune. Prin urmare, oamenii de știință de frunte din întreaga lume sunt ocupați să caute astfel de medicamente. Între timp, un astfel de medicament există deja, dar mai multe despre asta mai jos.
Stimulatori ai celulelor imune înnăscute
Din păcate, în aproape jumătate din populația planetei noastre, nivelul celulelor NK este semnificativ mai scăzut decât în mod normal. Această afecțiune se numește imunodeficiență. Imunodeficiența duce la boli infecțioase mai frecvente și este cauza unei morbidități și mortalități mai mari prin cancer. Prin urmare, astăzi este nevoie urgentă de mijloace care să stimuleze creșterea numărului și a activității funcționale a NK și, astfel, să conducă la eliminarea imunodeficienței și să ajute la întărirea sistemului imunitar.  În aceste scopuri, în practică sunt utilizați imunomodulatorii și adaptogenii. Cu toate acestea, activitatea lor nu este suficient de mare. S-a stabilit recent că cei mai activi stimulatori ai funcției celulelor NK sunt așa-numitele proteine factor de transfer, care sunt conținute în leucocitele din sânge și, după cum se dovedește, în colostrul vacilor, caprelor și gălbenușului de ou. Aceste proteine au o activitate imunostimulatoare de 4-5 ori mai mare în comparație cu imunomodulatorii activi cunoscuți utilizați în medicina practică. Și datorită disponibilității sursei factorilor de transfer, se deschide posibilitatea obținerii acesteia în cantități nelimitate. Compania 4Life, inspirată de posibilitățile factorilor de transfer, a început să fie prima care a produs medicamentul Transfer Factor, care se bazează pe factori de transfer din colostrul de vacă și gălbenușurile de ou. Absorbiți în sânge, factorii de transfer se grăbesc către molecula de ADN, o verifică dacă nu este deteriorată și îi restabilesc integritatea datorită informațiilor conținute în ei. Rezultatul este depanarea tuturor proceselor imunitare. Cu alte cuvinte, după ce a luat Transfer Factor, sistemul imunitar însuși începe să înțeleagă când, cum și cum să reacționeze la acest sau acel tip de pericol. Astăzi puteți cumpăra Transfer Factor în Ucraina, pentru a face acest lucru trebuie doar să ne sunați sau să completați un formular de comandă special.
În aceste scopuri, în practică sunt utilizați imunomodulatorii și adaptogenii. Cu toate acestea, activitatea lor nu este suficient de mare. S-a stabilit recent că cei mai activi stimulatori ai funcției celulelor NK sunt așa-numitele proteine factor de transfer, care sunt conținute în leucocitele din sânge și, după cum se dovedește, în colostrul vacilor, caprelor și gălbenușului de ou. Aceste proteine au o activitate imunostimulatoare de 4-5 ori mai mare în comparație cu imunomodulatorii activi cunoscuți utilizați în medicina practică. Și datorită disponibilității sursei factorilor de transfer, se deschide posibilitatea obținerii acesteia în cantități nelimitate. Compania 4Life, inspirată de posibilitățile factorilor de transfer, a început să fie prima care a produs medicamentul Transfer Factor, care se bazează pe factori de transfer din colostrul de vacă și gălbenușurile de ou. Absorbiți în sânge, factorii de transfer se grăbesc către molecula de ADN, o verifică dacă nu este deteriorată și îi restabilesc integritatea datorită informațiilor conținute în ei. Rezultatul este depanarea tuturor proceselor imunitare. Cu alte cuvinte, după ce a luat Transfer Factor, sistemul imunitar însuși începe să înțeleagă când, cum și cum să reacționeze la acest sau acel tip de pericol. Astăzi puteți cumpăra Transfer Factor în Ucraina, pentru a face acest lucru trebuie doar să ne sunați sau să completați un formular de comandă special.
Întărirea imunității. Cu toate acestea, puțini dintre noi știu că conceptul de sistem imunitar are propriile sale tipuri și caracteristici. Ce este imunitatea umană? Să ne dăm seama împreună.
O oarecare terminologie
Acest concept ascunde capacitatea organismului de a preveni activitatea bacteriilor, toxinelor și a altor substanțe dăunătoare. Medicii fac distincție între astfel de tipuri de imunitate ca înnăscute și dobândite, care, la rândul lor, sunt împărțite în alte forme, despre care vom vorbi puțin mai târziu.
Sarcina principală a sistemului imunitar al organismului este de a menține sănătatea și funcționarea normală a tuturor organelor și sistemelor umane. Astfel, imunitatea joacă rolul unei bariere protectoare de care ne desparte mediu inconjurator. Să aruncăm o privire mai atentă asupra tipurilor și formelor de funcții de protecție ale corpului uman.
Imunitatea înnăscută
Acest tip de protecție este asociat cu caracteristicile corpului care sunt moștenite la naștere. Funcționarea imunității înnăscute este asigurată de mulți factori celulari și necelulari (așa-zișii). De exemplu, pielea și membranele mucoase sunt o barieră de încredere pentru majoritatea microbilor. Corpul este, de asemenea, protejat de sudoare, sebacee, glandele salivare. Substanțele pe care le eliberează sunt dăunătoare pentru majoritatea bacterii patogene. Microflora intestinală normală conține microorganisme care sunt inamici naturali ai multor agenți patogeni. De asemenea, luptă împotriva infecțiilor din tractul digestiv suc gastric, enzime și bilă.
Apărarea naturală a organismului este foarte puternică. Dar dușmanii săi - microorganismele, moleculele și celulele străine - încearcă în mod constant să pătrundă în interior, perturbând integritatea barierelor sau secreția normală a organelor și sistemelor - scăzând imunitatea naturală. Factorii provocatori într-o astfel de situație sunt hipotermia sau stresul, lipsa de vitamine sau medicamente, dezechilibrul hormonal sau intervenție chirurgicală. În acest caz, pătrunderea microorganismelor în organism este mult facilitată. Dar aici intră în vigoare un alt tip de apărare a corpului. Vom vorbi despre asta în detaliu mai târziu.
Imunitatea dobândită
Dacă un agent străin a pătruns în bariera naturală în fluxul sanguin al corpului, atunci pot apărea mai multe opțiuni pentru relația dintre sistemul imunitar și bacterii, dintre care una este o boală infecțioasă. În acest caz, este activată imunitatea dobândită, care va lupta împotriva infecției în viitor.
Principala caracteristică a acestui tip de imunitate este producerea de anticorpi specifici împotriva unui anumit antigen. Se formează în timpul vieții unei persoane și nu este moștenit. Unicitatea imunității dobândite constă în faptul că, în funcție de bolile suferite, aceasta se modifică, producând noi anticorpi. Acest tip de funcții de protecție ale organismului pot fi naturale sau dobândite artificial. Să luăm în considerare aceste forme de imunitate în detaliu.
Dacă apare o barieră imunitară protectoare după boală trecută, se numește imunitate naturală dobândită. După un atac al agenților patogeni, organismul însuși produce anticorpi. Uneori, acestea protejează organismul de reinfecție timp de săptămâni și luni (cu gripă, ARVI) și poate chiar pentru ani lungi sau pe tot parcursul vieții, ca în cazul rujeolei sau scarlatinei (această imunitate se numește persistentă).
Când unei persoane i se injectează agenți patogeni slăbiți care provoacă un răspuns imunitar în organism, vorbim despre imunitatea activă dobândită artificial. Dacă în organism sunt introduși anticorpi gata preparate, apare imunitatea pasivă, ceea ce vă permite să protejați o persoană care a avut contact cu pacientul în cel mai scurt timp posibil. Dar această formă a funcțiilor de protecție ale corpului este mai slabă în comparație cu tipul activ de barieră imunitară dobândită.
Un reprezentant izbitor al imunității pasive este copilul nou-născut. În timp ce este încă în uter, bebelușul primește prin placentă anticorpi împotriva agenților patogeni ai bolilor de care suferea mama. Până la 3-6 luni de viață, acest tip de imunitate slăbește, iar la sfârșitul primului an de viață dispare complet. Dar poate fi întărită prin practicarea alăptării.
Rezumând toate cele de mai sus, putem concluziona că imunitatea este un sistem destul de complex care necesită ajutor extern constant sub formă de vaccinare, respectarea regulilor de igienă, mâncat sănătosȘi activitate fizica. Adică, pentru a fi sănătos, trebuie doar să respectați aceste reguli.
9.1. Introducere în imunologie9.1.1. Principalele etape ale dezvoltării imunologiei
Fiecare persoană de pe planetă (cu excepția gemenilor identici) are caracteristici unice determinate genetic ale biopolimerilor din care este construit corpul său. Cu toate acestea, corpul său trăiește și se dezvoltă în contact direct cu reprezentanți ai naturii vii și neînsuflețite și diverse molecule bioorganice de origine naturală sau artificială care au activitate biologică. La intrarea în corpul uman, deșeurile și țesuturile altor persoane, animale, plante, microbi, precum și molecule străine pot interfera și perturba procesele biologice, reprezentând o amenințare pentru viața unui individ. Trăsătură distinctivă dintre acești agenți este străinătatea genetică. Adesea, astfel de produse se formează în interiorul corpului uman ca urmare a activității sintetice a microflorei care locuiește în noi, a mutațiilor celulare și a diferitelor modificări ale macromoleculelor din care suntem construiți.
Pentru a proteja împotriva intervențiilor nedorite și distructive, evoluția a creat reprezentanți ai naturii vii sistem special contraacțiune, al cărei efect cumulativ a fost desemnat ca imunitate(din lat. immunitas- eliberare de ceva, inviolabilitate). Acest termen a fost folosit deja în Evul Mediu pentru a desemna, de exemplu, scutirea de la plata impozitelor, iar mai târziu - inviolabilitatea unei misiuni diplomatice. Sensul acestui termen corespunde exact sarcinilor biologice pe care evoluția le-a determinat în raport cu imunitatea.
Principalele sunt recunoașterea diferenței genetice dintre structurile intervenționist și propriile sale și eliminarea influenței acesteia asupra proceselor biologice care au loc în organism folosind un set de reacții și mecanisme speciale. Scopul final al sistemului imunitar este păstrarea homeostaziei, integrității structurale și funcționale și a individualității genetice atât a unui organism individual, cât și a speciei în ansamblu, precum și dezvoltarea mijloacelor de prevenire a unor astfel de intervenții în viitor.
În consecință, imunitatea este o modalitate de protejare a organismului de substanțe străine genetic de origine exogenă și endogenă, având ca scop menținerea și păstrarea homeostaziei, a integrității structurale și funcționale a organismului și a individualității genetice a fiecărui organism și specie în ansamblu.
Imunitatea ca fenomen biologic general și general medical, structurile sale anatomice și mecanismele de funcționare în organism sunt studiate de o știință specială - imunologia. Această știință a apărut acum mai bine de 100 de ani. Pe măsură ce cunoștințele umane au progresat, opiniile asupra imunității, rolul său în organism și mecanismele reacțiilor imune s-au schimbat, domeniul de aplicare practică a realizărilor imunologiei sa extins și, în conformitate cu aceasta, însăși definiția imunologiei ca știință sa schimbat. . Imunologia este adesea interpretată ca o știință care studiază imunitatea specifică față de agenții patogeni ai bolilor infecțioase și dezvoltă metode de protecție împotriva acestora. Aceasta este o viziune unilaterală care nu oferă o înțelegere cuprinzătoare și cuprinzătoare a științei, bazată pe esența și mecanismele imunității și rolul acesteia în viața corpului. Pe scena modernă dezvoltarea doctrinei imunității, imunologia poate fi definită ca o știință generală biologică și medicală generală care studiază metodele și mecanismele de protecție a organismului de substanțele străine genetic de origine exogenă și endogenă în scopul menținerii homeostaziei, integrității structurale și funcționale a corpul și individualitatea genetică a unui individ și a speciei în ansamblu. Această definiție subliniază că imunologia ca știință este unificată indiferent de obiectul de studiu: oameni, animale sau plante. Desigur, baza anatomică și fiziologică, un set de mecanisme și reacții, precum și metode de protecție împotriva antigenelor la reprezentanții animalelor
Și floră va varia, dar esența fundamentală a imunității nu se va schimba. În imunologie, există trei domenii: imunologie medicală (homoimunologie), zooimunologie și fitoimunologie, care studiază imunitatea la om, respectiv la animale și respectiv la plante, iar în fiecare dintre ele - generală și specifică. Una dintre cele mai importante secțiuni ale sale este imunologia medicală. Astăzi, imunologia medicală rezolvă probleme atât de importante precum diagnosticul, prevenirea și tratamentul bolilor infecțioase (imunoprevenire sau vaccinologie), afecțiunilor alergice (alergologie), tumori maligne(imuno-oncologie), boli în mecanismul cărora procesele imunopatologice joacă un rol (imunopatologie), relațiile imune dintre mamă și făt în toate etapele reproducerii (imunologia reproducerii), studiază mecanismele imune și aduce o contribuție practică la rezolvarea problemei de transplant de organe și țesuturi (imunologia transplantului); Se mai pot distinge imunohematologia, care studiază relația dintre donator și primitor în timpul transfuziei de sânge, imunofarmacologia, care studiază efectul asupra proceselor imune. substante medicinale. ÎN anul trecut s-au distins imunologia clinică și de mediu. Imunologia clinică studiază și dezvoltă problemele de diagnostic și tratament al bolilor apărute ca urmare a imunodeficiențelor congenitale (primare) și dobândite (secundar), iar imunologia mediului are influență asupra sistemului imunitar de toate tipurile. factori de mediu(climat-geografice, social, profesional etc.).
Cronologic, imunologia ca știință a trecut deja prin două perioade mari (Ulyankina T.I., 1994): perioada protoimunologiei (de la perioada antica până în anii 80 ai secolului al XIX-lea), asociată cu cunoașterea spontană, empirică, a reacțiilor de apărare ale organismului și perioada apariției imunologiei experimentale și teoretice (din anii 80 ai secolului al XIX-lea până în al doilea deceniu al secolului al XX-lea). În a doua perioadă, formarea imunologiei clasice, care era în principal în natura imunologiei infecțioase, a fost finalizată. De la mijlocul secolului al XX-lea, imunologia a intrat în a treia perioadă, genetică moleculară, care continuă până în zilele noastre. Această perioadă este caracterizată de dezvoltarea rapidă a imunologiei moleculare și celulare și a imunogeneticii.
Prevenirea variolei prin inocularea oamenilor cu variola bovină a fost propusă în urmă cu mai bine de 200 de ani doctor englez E. Jenner, însă, această observație a fost pur empirică. Prin urmare, chimistul francez L. Pasteur, care a descoperit principiul vaccinării, și zoologul rus I.I. sunt considerați pe bună dreptate fondatorii imunologiei științifice. Mechnikov este autorul doctrinei fagocitozei și biochimistul german P. Ehrlich, care a formulat ipoteza anticorpilor. În 1888, pentru serviciile deosebite ale lui L. Pasteur aduse omenirii, s-a înființat cu donații publice Institutul de Imunologie (acum Institutul Pasteur), care era o școală în jurul căreia se grupau imunologi din multe țări. Oamenii de știință ruși au participat activ la formarea și dezvoltarea imunologiei. De mai bine de 25 de ani I.I. Mechnikov a fost director adjunct pentru știință la Institutul Pasteur, adică. a fost cel mai apropiat asistent al lui și persoană cu gânduri asemănătoare. Mulți oameni de știință ruși remarcabili au lucrat la Institutul Pasteur: M. Bezredka, N.F. Gamaleya, L.A. Tarasovici, G.N. Gabrichevsky, I.G. Savcenko, S.V. Korshun, D.K. Zabolotny, V.A. Barykin, N.Ya. și F.Ya. Chistovichi și mulți alții. Acești oameni de știință au continuat să dezvolte tradițiile lui Pasteur și Mechnikov în imunologie și, în esență, au creat școala rusă de imunologi.
Oamenii de știință ruși dețin multe descoperiri remarcabileîn domeniul imunologiei: I.I. Mechnikov a pus bazele doctrinei fagocitozei, V.K. Vysokovych a fost unul dintre primii care a formulat rolul sistemului reticuloendotelial în imunitate, G.N. Gabrichevsky a descris fenomenul de chemotaxie a leucocitelor, F.Ya. Chistovici a stat la originile descoperirii antigenelor tisulare, M. Raisky a stabilit fenomenul revaccinării, adică. memorie imunologică, M. Saharov - unul dintre fondatorii doctrinei anafilaxiei, academician. LA. Zilber a stat la originile doctrinei antigenelor tumorale, academician. P.F. Zdrodovsky a fundamentat direcția fiziologică în imunologie, academician. R.V. Petrov a avut o contribuție semnificativă la dezvoltarea imunologiei non-infecțioase.
Oamenii de știință ruși sunt pe drept lideri în dezvoltarea problemelor fundamentale și aplicate ale vaccinologiei și imunoprofilaxiei în general. Numele creatorilor de vaccinuri împotriva tularemiei (B.Ya. Elbert și N.A. Gaisky) sunt bine cunoscute în țara noastră și în străinătate. antrax(N.N. Ginzburg), poliomielita-
lita (M.P. Chumakov, A.A. Smorodintsev), rujeolă, oreion, gripă (A.A. Smorodintsev), febră Q și tifos (P.F. Zdrodovsky), polianatoxine împotriva infecțiilor rănilor și botulismului (A A. Vorobyov, G. V. oamenii de știință au participat activ la dezvoltarea vaccinurilor și a altor medicamente imunobiologice, strategii și tactici de imunoprofilaxie, eliminarea globală și reducerea bolilor infecțioase. În special, din inițiativa lor și cu ajutorul lor, variola a fost eradicată de pe glob (V.M. Zhdanov, O.G. Andzhaparidze), poliomielita a fost eradicată cu succes (M.P. Chumakov, S.G. Drozdov).
Într-o perioadă istorică relativ scurtă, imunologia a obținut rezultate semnificative în reducerea și eliminarea bolilor umane, păstrarea și menținerea sănătății oamenilor de pe planeta noastră.
9.1.2. Tipuri de imunitate
Abilitatea de a recunoaște structuri străine și de a-și proteja propriul corp de invadatori s-a format destul de devreme. Organismele inferioare, în special nevertebratele (bureți, celenterate, viermi), au deja sisteme elementare de protecție împotriva oricăror substanțe străine. Corpul uman, ca toate animalele cu sânge cald, are deja un sistem complex de contracarare a agenților străini genetic. Cu toate acestea, structura anatomică, funcțiile fiziologice și reacțiile care asigură o astfel de protecție la anumite specii de animale, la oameni și organisme inferioareîn conformitate cu nivelul de dezvoltare evolutivă diferă semnificativ.
Astfel, fagocitoza și inhibarea alogenă, ca una dintre reacțiile filogenetice timpurii de apărare, sunt inerente tuturor organismelor multicelulare; celulele asemănătoare leucocitelor diferențiate care îndeplinesc funcțiile imunității celulare apar deja în celenterate și moluște; în ciclostomi (lamrey) apar rudimente de timus, limfocite T, imunoglobuline și se notează memoria imună; peștii au deja organe limfoide tipice animalelor superioare - timusul și splina, celulele plasmatice și anticorpii de clasa M; păsările au autoritatea centrală imunitate sub forma unei burse de Fabricius, au capacitatea de a reacționa sub formă de hipersensibilitate imediat
tip nou. În cele din urmă, la mamifere sistemul imunitar ajunge la maximum nivel inalt dezvoltare: se formează sistemele T, B și A celule ale sistemului imunitar, apare interacțiunea lor de cooperare, apare capacitatea de a sintetiza imunoglobuline de diferite clase și forme de răspuns imun.
În funcție de nivelul de dezvoltare evolutivă, de caracteristicile și complexitatea sistemului imunitar format și de capacitatea acestuia din urmă de a răspunde cu anumite reacții la antigene, în imunologie se obișnuiește să se distingă tipuri separate de imunitate.
Astfel, a fost introdus conceptul de imunitate înnăscută și dobândită (Fig. 9.1). Imunitatea înnăscută sau de specie, cunoscută și ca ereditară, genetică, constituțională, este imunitatea moștenită, fixată genetic, a indivizilor unei anumite specii față de orice agent străin dezvoltat în procesul de filogeneză. Un exemplu este imunitatea umană la anumiți agenți patogeni, inclusiv cei care sunt deosebit de periculoși pentru animalele de fermă (pesta bovină, boala Newcastle, care afectează păsările, variola calului etc.) și insensibilitatea umană la bacteriofagi care infectează celulele bacteriene. Imunitatea speciei poate fi explicată din diferite poziții: incapacitatea unui agent străin de a adera la celule și molecule țintă care determină inițierea procesului patologic și activarea sistemului imunitar, distrugerea sa rapidă de către enzimele macroorganismului și absența condiţiile de colonizare a macroorganismului.
Imunitatea speciei poate fi absolutȘi relativ. De exemplu, broaștele care sunt insensibile la toxina tetanosă răspund la administrarea acesteia atunci când temperatura corpului lor crește. Animalele de laborator care sunt insensibile la orice agent străin reacționează la acesta pe fondul introducerii imunosupresoarelor sau al îndepărtării organului central al imunității - timusul.
Imunitatea dobândită este imunitatea la un agent străin dintr-un corp uman sau animal care este sensibil la acesta, dobândită în procesul de dezvoltare individuală, adică. dezvoltarea individuală a fiecărui individ. Baza sa este potențialul de protecție imunitară, care se realizează numai atunci când este necesar și în anumite condiții. Imunitatea dobândită, sau mai degrabă rezultatul său final, nu este moștenită în sine (spre deosebire, desigur, de potență); este o experiență individuală de-a lungul vieții.
Orez. 9.1. Clasificarea tipurilor de imunitate
Distinge naturalȘi artificial imunitatea dobândită. Un exemplu de imunitate naturală dobândită la om este imunitatea la infecția care apare după o istorie de boală infecțioasă(așa-numita imunitate post-infecțioasă), de exemplu după scarlatina. Imunitatea dobândită artificială este creată în mod deliberat pentru a crea imunitate în organism
la un agent specific prin introducerea de preparate imunobiologice speciale, de exemplu vaccinuri, seruri imune, celule imunocompetente (vezi capitolul 14).
Imunitatea dobândită poate fi activȘi pasiv. Imunitate activă datorită implicării directe a sistemului imunitar în procesul de formare a acestuia (de exemplu, post-vaccinare, imunitatea post-infecțioasă). Imunitate pasivă se formează prin introducerea în organism a imunoreactivilor gata preparate care pot oferi protecția necesară. Aceste medicamente includ anticorpi (preparate de imunoglobuline și seruri imune) și limfocite. Imunitatea pasivă se formează la făt în perioada embrionară datorită pătrunderii anticorpilor materni prin placentă, iar în timpul alăptării - când copilul absoarbe anticorpii conținuti în lapte.
Deoarece celulele sistemului imunitar și factorii umorali participă la formarea imunității, este acceptat imunitate activă se diferențiază în funcție de ce componentă a răspunsului imun joacă rolul principal în formarea protecției împotriva antigenului. În acest sens, există o distincție umoral, celular imunitate. Un exemplu de imunitate celulară este imunitatea de transplant, când rolul principal în imunitate este jucat de limfocitele T ucigașe citotoxice. Imunitatea în timpul infecțiilor toxinemice (difterie) și intoxicațiilor (tetanos, botulism) se datorează în principal anticorpilor (antitoxine).
În funcție de direcția imunității, i.e. natura agentului străin, emit antitoxic, antiviral, antifungic, antibacterian, antiprotozoar, transplant, antitumoralși alte tipuri de imunitate.
Imunitatea poate fi menținută sau menținută fie în absența, fie numai în prezența unui agent străin în organism. În primul caz, un astfel de agent joacă rolul unui factor declanșator, iar imunitatea este numită steril, in secunda - Nesterile. Un exemplu de imunitate sterilă este imunitatea post-vaccinare cu introducerea vaccinurilor ucise, iar imunitatea nesterilă este imunitatea la tuberculoză, care este menținută prin prezența constantă a Mycobacterium tuberculosis în organism.
Imunitatea poate fi sistemică acestea. generalizat, răspândindu-se pe tot corpul și local, la care
Se observă o rezistență mai pronunțată a organelor și țesuturilor individuale. De regulă, luând în considerare caracteristicile structura anatomicăși organizarea funcționării, conceptul de „imunitate locală” este folosit pentru a se referi la rezistența membranelor mucoase (de aceea se numește uneori mucoase) și piele. Această diviziune este, de asemenea, condiționată, deoarece în procesul de dezvoltare a imunității aceste tipuri de imunitate se pot transforma unele în altele.
9.2. Imunitatea înnăscută
Congenital(specie, genetică, constituțională, naturală, nespecifică) imunitate- aceasta este rezistența la agenți infecțioși (sau antigene) dezvoltată în procesul de filogeneză, moștenită și inerentă tuturor indivizilor aceleiași specii.
Principala caracteristică a factorilor și mecanismelor biologice care asigură o astfel de rezistență este prezența în organism a efectorilor gata pregătiți (preformați), care sunt capabili să asigure distrugerea agentului patogen rapid, fără reacții pregătitoare îndelungate. Ele constituie prima linie de apărare a organismului împotriva agresiunii microbiene sau antigenice externe.
9.2.1. Factori ai imunității înnăscute
Dacă luăm în considerare traiectoria unui microb patogen în dinamica procesului infecțios, este ușor de observat că organismul își construiește diverse linii de apărare pe această cale (Tabelul 9.1). În primul rând, este epiteliul tegumentar al pielii și mucoaselor, care are rezistență la colonizare. Dacă agentul patogen este înarmat cu factori invazivi corespunzători, atunci acesta pătrunde în țesutul subepitelial, unde se dezvoltă o reacție inflamatorie acută, limitând agentul patogen la poarta de intrare. Următoarea stație pe calea agentului patogen sunt ganglionii limfatici regionali, unde este transportat de limfă prin vase limfatice, drenând țesutul conjunctiv. Vasele și ganglionii limfatici răspund la penetrare prin dezvoltarea limfangitei și limfadenitei. După depășirea acestei bariere, microbii pătrund în sânge prin vasele limfatice eferente - ca răspuns, se poate dezvolta un răspuns inflamator sistemic.
veterinar. Dacă microbul nu moare în sânge, atunci se răspândește hematogen în organele interne - se dezvoltă forme generalizate de infecție.
Tabelul 9.1. Factori și mecanisme ale imunității antiinfecțioase (principiul eșalonării apărării antimicrobiene conform Mayansky A.N., 2003)
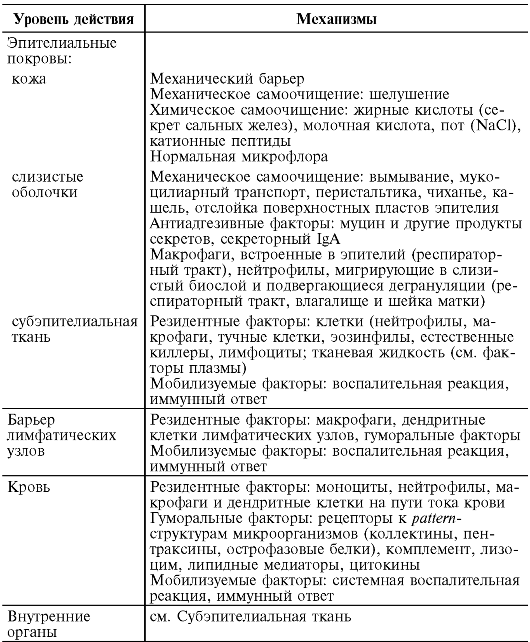 Factorii ai imunității înnăscute includ:
Factorii ai imunității înnăscute includ:
Piele și mucoase;
Factori celulari: neutrofile, macrofage, celule dendritice, eozinofile, bazofile, celule natural killer;
Factori umorali: sistemul de complement, receptori solubili pentru structurile de suprafață ale microorganismelor (structuri de tipar), peptide antimicrobiene, interferoni.
Piele și mucoase. Stratul subțire de celule epiteliale care căptușește suprafața pielii și a membranelor mucoase este o barieră care este practic impenetrabilă pentru microorganisme. Separă țesuturile sterile ale corpului de lumea exterioară microbiană.
Piele acoperit cu epiteliu scuamos multistrat, în care se disting două straturi: cornos și bazal.
Keratinocitele stratului cornos sunt celule moarte care sunt rezistente la compuși chimici agresivi. Nu există receptori pe suprafața lor pentru moleculele adezive ale microorganismelor, prin urmare au o rezistență semnificativă la colonizare și reprezintă cea mai sigură barieră pentru majoritatea bacteriilor, ciupercilor, virușilor și protozoarelor. Excepția este S. aureus, Pr. acnee, I. pestis, si cel mai probabil patrund fie prin microfisuri, fie cu ajutorul insectelor suge de sange, fie prin gura glandelor sudoripare si sebacee. Gura glandelor sebacee și sudoripare, foliculii de păr din piele sunt cei mai vulnerabili, deoarece aici stratul de epiteliu keratinizat devine mai subțire. În protejarea acestor zone, un rol important joacă produsele sudoripare și glandelor sebacee, care conțin acizi lactici și grași, enzime și peptide antibacteriene care au efect antimicrobian. În gurile anexelor pielii se află microflora rezidentă profundă, formând microcolonii și producând factori de protecție (vezi capitolul 4).
Pe lângă keratinocite, epiderma mai conține două tipuri de celule - celule Langerhans și celule Greenstein (epidermocite procesate, constituind 1-3% din cariocitele stratului bazal). Celulele Langerhans și Greenstein sunt de origine mieloidă și aparțin celulelor dendritice. Se presupune că aceste celule sunt opuse în funcție. Celulele Langerhans sunt implicate în prezentarea antigenului și induc un răspuns imun, iar celulele Greenstein produc citokine care suprimă răspunsul imun.
reacții mune la nivelul pielii. Keratinocitele și celulele dendritice tipice ale epidermei, împreună cu structurile limfoide ale dermei, participă activ la reacțiile imunității dobândite (vezi mai jos).
Pielea sănătoasă are capacitate mare spre autopurificare. Acest lucru este ușor de demonstrat dacă aplicați bacterii atipice pentru piele pe suprafața acesteia - după un timp astfel de microbi dispar. Metodele de evaluare a funcției bactericide a pielii se bazează pe acest principiu.
Membrana mucoasă. Majoritatea infecțiilor nu încep de la piele, ci de la mucoasele. Acest lucru se datorează, în primul rând suprafata mai mare suprafețele lor (mucoase cca 400 m 2, piele cca 2 m 2), în al doilea rând, cu o protecție mai redusă.
Membranele mucoase nu au epiteliu scuamos stratificat. Pe suprafața lor există un singur strat de celule epiteliale. În intestin, acestea sunt epiteliu columnar cu un singur strat, celule secretoare caliciforme și celule M (celule epiteliale membranare), situate în stratul de celule epiteliale, care acoperă acumulările limfoide. Celulele M sunt cele mai vulnerabile la pătrunderea multor microorganisme patogene datorită unui număr de caracteristici: prezența unor receptori specifici pentru unele microorganisme (Salmonella, Shigella, Escherichia patogenă etc.), care nu se găsesc pe enterocitele învecinate; stratul mucos subțire; capacitatea de endocitoză și pipocitoză, care asigură transportul facilitat al antigenelor și microorganismelor din tubul intestinal în țesutul limfoid asociat mucoasei (vezi capitolul 12); absența unui aparat lizozomal puternic, caracteristic macrofagelor și neutrofilelor, datorită căruia bacteriile și virușii se deplasează în spațiul subepitelial fără distrugere.
Celulele M aparțin unui sistem format evolutiv de transport facilitat al antigenelor către celulele imunocompetente, iar bacteriile și virusurile folosesc această cale pentru translocarea lor prin bariera epitelială.
Celulele epiteliale, asemănătoare cu celulele M intestinale, asociate cu țesutul limfoid, sunt prezente în mucoasele arborelui bronhoalveolar, nazofaringe și în sistemul reproducător.
Rezistența la colonizare a epiteliului tegumentar. Orice proces infecțiosîncepe cu aderarea agentului patogen la
suprafața celulelor epiteliale sensibile (cu excepția microorganismelor transmise prin mușcături de insecte sau pe verticală, adică de la mamă la făt). Abia după ce au câștigat un punct de sprijin, microbii dobândesc capacitatea de a se înmulți la poarta de intrare și de a forma o colonie. Toxinele și enzimele de patogenitate se acumulează în colonie în cantități necesare depășirii barierei epiteliale. Acest proces se numește colonizare. Rezistența la colonizare este înțeleasă ca rezistența epiteliului pielii și mucoaselor la colonizarea de către microorganisme străine. Rezistența la colonizare a membranelor mucoase este asigurată de mucină, secretată de celulele caliciforme și formând un biofilm complex la suprafață. Toate instrumentele de protecție sunt încorporate în acest biostrat: microfloră rezidentă, substanțe bactericide (lizozimă, lactoferină, metaboliți toxici ai oxigenului, azotului etc.), imunoglobuline secretoare, fagocite.
Rolul microflorei normale(vezi capitolul 4.3). Cel mai important mecanism pentru participarea microflorei rezidente la rezistența la colonizare este capacitatea lor de a produce bacteriocine (substanțe asemănătoare antibioticelor), acizi grași cu lanț scurt, acid lactic, hidrogen sulfurat și peroxid de hidrogen. Lacto-, bifidobacteriile și bacteriidele au aceste proprietăți.
Datorită activității enzimatice a bacteriilor anaerobe din intestin, acizii biliari sunt deconjugați pentru a forma acid deoxicolic, care este toxic pentru bacteriile patogene și oportuniste.
Mucinîmpreună cu polizaharidele produse de bacteriile rezidente (în special, lactobacili), formează un gliconalix pronunțat (biofilm) pe suprafața membranelor mucoase, care ecranează eficient locurile de aderență și le face inaccesibile bacteriilor aleatorii. Celulele caliciforme formează un amestec de sialo- și sulfomicine, al căror raport variază în diferite biotone. Compoziția unică a microflorei în diferite nișe ecologice este în mare măsură determinată de cantitatea și calitatea mucinei.
Celulele fagocitare și produsele lor de degranulare. Macrofagele și neutrofilele migrează în biostratul mucos de pe suprafața epiteliului. Odată cu fagocitoza, aceste celule secretă biocid
produse exterioare conținute în lizozomii acestora (lizozimă, peroxidază, lactoferină, defensine, metaboliți toxici de oxigen și azot), care cresc proprietățile antimicrobiene ale secrețiilor.
Factori chimici și mecanici.În rezistența epiteliului tegumentar al mucoaselor, un rol important îl joacă secrețiile care au proprietăți biocide și antiadezive pronunțate: lacrimi, salivă, suc gastric, enzime și acizi biliari ai intestinului subțire, secreții cervicale și vaginale ale sistemul reproducător feminin.
Datorită mișcărilor direcționate - peristaltismul mușchilor netezi din intestine, cilii epiteliului ciliat din tractul respirator, urină în sistem urinar- secretiile rezultate, impreuna cu microorganismele continute de ele, se deplaseaza in directia de iesire si sunt scoase la exterior.
Rezistența la colonizare a membranelor mucoase este sporită de imunoglobulinele A secretorii, sintetizate de țesutul limfoid asociat mucoasei.
Epiteliul tegumentar al căilor mucoase se regenerează constant datorită celulelor stem situate în grosimea membranelor mucoase. În intestin, această funcție este îndeplinită de celulele cripte, în care, împreună cu celulele stem, sunt localizate și celulele Paneth - celule speciale care sintetizează proteine antibacteriene (lizozimă, peptide cationice). Aceste proteine protejează nu numai celulele stem, ci și celulele epiteliale tegumentare. Odată cu inflamația în peretele membranei mucoase, producția acestor proteine crește.
Rezistența la colonizare a epiteliului tegumentar este asigurată de întregul set de mecanisme de protecție ale imunității înnăscute și dobândite (imunoglobuline secretoare) și stă la baza rezistenței organismului la majoritatea microorganismelor care trăiesc în Mediul extern. Absența receptorilor specifici pentru anumite microorganisme de pe celulele epiteliale pare a fi mecanismul de bază al rezistenței genetice a animalelor dintr-o specie la microbii care sunt patogeni pentru animalele din altă specie.
9.2.2. Factori celulari
Neutrofile și macrofage. Capacitatea de endocitoză (absorbția particulelor cu formarea unei vacuole intracelulare) este
produs de toate celulele eucariote. Acesta este cât de multe microorganisme patogene pătrund în celule. Cu toate acestea, în majoritatea celulelor infectate nu există mecanisme (sau sunt slabe) care să asigure distrugerea agentului patogen. În procesul de evoluție, în corpul organismelor multicelulare s-au format celule specializate cu sisteme puternice de distrugere intracelulare, a căror „profesie” principală este fagocitoza (din greacă. phagos- Devorez, citos- celulă) - absorbția particulelor cu diametrul de cel puțin 0,1 microni (spre deosebire de pinocitoză - absorbția particulelor cu diametru mai mic și a macromoleculelor) și distrugerea microbilor capturați. Leucocitele polimorfonucleare (în principal neutrofile) și fagocitele mononucleare (aceste celule sunt uneori numite fagocite profesionale) au aceste proprietăți.
Pentru prima dată ideea de rol protector celulele mobile (micro- și macrofage) a fost formulată în 1883 de I.I. Mechnikov, care a primit Premiul Nobel în 1909 pentru crearea teoriei celular-umorale a imunității (în colaborare cu P. Ehrlich).
Neutrofilele și fagocitele mononucleare au o origine mieloidă comună din celula stem hematopoietică. Cu toate acestea, aceste celule diferă într-un număr de proprietăți.
Neutrofilele sunt populația cea mai numeroasă și mobilă de fagocite, a cărei maturare începe și se termină în măduva osoasă. Aproximativ 70% din toate neutrofilele sunt stocate ca rezervă în depozitele măduvei, de unde, sub influența unor stimuli corespunzători (citokine proinflamatorii, produse de origine microbiană, componenta C5a a complementului, factori de stimulare a coloniilor, corticosteroizi, catecolamine) se pot deplasa de urgență prin sânge până la locul distrugerii țesuturilor și pot participa la dezvoltarea răspunsului inflamator acut. Neutrofilele sunt „echipa de răspuns rapid” în sistemul de apărare antimicrobiană.
Neutrofilele sunt celule cu viață scurtă, durata lor de viață este de aproximativ 15 zile. Din măduva osoasă intră în sânge ca celule mature care și-au pierdut capacitatea de diferențiere și proliferare. Din sânge, neutrofilele se deplasează în țesuturi, unde fie mor, fie ies la suprafața membranelor mucoase, unde își încheie ciclul de viață.
Fagocitele mononucleare sunt reprezentate de promonocitele măduvei osoase, monocitele din sânge și macrofagele tisulare. Monocitele, spre deosebire de neutrofile, sunt celule imature care, atunci când intră fluxul sanguinși mai departe în țesut, se maturizează în macrofage tisulare (pleurale și peritoneale, celule Kupffer ale ficatului, alveolare, celule interdigitale ale ganglionilor limfatici, măduvă osoasă, osteoclaste, microgliocite, celule mezangiale ale rinichilor, celule Sertoli ale testiculelor, Langerhans). și celulele Greenstein ale pielii). Durata de viață a fagocitelor mononucleare este de la 40 la 60 de zile. Macrofagele nu sunt celule foarte rapide, dar sunt împrăștiate în toate țesuturile și, spre deosebire de neutrofile, nu au nevoie de o mobilizare atât de urgentă. Dacă continuăm analogia cu neutrofilele, atunci macrofagele din sistemul imunitar înnăscut sunt „forțe speciale”.
O caracteristică importantă a neutrofilelor și macrofagelor este prezența în citoplasma lor a unui număr mare de lizozomi - granule cu dimensiunea de 200-500 nm care conțin diverse enzime, produse bactericide și biologic active (lizozimă, mieloperoxidază, defensine, proteine bactericide, lactoferină, proteinaze, catepsine, colagenază etc.) d.). Datorită unor „arme” atât de diverse, fagocitele au un potențial distructiv și de reglementare puternic.
Neutrofilele și macrofagele sunt sensibile la orice modificări ale homeostaziei. În acest scop, ele sunt echipate cu un arsenal bogat de receptori localizați pe membrana lor citoplasmatică (Fig. 9.2):
Receptori pentru recunoașterea străină - receptori de tip Toll (Receptor de tip Toll- TLR), descoperit pentru prima dată de A. Poltorak în 1998 la musca fructelor și găsit ulterior în neutrofile, macrofage și celule dendritice. Semnificația descoperirii receptorilor de tip Toll este comparabilă cu descoperirea anterioară a receptorilor de recunoaștere a antigenului în limfocite. Receptorii toll-like nu recunosc antigenele, a căror diversitate în natură este extrem de mare (aproximativ 10 18 variante), ci modele moleculare repetate mai grosoare de carbohidrați și lipide - structuri de model (din engleză. model- model), care nu se află pe celulele corpului gazdă, dar care sunt prezente în protozoare, ciuperci, bacterii, viruși. Repertoriul unor astfel de modele este mic și se ridică la aproximativ 20
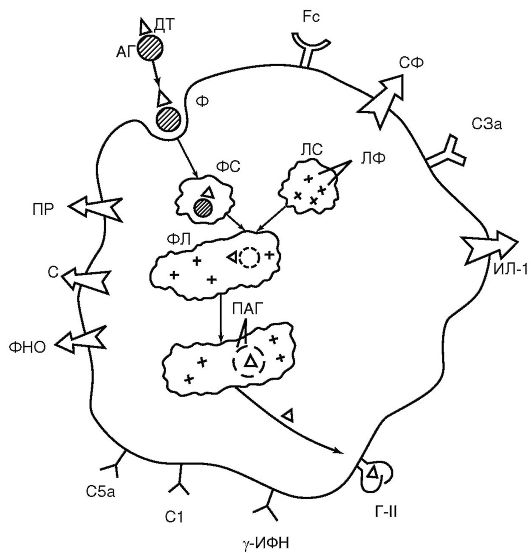 Orez. 9.2. Structuri funcționale ale unui macrofag (diagrama): AG - antigen; DT - determinant antigenic; FS - fagozom; LS - lizozom; LF - enzime lizozomale; PL - fagolizozom; PAG - antigen procesat; G-II - antigen de histocompatibilitate clasa II (MHC II); Fc - receptor pentru fragmentul Fc al moleculei de imunoglobulină; C1, C3a, C5a - receptori pentru componentele complementului; y-IFN - receptor pentru y-MFN; C - secretia componentelor complementului; PR - secreția de radicali peroxid; ILD-1 - secretie; TNF - secreția factorului de necroză tumorală; SF - secretia de enzime
Orez. 9.2. Structuri funcționale ale unui macrofag (diagrama): AG - antigen; DT - determinant antigenic; FS - fagozom; LS - lizozom; LF - enzime lizozomale; PL - fagolizozom; PAG - antigen procesat; G-II - antigen de histocompatibilitate clasa II (MHC II); Fc - receptor pentru fragmentul Fc al moleculei de imunoglobulină; C1, C3a, C5a - receptori pentru componentele complementului; y-IFN - receptor pentru y-MFN; C - secretia componentelor complementului; PR - secreția de radicali peroxid; ILD-1 - secretie; TNF - secreția factorului de necroză tumorală; SF - secretia de enzime
riants. Taxă receptorii asemănători sunt o familie de glicoproteine membranare; sunt cunoscute 11 tipuri de astfel de receptori, capabili să recunoască întreaga paletă model-structuri ale microorganismelor (lipopolizaharide, glico-, lipoproteine-
da, acizi nucleici, proteine șoc termic etc.). Interacțiunea receptorilor Toll-like cu liganzi adecvați declanșează transcrierea genelor pentru citokine proinflamatorii și molecule co-stimulatoare, care sunt necesare pentru migrare, aderență celulară, fagocitoză și prezentarea antigenelor la limfocite;
Receptori manoză-fucoză care recunosc componentele carbohidrate ale structurilor de suprafață ale microorganismelor;
Receptori pentru gunoi (receptor scavenger)- pentru legarea membranelor fosfolipide și a componentelor propriilor celule distruse. Participa la fagocitoza celulelor deteriorate și pe moarte;
Receptori pentru componentele complementului C3b și C4b;
Receptori pentru fragmentele Fc ale IgG. Acești receptori, ca și receptorii pentru componentele complementului, joacă un rol important în legarea complexelor imune și fagocitoza bacteriilor marcate cu imunoglobuline și complement (efect de opsonizare);
Receptori pentru citokine, chemokine, hormoni, leucotriene, prostaglandine etc. vă permit să interacționați cu limfocitele și să răspundeți la orice modificări ale mediului intern al corpului.
Funcția principală a neutrofilelor și macrofagelor este fagocitoza. Fagocitoza este procesul de absorbție a particulelor sau a complexelor macromoleculare mari de către o celulă. Constă din mai multe etape succesive:
Activare și chemotaxie - mișcarea țintită a unei celule spre obiectul fagocitozei către o concentrație crescândă de chemoatractanți, al căror rol îl joacă chemokinele, componente ale complementului și celulele microbiene, produse de degradare a țesuturilor corpului;
Adeziunea (atașarea) particulelor la suprafața fagocitei. Receptorii Toll-like joacă un rol important în aderență, precum și receptorii pentru fragmentul Fc al imunoglobulinei și componenta C3b a complementului (această fagocitoză se numește imună). Componentele complementului imunoglobulinelor M, G, C3b, C4b sporesc aderența (sunt opsonine) și servesc ca punte între celula microbiană și fagocit;
Absorbția particulelor, imersiunea lor în citoplasmă și formarea unei vacuole (fagozom);
Uciderea (uciderea) și digestia intracelulară. După absorbție, particulele de fagozom se contopesc cu lizozomi - se formează un fagolizozom, în care bacteriile mor sub influența produșilor bactericide ai granulelor (sistem bactericid independent de oxigen). În același timp, consumul de oxigen și glucoză în celulă crește - se dezvoltă așa-numita explozie respiratorie (oxidativă), care duce la formarea de metaboliți toxici ai oxigenului și azotului (H 2 O 2, anion superoxid O 2, acid hipocloros, piroxinitrit), care sunt foarte bactericide (sistem bactericid dependent de oxigen). Nu toate microorganismele sunt sensibile la sistemele bactericide ale fagocitelor. Gonococii, streptococii, micobacteriile și altele supraviețuiesc după contactul cu fagocitele; o astfel de fagocitoză se numește incompletă.
Fagocitele, pe lângă fagocitoză (endocitoză), își pot desfășura reacțiile citotoxice prin exocitoză - eliberându-și granulele în exterior (degranulare) - astfel fagocitele efectuează uciderea extracelulară. Neutrofilele, spre deosebire de macrofage, sunt capabile să formeze capcane bactericide extracelulare - în timpul procesului de activare, celula aruncă fire de ADN în care se află granule cu enzime bactericide. Datorită adezivității ADN-ului, bacteriile se lipesc de capcane și sunt ucise de enzimă.
Neutrofilele și macrofagele sunt cea mai importantă componentă a imunității înnăscute, dar rolul lor în protecția împotriva diferiților microbi este diferit. Neutrofilele sunt eficiente împotriva infecțiilor cauzate de agenți patogeni extracelulari (coci piogeni, enterobacterii etc.) care induc dezvoltarea unui răspuns inflamator acut. Cooperarea neutrofil-complement-anticorp este eficientă în astfel de infecții. Macrofagele protejează împotriva agenților patogeni intracelulari (micobacterii, rickettsia, chlamydia etc.) care provoacă dezvoltarea inflamației granulomatoase cronice, unde cooperarea macrofag-limfocite T joacă un rol major.
Pe lângă participarea la apărarea antimicrobiană, fagocitele sunt implicate în îndepărtarea celulelor muritoare, vechi și a produselor lor de degradare, a particulelor anorganice (cărbune, praf mineral etc.) din organism. Fagocitele (în special macrofagele) sunt pregătitoare de antigen
constituenți, au o funcție secretorie, sintetizează și secretă gamă largă compuși biologic activi: citokine (interleukine-1, 6, 8, 12, factor de necroză tumorală), prostaglandine, leucotriene, interferoni α și γ. Datorită acestor mediatori, fagocitele participă activ la menținerea homeostaziei, la procesele de inflamație, la răspunsul imun adaptativ și la regenerare.
Eozinofile aparțin leucocitelor polimorfonucleare. Ele diferă de neutrofile prin faptul că au activitate fagocitară slabă. Eozinofilele ingerează unele bacterii, dar distrugerea lor intracelulară este mai puțin eficientă decât cea a neutrofilelor.
Ucigași naturali. Celulele natural killer sunt celule mari asemănătoare limfocitelor care apar din precursorii limfoizi. Se găsesc în sânge și țesuturi, în special în ficat, membrana mucoasă a sistemului reproducător feminin și splină. Celulele ucigașe naturale, precum fagocitele, conțin lizozomi, dar nu au activitate fagocitară.
Celulele ucigașe naturale recunosc și elimină celulele țintă care au markeri modificați sau absenți caracteristici celulelor sănătoase. Se știe că acest lucru se întâmplă în primul rând celulelor care au fost mutate sau infectate de un virus. De aceea, celulele natural killer joacă un rol important în supravegherea antitumorală, distrugerea celulelor infectate cu viruși. Celulele ucigașe naturale își exercită efectul citotoxic cu ajutorul unei proteine speciale, perforina, care, la fel ca complexul de complement de atac membranar, formează pori în membranele celulelor țintă.
9.2.3. Factori umorali
Sistemul de complement. Sistemul de complement este un sistem multicomponent cu auto-asamblare multienzimatică de proteine serice care sunt în mod normal într-o stare inactivă. Când produsele microbiene apar în mediul intern, se declanșează un proces numit activare a complementului. Activarea are loc ca o reacție în cascadă, când fiecare componentă anterioară a sistemului o activează pe următoarea. În timpul auto-asamblarii sistemului, se formează produse active de descompunere a proteinelor, care îndeplinesc trei funcții importante: provoacă perforarea membranei și liza celulară, asigură opsonizarea microorganismelor pentru fagocitoza lor ulterioară și inițiază dezvoltarea reacțiilor inflamatorii vasculare.
Complementul numit „alexin” a fost descris în 1899 de microbiologul francez J. Bordet, iar apoi numit complement de microbiologul german P. Ehrlich (completa- adiţie) ca factor suplimentar faţă de anticorpii care provoacă liza celulară.
Sistemul de complement include 9 proteine principale (denumite C1, C2-C9), precum și subcomponente - produsele de descompunere a acestor proteine (Clg, C3b, C3a etc.), inhibitori.
Evenimentul cheie pentru sistemul de complement este activarea acestuia. Poate apărea în trei moduri: clasic, lectin și alternativ (Fig. 9.3).
Modul clasic.În calea clasică, factorul de activare sunt complexele antigen-anticorp. În acest caz, fragmentul Fc și IgG ale complexelor imune sunt activate de subcomponenta Cr, Cr este scindat pentru a forma Cl, care hidrolizează C4, care este scindat în C4a (anafilotoxină) și C4b. C4b activează C2, care, la rândul său, activează componenta C3 (o componentă cheie a sistemului). Componenta C3 este scindată în anafilotoxină C3a și opsonină C3b. Activarea componentei C5 a complementului este, de asemenea, însoțită de formarea a două fragmente de proteine active: C5a - anafilotoxina, un chemoatractant pentru neutrofile și C5b - care activează componenta C6. Ca rezultat, se formează complexul C5, b, 7, 8, 9, care se numește atac membranar. Faza terminală a activării complementului este formarea unui por transmembranar în celulă și eliberarea conținutului acestuia în exterior. Ca urmare, celula se umflă și se lizează.
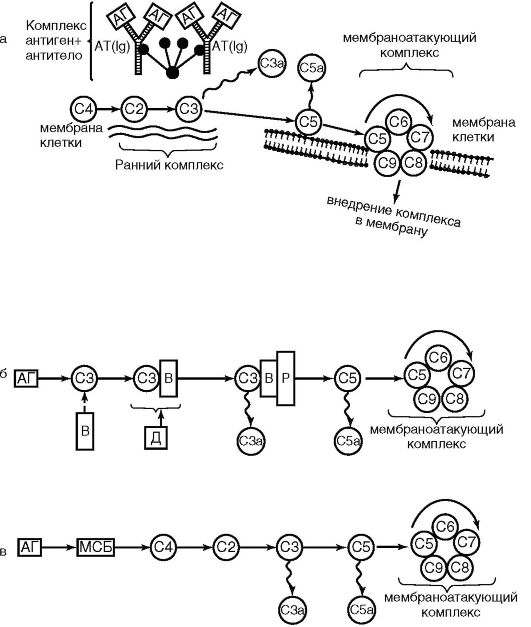 Orez. 9.3. Căile de activare a complementului: clasice (a); alternativa (b); lectină (c); C1-C9 - componente ale complementului; AG - antigen; AT - anticorp; ViD - proteine; P - properdin; MBP - proteina de legare a manozei
Orez. 9.3. Căile de activare a complementului: clasice (a); alternativa (b); lectină (c); C1-C9 - componente ale complementului; AG - antigen; AT - anticorp; ViD - proteine; P - properdin; MBP - proteina de legare a manozei
Calea lectinei. Este în multe privințe similar cu cel clasic. Singura diferență este că în calea lectinei, una dintre proteinele de fază acută, lectina care leagă manoza, interacționează cu manoza de pe suprafața celulelor microbiene (prototipul complexului antigen-anticorp), iar acest complex activează C4 și C2.
Mod alternativ. Apare fără participarea anticorpilor și ocolește primele 3 componente C1-C4-C2. Calea alternativă este inițiată de componente ale peretelui celular al bacteriilor gram-negative (lipopolizaharide, peptidoglicani), virusuri care se leagă secvenţial la proteinele P (properdin), B și D. Aceste complexe transformă direct componenta C3.
O reacție complexă în cascadă a complementului are loc numai în prezența ionilor de Ca și Mg.
Efectele biologice ale produselor de activare a complementului:
Indiferent de cale, activarea complementului se încheie cu formarea complexului de atac membranar (C5, b, 7, 8, 9) și liza celulară (bacterii, eritrocite și alte celule);
Componentele rezultate C3a, C4a și C5a sunt anafilotoxine, se leagă de receptorii bazofilelor din sânge și țesut, inducând degranularea acestora - eliberarea histaminei, serotoninei și a altor mediatori vasoactivi (mediatori ai răspunsului inflamator). În plus, C5a este un chimioatractant pentru fagocite, atrage aceste celule la locul inflamației;
C3b, C4b sunt opsonine, cresc aderența complexelor imune la membranele macrofagelor, neutrofilelor, eritrocitelor și, prin urmare, îmbunătățesc fagocitoza.
Receptori solubili pentru agenți patogeni. Acestea sunt proteine din sânge care se leagă direct la diferite structuri conservatoare, repetate de carbohidrați sau lipide ale celulei microbiene ( model-structuri). Aceste proteine au proprietăți opsonice, unele dintre ele activează complementul.
Partea principală a receptorilor solubili sunt proteinele de fază acută. Concentrația acestor proteine în sânge crește rapid ca răspuns la dezvoltarea inflamației din cauza infecției sau a leziunilor tisulare. Proteinele de fază acută includ:
Proteina C reactivă (alcătuiește cea mai mare parte a proteinelor de fază acută), care și-a primit numele datorită capacității sale
se leagă de fosforilcolină (polizaharidă C) a pneumococilor. Formarea complexului CRP-fosforilcolină promovează fagocitoza bacteriană, deoarece complexul se leagă de Clg și activează calea clasică a complementului. Proteina este sintetizată în ficat, iar concentrația acesteia crește rapid ca răspuns la interleukina-b;
Amiloidul seric P este similar ca structură și funcție cu proteina C reactivă;
Lectina care leagă manoza activează complementul prin calea lectinei și este unul dintre reprezentanții proteinelor colectinei din zer care recunosc reziduurile de carbohidrați și acționează ca opsonine. Sintetizată în ficat;
Proteinele surfactantului pulmonar aparțin, de asemenea, familiei colectinei. Au proprietăți opsonice, în special împotriva ciupercilor unicelulare Pneumocystis carinii;
Un alt grup de proteine de fază acută este format din proteine care leagă fierul - transferină, haptoglobină, hemopexină. Astfel de proteine împiedică proliferarea bacteriilor care necesită acest element.
Peptide antimicrobiene. O astfel de peptidă este lizozima. Lizozima este o enzimă muromidază cu o greutate moleculară de 14.000-16.000, care determină hidroliza mureinei (peptidoglicanului) peretelui celular bacterian și liza acestora. Deschis în 1909 de P.L. Lașcenkov, izolat în 1922 de A. Fleming.
Lizozima se găsește în toate fluidele biologice: ser de sânge, saliva, lacrimi, lapte. Este produs de neutrofile și macrofage (conținute în granulele lor). Lizozima are un efect mai mare asupra bacteriilor gram-pozitive, pe baza peretelui celular al căruia este peptidoglicanul. Pereții celulari ai bacteriilor Gram-negative pot fi, de asemenea, deteriorați de lizozimă dacă acestea au fost expuse anterior la complexul de atac membranar al sistemului complement.
Defensinele și catelicidinele sunt peptide cu activitate antimicrobiană. Sunt formate din celulele multor eucariote și conțin 13-18 resturi de aminoacizi. Până în prezent, sunt cunoscute aproximativ 500 de astfel de peptide. La mamifere, peptidele bactericide aparțin familiilor defensină și catelicidine. Granulele de macrofage și neutrofile umane conțin α-defensine. Ele sunt, de asemenea, sintetizate de celulele epiteliale ale intestinelor, plămânilor și vezicii urinare.
Familia interferonului. Interferonul (IFN) a fost descoperit în 1957 de A. Isaacs și J. Lindeman în timp ce studiau interferența virușilor (din lat. inter- între, ferens- purtător). Interferența este un fenomen în care țesuturile infectate cu un virus devin rezistente la infecția cu un alt virus. S-a descoperit că o astfel de rezistență este asociată cu producerea unei proteine speciale de către celulele infectate, care a fost numită interferon.
În prezent, interferonii sunt bine studiati. Sunt o familie de glicoproteine cu o greutate moleculară de la 15 000 la 70 000. În funcție de sursa de producție, aceste proteine sunt împărțite în interferoni de tip I și de tip II.
Tipul I include IFN α și β, care sunt produse de celulele infectate cu virus: IFN-α de către leucocite, IFN-β de către fibroblaste. În ultimii ani, au fost descriși trei noi interferoni: IFN-τ/ε (IFN derivat din trofoblast), IFN-λ și IFN-K. IFN-α și β sunt implicați în apărarea antivirală.
Mecanismul de acțiune al IFN-α și β nu este asociat cu un efect direct asupra virusurilor. Este cauzată de activarea în celulă a unui număr de gene care blochează reproducerea virusului. Legătura cheie este inducerea sintezei proteinei kinazei R, care perturbă translația ARNm viral și declanșează apoptoza celulelor infectate prin reacții Bc1-2 și dependente de caspază. Un alt mecanism este activarea endonucleazei ARN latente, care determină distrugerea acidului nucleic viral.
Tipul II include interferonul γ. Este produs de limfocitele T și celulele natural killer după stimularea antigenică.
Interferonul este sintetizat constant de către celule; concentrația sa în sânge se modifică în mod normal puțin. Totuși, producția de IF crește atunci când celulele sunt infectate cu viruși sau prin acțiunea inductorilor săi - interferonogeni (ARN viral, ADN, polimeri complecși).
În prezent, interferonii (atât leucocitari, cât și recombinanți) și interferonogenii sunt utilizați pe scară largă în practica clinica pentru prevenirea și tratamentul infecțiilor virale acute (gripa), precum și în scop terapeutic în infecții virale(hepatită B, C, herpes, scleroză multiplă etc.). Deoarece interferonii au nu numai activitate antivirală, ci și antitumorală, ei sunt utilizați și pentru tratarea cancerului.
9.2.4. Caracteristici ale imunității înnăscute și dobândite
În prezent, factorii imunității înnăscute nu sunt de obicei numiți nespecifici. Mecanismele de barieră ale imunității înnăscute și dobândite diferă doar prin precizia acordării la „străin”. Fagocitele și receptorii imuni înnăscuți solubili recunosc „modele”, iar limfocitele recunosc detaliile unei astfel de imagini. Imunitatea înnăscută este o metodă de apărare mai veche din punct de vedere evolutiv, inerentă aproape tuturor ființelor vii, de la organisme multicelulare, de la plante la mamifere, datorită vitezei de reacție la invazia unui agent străin; ea formează baza rezistenței la infecții și protejează organismul. de la majoritatea microbilor patogeni. Numai acei agenți patogeni cărora factorii de imunitate înnăscuți nu le pot face față includ imunitatea limfocitară.
Împărțirea mecanismelor de apărare antimicrobiană în înnăscute și dobândite sau preimune și imune (după R.M. Khaitov, 200b) este condiționată, deoarece dacă luăm în considerare procesul imunitar în timp, atunci ambele sunt verigă din același lanț: mai întâi, fagocitele și receptori solubili pentru model- structuri microbiene, fără o astfel de editare, dezvoltarea ulterioară a unui răspuns limfocitar este imposibilă, după care limfocitele atrag din nou fagocitele ca celule efectoare pentru distrugerea agenților patogeni.
În același timp, împărțirea imunității în înnăscută și dobândită este recomandabilă pentru o mai bună înțelegere a acestui fenomen complex (Tabelul 9.2). Mecanismele de rezistență înnăscută asigură o protecție rapidă, după care organismul își construiește o apărare mai puternică, stratificată.
Tabelul 9.2. Caracteristici ale imunității înnăscute și dobândite
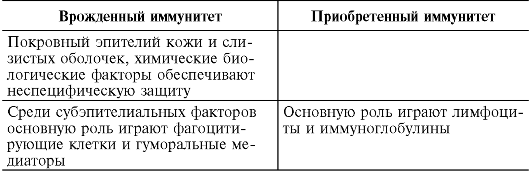 Sfârșitul mesei. 9.2
Sfârșitul mesei. 9.2
 Sarcini pentru auto-pregătire (autocontrol)
Sarcini pentru auto-pregătire (autocontrol)
Multe substanțe și infecții (microorganisme, viruși), care pătrund în organism, provoacă boli. Inamicii interni ai corpului sunt si ei periculosi - celulele sale moarte, canceroase sau infectate cu virusi. Cu toate acestea, corpul nostru este capabil să se protejeze de agenții străini externi și interni. Această abilitate se numește imunitate. Imunitatea este asigurată de sistemul imunitar al organismului. componentele sale sunt leucocitele și organele în care se înmulțesc și se specializează (maturează). Aceasta este măduva osoasă roșie timus(timus), splină, Ganglionii limfaticiși țesuturi limfoide situate în sistemele digestiv, respirator și urinar. Toate leucocitele se formează în măduva osoasă și se maturizează în diferite organe. Din ele, leucocitele circulă împreună cu sângele și limfa și pătrund în țesuturi.
Leucocitele includ mai multe tipuri de celule a diferitelor structuri(limfocite, monocite, eozinofile etc.). Limfocitele sunt împărțite în limfocite T (mature în timus) și limfocite B (mature în măduva osoasă).
Număr semnificativ de leucocite tipuri variate(53-81%) sunt capabili de fagocitoză. Mai multe fagocite sunt localizate în țesuturi conjunctive rinichi, plămâni, ficat, piele.
Imunitatea înnăscută nespecifică
Pielea și mucoasele împiedică pătrunderea străinilor în organism. Peelingul celulelor epiteliale ale pielii moarte și mișcarea vilozităților membranei mucoase le îndepărtează și distrug substanțele bactericide ale secrețiilor glandelor sudoripare și sebacee, mucusul epitelial etc.
Dacă agenții străini au pătruns în organism, li se trimit fagocitele și îi distrug pe agresori. În caz de pătrundere cantitate mare străini sau moartea în masă a fagocitelor în lupta cu ei, măduva osoasă accelerează reproducerea unor astfel de celule și noi forțe devin disponibile pentru a lupta. Asa functioneaza imunitatea celulară. Este strâns legat de factorii de imunitate umorală - anumite proteine care sunt prezente constant în sânge. Unele proteine se atașează de membrana microorganismului, indicând un extraterestru - acest lucru facilitează fagocitoza. Alții sunt implicați în distrugerea membranei celulare străine. Proteinele plasmatice din sânge interferonii ajută organismul să lupte împotriva virușilor.
FagociteȘi
FagociteȘi factori de imunitate umorală, care acționează în prima etapă a luptei, influențează pe toți agresorii în aceleași moduri. Aceste metode de protecție sunt moștenite, adică. congenital. Prin urmare, o astfel de imunitate este numită nespecifică înnăscută.
Imunitatea specifică dobândită. Corpul nu poate face față întotdeauna agenților străini fără ajutorul imunitatea specifică. În consecință, el folosește alte metode - cele care acționează asupra agresorilor în conformitate cu caracteristicile acestora. În aceste reacții specifice ale corpului, se disting și două părți - umorală și celulară. Imunitatea umorală este realizată de limfocitele B, iar imunitatea celulară de limfocitele T.
Factori umorali
Factori umorali anticorpi reacții imune specifice – proteine imunoglobuline. sunt produse de limfocitele B ca răspuns la antigene – substanțe pe care organismul le percepe ca fiind străine. De obicei, acestea sunt anumite proteine din cojile agresorilor sau toxinele pe care le produc. Limfocitele B răspund la fiecare antigen producând un anticorp care corespunde în mod specific acelui antigen. Aceste proteine se combină cu antigenul și formează complexe antigen-anticorp - are loc neutralizarea atât a antigenului, cât și a agresorului.
Legătură celulară
Legătură celulară imunitatea specifică distruge străinii altfel. Astfel, limfocitele T se pot atasa de membranele celulelor afectate de un virus sau bacterii si sa le distruga.
Consecințele distructive Activități Limfocitele T sunt eliminate de fagocitele care devorează agresorii neutralizați și celulele moarte.
Limfocitele care circulă în sânge și fluxul limfatic sunt activate numai atunci când recunosc un antigen. Identificarea lor a antigenului care a intrat prima dată în corpul uman este un proces complex care poate dura până la 14 zile. Consecința acestuia este un răspuns imun, care implică de obicei limfocitele T și B. Limfocitele B recunosc antigenul și încep să sintetizeze anticorpi împotriva acestuia. În același timp, limfocitele B, care sunt și ele sensibile la acest antigen, se înmulțesc în organele sistemului imunitar. Unii dintre ei se alătură atacului umoral, producând anticorpi cu o viteză enormă (până la 30.000 de molecule pe secundă). Alte limfocite B devin celule de memorie. Limfocitele T controlează răspunsul imun prin producerea diferitelor interleukine. Interleukinele pot crește sau scădea activitatea limfocitelor B, pot stimula proliferarea limfocitelor T și formarea celulelor T de memorie sau pot suprima aceste procese.
Celulele de memorie
Celulele de memorie luni de zile, și uneori ani de zile, își păstrează capacitatea de a răspunde la invazia unui antigen „familiar”. Ei nu pierd timpul recunoscându-l, răspunsul imun apare imediat și se produc mai mulți anticorpi. Acesta este modul în care se formează imunitatea specifică dobândită.
Răspuns imun
Răspuns imun la prima întâlnire cu infecția este de obicei însoțită de a nu se simti bine persoană, febră etc. Dacă o persoană a dobândit imunitate la această infecție, simptomele bolii nu sunt observate.
Imunitatea artificială dobândită. Există infecții, prima întâlnire cu care poate fi fatală pentru o persoană. Pentru a crea imunitate împotriva lor, ei sunt vaccinați - un vaccin este introdus în corpul uman. Aceasta este o cantitate mică de agenți patogeni sau substanțe uciși sau slăbiți care sunt produse ale activității lor vitale. O astfel de infecție nu duce la boală. Cu toate acestea, atunci când se administrează un vaccin, se dezvoltă o reacție imună cu drepturi depline: se produc anticorpi specifici acestui agent patogen și se formează celule de memorie. Prin urmare, după vaccinare, organismul întâlnește agenți patogeni vii, invadând complet înarmat. Astfel, prin introducerea vaccinurilor se creează imunitatea artificială dobândită.


